TRAUMA-INDUZIERTE KOAGULOPATHIE (TIC)
Die Trauma-induzierte Koagulopathie (TIC) ist eine häufig auftretende Komplikation bei polytraumatisierten Patienten. Sie ist mit einer erhöhten Mortalität assoziiert und besitzt eine Schlüsselrolle bei der Traumaversorgung. 30 - 40 % aller Patienten, die nach einem Trauma versterben, verbluten in den ersten Stunden. Bei zivilen Traumen in Westeuropa liegt der Prozentsatz der Polytraumatisierten bei etwa 1%. Beim Combat-Trauma ist dieser Anteil mit etwa 10 % deutlich höher.
Hinzu können verzögerte und eingeschränkte Behandlungsmöglichkeiten kommen. Daher ist es im militärischen Setting von besonderer Wichtigkeit, Kenntnisse über Prävention, Diagnostik und Management der TIC zu besitzen. Nur mit einer klaren Strategie kann eine Koagulopathie verhindert bzw. das hämostatische Gleichgewicht wiederhergestellt werden.
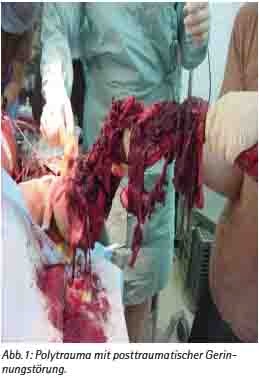
Pathophysiologie der posttraumatischen Gerinnungsstörung
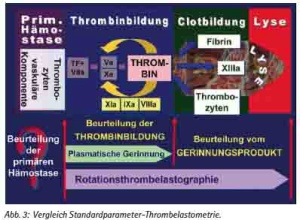
Unsere Vorstellungen vom Gerinnungssystem haben sich in den letzten Jahren dramatisch verändert. Das Konzept der klassischen Gerinnungskaskade mit einem extrinsischen und einem intrinsischen System wurde durch ein dreiphasiges System der zellbasierten Gerinnung ersetzt (Initiation, Amplifikation, Propagation). Damit lässt sich die enge Interaktion zwischen zellulären (Thrombozyten, Erythrozyten, Gefässendothel, -subendothel) und plasmatischen Anteilen besser verstehen.
Jede schwere Blutung führt durch Verlust und Verbrauch zu einer quantitiven Verminderung von Gerinnungsfaktoren. Durch kristalloide und kolloidale Volumenersatzmittel, aber auch durch Erythrozytenkonzentrate wird die Dilution zusätzlich verstärkt. Neben dem reinen Verdünnungseffekt interagieren Kolloide mit der Fibrinpolymerisation, was zu einer verminderten Gerinnselstabilität führt. Hinzu kommen häufig Hypothermie und Azidose, die sich ebenfalls negativ auf die Gerinnung auswirken.
Die TIC setzt häufig so früh nach einem Trauma ein, dass sie sich mit den obigen Ursachen alleine nicht hinreichend erklären lässt. Inzwischen wird sie als eigenständige Entität und als Problem „der ersten Stunde“ verstanden.
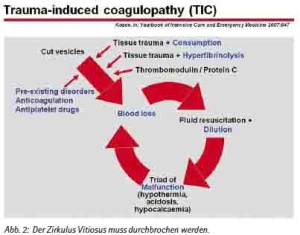
Der primäre Auslöser der TIC ist nach heutiger Auffassung die massive Endothelverletzung mit Freisetzung des TF (Tissue Faktor = Gewebefaktor) in Kombination mit einer systemischen Hypoperfusion. Am Endothel wird dabei Thrombomodulin exprimiert, das mit freiem Thrombin einen stabilen Komplex bildet, der antikoagulatorisch wirkt. Zusätzlich führt dies zur Aktivierung von Protein C, einem effektiven Antikoagulanz. Das hemmt die Faktoren Va und VIIIa, und in der Folge nimmt die Thrombinbildung ab.
Das massive Gewebetrauma in Verbindung mit einem Schock kann zu einer verstärkten Freisetzung von Plasminogenaktivator führen. Dadurch wird vermehrt Plasmin gebildet und die Fibrinolyse in Gang gesetzt. Dies ist an sich ein sinnvoller Mechanismus, um Mikrozirkulationsstörungen nach Aktivierung der Gerinnung rasch zu beseitigen. Insbesondere wenn die Leberperfusion reduziert ist (Schockleber), kann es jedoch zu einer gesteigerten Fibrinolyse kommen, ggfls. zu einer Hyperfibrinolyse (bei 20 – 30 % der Polytraumen) mit verstärkter Blutungsneigung.
Verbrauch, Hämodilution, Hypothermie und Azidose verstärken erst sekundär die Gerinnungsstörung, können sich dann aber zu einem fatalen Zirkulus Vitiosus entwickeln.
Diagnostik der TIC
Die Grundvoraussetzung für ein adäquates Gerinnungsmanagement ist die frühe Diagnostik und Therapiekontrolle.
Die Diagnose traumaassoziierter Gerinnungsstörungen fußt auf einer Kombination klinischer Parameter sowie laborchemischer Befunde. Klinisch fällt bei diesen Patienten eine diffuse mikrovaskuläre Blutung an Wundoberflächen und Schleimhäuten sowie an Kathetereinstichstellen auf.
Standardgerinnungstests
Zur Routinediagnostik gehören Prothrombinzeit/Quick, aPTT sowie die Thrombozytenzahl. Die Bedeutung von Prothrombinzeit/Quick und aPTT wird in der Gerinnungsdiagnostik häufig überschätzt. Normalwerte bedeuten nicht, dass keine vermehrte Blutungsneigung besteht. Eine sichere Korrelation zwischen pathologischen Messwerten und Transfusionsbedarf besteht ebenfalls nicht. Prothrombinzeit/Quick und aPTT wurden vor Jahrzehnten zur Steuerung der Therapie von Cumarinen und unfraktioniertem Heparin entwickelt, was sie auch hervorragend leisten.
Bei beiden Tests wird die Zeit (in Sekunden) bis zum Beginn der Gerinnselbildung gemessen (initiale Thrombusbildung). Diese Zeitwerte haben aber keinerlei Aussagekraft hinsichtlich der primären Hämostase, der Festigkeit sowie der Konstanz des Gerinnsels.
Hinzu kommt, dass innerklinisch der Transport, die Aufbereitung im Labor, das Zentrifugieren und die folgende Analytik zeitintensive Prozesse sind. Auch bei guter Logistik sind 30 – 40 Minuten zu veranschlagen bis die Resultate von Prothrombinzeit/Quick und aPTT vorliegen. Bei dem dynamischen Geschehen einer Polytraumaversorgung ist aber eine schnellere Diagnostik unabdingbar. Eine Hypothermie wird nie berücksichtigt, da die Tests im Labor bei 37°C durchgeführt werden.
Somit kann die Diagnose einer TIC durch die klassischen Laborparameter (Prothrombinzeit/Quick, aPTT, Thrombozytenzahl) nur ungenügend gestellt werden. Der Einsatz von Point-of-care-Diagnostik kann diese diagnostische Lücke größtenteils schließen.
POC (Point-of-Care-Diagnostik)
Hinter dem Begriff POC verbergen sich eine Reihe unterschiedlicher laborchemischer Verfahren, die durch den geschulten Arzt bzw. Pflegepersonal „bettseitig“ ohne zeitlichen Verzug durchgeführt werden können. Allen Verfahren gemeinsam ist, dass sie mit Vollblut arbeiten und keine Zentrifugation benötigen.
In den Bundeswehrkrankenhäusern wie auch im Auslandseinsatz ist als POC-Verfahren die Rotationsthrombelastometrie mit dem ROTEM® eingeführt. Damit kann „bettseitig“ Entstehung, Stabilität und Auflösung eines Gerinnsels erfasst und graphisch dargestellt werden.
Rotationsthrombelastometrie (ROTEM®)
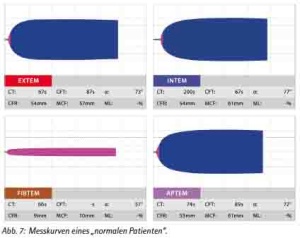
Die Thrombelastometrie ist ein POC-Verfahren zur raschen Gerinnungsanalytik. Im Unterschied zu den Standardgerinnungstests wird hier nicht nur die Zeit bis zum Einsetzen der Gerinnung, sondern auch die Geschwindigkeit der Clotbildung sowie die maximale Festigkeit und Stabilität des Gerinnsels erfasst. Dies wird idealerweise bereits im Schockraum durchgeführt, so dass nach wenigen Minuten Laufzeit mit einem Blick auf die Messkurven des ROTEMs bereits Therapieentscheidungen gefällt werden können.
Ein weiterer Vorteil ist das Erkennen einer gesteigerten Fibrinolyse. Hierzu gibt es an Standardtests keine Alternativen. Im ROTEM® lassen sich bei etwa 20 % der Schockraumpatienten Hyperfibrinolysen nachweisen. Die Zahl der okkulten Hyperfibrinolysen liegt noch weit höher.
Als Untersuchungsmaterial wird Citratblut verwendet. Die Messung wird standardmässig bei 37°C durchgeführt, daher fallen hypothermiebedingte Koagulopathien nicht in das diagnostische Spektrum. Das Gerät bietet aber prinzipiell die Möglichkeit bei niedrigeren Temperaturen zu messen.
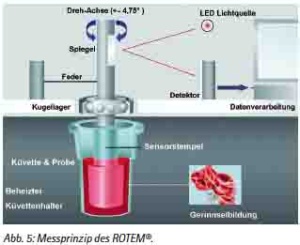
Das Messprinzip des ROTEM® basiert auf einer Testküvette mit Citratblut, in der sich ein Stempel mit einer definierten Geschwindigkeit dreht. Nach Zugabe verschiedener Aktivatoren startet die Gerinnung. Die Viskosität nimmt zu, und der Widerstand, den der Stempel zur Rotation in der Küvette aufbringen muss, vergrößert sich. Diese Drehmomentsveränderung wird graphisch gegen die Zeit aufgetragen.
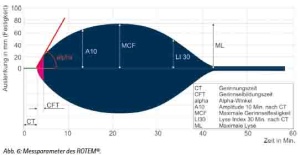
Standardmässig werden drei oder vier Testansätze gleichzeitig durchgeführt. Jeder Testansatz wird nach folgenden Messparametern beurteilt:
CT-Wert (Coagulation Time):
Zeitspanne (in Sekunden) zwischen Gerinnungaktivierung und Start der Gerinnselbildung (je kürzer, desto besser).
CFT-Wert (Clot Formation Time):
Zeitspanne zwischen Start der Gerinnselbildung und Erreichen der Amplitude von 20 mm, Mass für die Geschwindigkeit der Gerinnselbildung.
Amplitude (A):
Stand der Messkurve zu einem bestimmten Zeitpunkt (z. B. A10, Amplitude nach 10 Min., A20, usw.).
Alpha Winkel:
Mass für die Steilheit der Kurve, Mass für die Geschwindigkeit der Gerinnselbildung.
MCF (Maximum Clot Firmness):
Maximale Festigkeit des Gerinnsels in mm (je dicker, desto fester der Clot).
LI (Lyse Index):
Prozentuale Abnahme der Gerinnselfestigkeit durch Fibrinolyse. Höhe der Amplitude nach 60 Min. im Verhältnis zum MCF; ist der Lyse Index unter 85 % handelt es sich um einen instabilen Clot und eine vorzeitige Lyse.
Folgende Testansätze stehen zur Verfügung und werden im Kontext beurteilt. Vier Testansätze können am Gerät gleichzeitig durchgeführt werden.
EXTEM:
Gerinnungsaktivierung mit Tissue Faktor, die CT entspricht hier weitgehend der Prothrombinzeit, nicht heparinsensibel.
INTEM:
Gerinnungsaktivierung mit Kaolin, CT entspricht hier weitgehend der aPTT, heparinsensibel.
FIBTEM:
Die Gerinnselfestigkeit wird zu etwa 80 % von den Thrombozyten beeinflusst. Beim FIBTEM wird der Einfluss der Thrombozyten pharmakologisch gehemmt. Übrig bleibt der rein plasmatische Anteil an der Gerinnselfestigkeit. Beurteilung hier nur der MCF. Sensibel auf Fibrinogenmangel/-polymerisationsstörungen.
APTEM:
Dieser Test entspricht einem EXTEM unter Zugabe des Fibrinolyseinhibitors Aprotinin. Die Beurteilung erfolgt nur im Vergleich zum EXTEM. Kann eine dort beobachtete Hypokoagubilität im APTEM verbessert oder ausgeglichen werden, gilt dies als ein Zeichen für eine Hyperfibrinolyse.
HEPTEM:
INTEM mit Zusatz Heparinase, Einsatz bei verlängerter CT im INTEM; falls Heparin die Ursache, verkürzt sich die CT.
Die Bedienung des ROTEM® ist leicht erlernbar. Der Bediener wird durch das Menü geführt. Fehlbedienungen sind grundsätzlich möglich (z. B. Fehlpipettierungen, falsches Anstecken der Cups, Messküvetten). So sind Messergebnisse mit undulierenden Wellen oder stufenförmige Kurven als Messfehler zu verwerfen. Eine Nulllinie bedeutet nicht unbedingt eine Fehlmessung. Wie immer sind Routine und Übung für Durchführung und Interpretation der Messkurven unerlässlich.
Einsatz des ROTEM®
Die Stärke des ROTEM® liegt in der Beurteilung der Dynamik und Qualität der gesamten Gerinnung (Gerinnungsinitiation, Gerinnselbildung, Gerinnselstabilität) sowie in der Erfassung einer vorzeitigen Lyse. Mit dem ROTEM® lassen sich innerhalb von Minuten Fibrinogenmangel, Fibrinpolymerisationsstörungen, Thrombozyten-, Faktorendefizit und Hyperfibrinolysen differenzieren. Damit rückt die Thrombelastometrie zunehmend in den Focus von Diagnostik und Therapie massiver Blutungen. Die Messkurven ermöglichen auch erstmalig eine zielgerichtete Therapie (early goal-directed therapy) mit Gerinnungsfaktorenkonzentraten.
Die Schwere des Injury Severity Score wie auch Messergebnisse des ROTEM® lassen eine Vorhersage für den Verbrauch von Blutprodukten zu. So ist eine Massivtransfusion zu erwarten, wenn man initial im Schockraum nach 10 min (A10) im EXTEM eine Clotdicke von < 25 mm und im FIBTEM von < 3 mm mißt.
Der zunehmende Einsatz der POC-gesteuerten Gerinnungstherapie mit dem ROTEM® senkt einerseits die Transfusionsrate allogener Blutprodukte (massgeblich FFP und EK und damit auch deren unerwünschten Wirkungen), während es andererseits zu einem signifikanten Mehrverbrauch an Gerinnungsfaktorenkonzentraten (hauptsächlich Fibrinogen und PPSB) kommt. Dies kommt der Situation im Auslandseinsatz entgegen, wo Faktorenkonzentrate problemlos gelagert werden können, Erythrozytenkonzentrate aber eine limitierte Ressource darstellen und Thrombozytenkonzentrate nur begrenzt zum Einsatz kommen können.
Störungen der primären Hämostase werden bei der Thrombelastometrie nicht erfasst (vWillebrand-Syndrom, Thrombozytopathien). Das erfordert im Inland ggfls. eine zusätzliche Thrombozytenfunktionsdiagnostik.
Unauffällige ROTEM®-Messkurven schließen daher eine Störung der Hämostase nicht aus. Der Patient sollte immer aufgrund seines klinischen Bildes und nie allein aufgrund eines Gerinnungsbefundes therapiert werden.
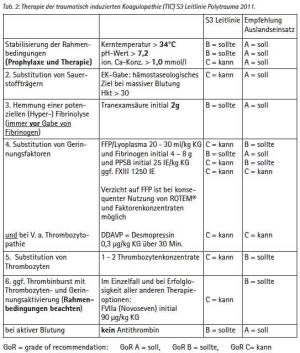
Therapeutische Maßnahmen bei der TIC
Optimierung der Rahmenbedingungen
Die Aufrechterhaltung bzw. aggressive Korrektur der sogenannten hämostaseologischen Rahmenbedingungen ist eine Basismaßnahme jeder Gerinnungstherapie.
Damage Control Surgery
Die chirurgische, ggf. interventionelle Blutstillung ist eine Basismassnahme für die Therapie der TIC. Keine hämostaseologische Massnahme alleine kann eine chirurgische Blutung stoppen.
Damage-Control-Surgery bedeutet schnelle chirurgische Blutstillung durch Gefäßnaht, Abklemmung, Kompression, Fixateur externe. Damit wird eine definitive anatomische Versorgung zugunsten einer raschen Blutungs- und Kontaminationskontrolle zurückgestellt. Wenn die physiologischen Rahmenbedingungen wieder erreicht sind, erfolgt die definitive operative Versorgung zu einem späteren Zeitpunkt. Mit diesem Vorgehen konnte die Mortalität deutlich gesenkt werden.
Damage control resuscitation (DCR)
Analog zum Prinzip der Damage Control Surgery wurde zur Therapie der TIC das Konzept der Damage Control Resuscitation entwickelt.
Diese Strategie beeinhaltet einen restriktiven Volumenersatz, die permissive Hypotension, das (Wieder)-Erwärmen, den Ausgleich von Azidose und Hypokalzämie, die Transfusion von Blutprodukten sowie die Substitution gerinnungsaktiver Produkte (haemostatic resuscitation).
Diese Maßnahmen sollten so früh wie möglich erfolgen und engmaschig überwacht werden.
Volumentherapie
Die Volumensubstitution zur Aufrechterhaltug der Gewebeperfusion ist ein elementarer Bestandteil der Traumatherapie. Allerdings ist dabei eine Dilution der verbleibenden Gerinnungsfaktoren unvermeidlich. Es besteht ein signifikanter Zusammenhang zwischen der Menge des substitutierten Volumens und dem Ausprägungsgrad der Koagulopathie. Eine präklinische Volumengabe von mehr als 3 000 ml und ein Kolloid / Kristalloid Verhältnis von > 1:2 sind unabhängige Risikofaktoren für die Entstehung einer TIC.
Zur Volumentherapie gehören kristalloide sowie kolloidale Lösungen. Die kolloidalen Lösungen beeinflussen Thrombozytenfunktion und Clotstabilität negativ. Dies gilt auch für die neueren HAES–Produkte. Bei Gelatine-Präparaten scheint dieser Effekt etwas geringer ausgeprägt zu sein. Der Volumenersatz sollte primär mit kristalloiden Lösungen erfolgen.
Die einmalige Applikation hyperosmolarer Lösungen scheint die Gerinnselbildung ebenfalls in geringem Maß zu beeinträchtigen.
Permissive Hypotension
Bei aktiver Blutung soll bis zum Erreichen einer chirurgischen Blutstillung ein niedriger Blutdruck nicht nur toleriert, sondern ggfls. aktiv angestrebt werden. Dadurch wird einerseits der Blutverlust reduziert, andererseits kann der Volumenersatz und damit die Dilution geringer gehalten werden.
Es gibt keinen endgültigen Konsens darüber, in welcher Höhe der Blutdruck von Traumapatienten gehalten werden sollte. Bis zur chirurgischen Blutstillung wird ein mittlerer arterieller Druck von 60 - 65 mmHg empfohlen. Möglicherweise ist bei Patienten ohne Schädel-Hirn-Trauma oder koronarer Herzkrankheit die Mortalität bei 50 mmHg sogar geringer. Bei Verletzungen des zentralen Nervensystems sind höhere RR-Werte anzustreben.
Hypothermie
Ein massives Trauma führt immer zu einer deutlichen Beeinträchtigung der körpereigenen Thermoregulation. Das Entkleiden für den „Body Check“ verstärkt die Auskühlung noch.
Eine Körpertemperatur < 35 °C verlangsamt die primäre Hämostase sowie die plasmatische Gerinnung. Pro 1°C Temperaturverlust reduziert sich die Aktivität der Gerinnungsfaktoren um 10 %. Aggraviert wird die hypothermiebedingte Thrombozytopathie durch die Sequestration der Thrombozyten in Milz und Leber.
Die Bemühungen müssen initial darauf abzielen, die Körpertemperatur im Normbereich zu halten. Volumenersatzmittel und Erythrozytenkonzentrate sind mittels Wärmesystemen (z. B. Level 1®) zu infundieren. Die Entkleidung des traumatisierten Patienten ist zwar obligat, unnötige Kälteexposition aber zu vermeiden. Die Temperatur während des Transports sowie im Schockraum sollte angehoben werden (bis zu 28°). Eine Temperaturmonitoring ist obligat.
Azidose
Hypovolämie und die damit einhergehende Minderperfusion des Gewebes generieren zwangsläufig eine Azidose. Eine Azidose von < 7,2 beeinflusst die primäre Hämostase und führt zu einer signifikanten Reduktion der thrombozytären Adhäsions- und Aggregationsfähigkeit. Gleichzeitig wird auch die Geschwindigkeit der Thrombinbildung reduziert. Da die gestörte Mikroperfusion die Ursache der Azidose ist, wird diese bis zur Wiederherstellung einer suffizienten Gewebedurchblutung anhalten. Eine Pufferung führt als Einzelmassnahme zu keiner Gerinnungsverbesserung, ist aber bei Gabe von Gerinnungsfaktoren sinnvoll, da diese in ihrer Wirkung pH-abhängig sind.
Auch Transfusionen erhöhen die Belastung mit sauren Valenzen (der BE von frischen EK liegt bei -20 mmol/l, der von EK nahe dem Verfalldatum bei -50 mmol/l). Bei einem BE von -15 mmol/l liegt die Aktivität der Gerinnungsfaktoren nur noch bei 50 %. Der Base Excess (BE) ist ein prognostischer Parameter für die Mortalität.
Kalzium (Faktor IV)
Kalzium ist als Cofaktor essentiell für die Gerinnung. Die Reduktion des ionisierten Kalziums nach Transfusionen ist durch das als Antikoagulanz genutzte Zitrat bedingt. Sie tritt bei Frischplasmen eher und massiver auf als bei Erythrozytenkonzentraten. Dabei ist die Abnahme umso deutlicher, je schneller die Produkte transfundiert werden (> 50 ml/min). Es besteht ein inverses Verhältnis zwischen Laktat und Kalzium, so dass sich bei metabolischer Azidose eine relevante Hypokalzämie entwickelt.
Die Plasmakonzentration des ionisierten Kalziums sollte über 1,0 mmol/L gehalten werden.
Substitution von Blutprodukten
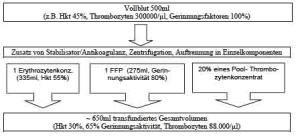
Warmblut
Innerhalb der ersten sechs Stunden nach der Spende wird das Vollblut als Warmblut bezeichnet. Die Verwendung von Warmblut begann im 1. Weltkrieg und ist bis zum heutigen Tag im militärischen Bereich eine bedeutende Notfalloption.
Physiologisch betrachtet wäre die Transfusion von Warmblut ideal: der Traumapatient erhielte genau das zurück, was er verloren hat. Wegen der damit verbundenen Transfusionsrisiken steht diese Option im Inland jedoch nicht zur Verfügung. Im Auslandseinsatz bleibt es eine Notfalloption.
Die Thrombozytenfunktion ist beim Warmblut noch erhalten. Falls besonderer Wert auf die Transfusion funktionstüchtiger Thrombozyten gelegt wird, darf das Warmblut nicht leukozytenfiltriert werden. Sonst werden 90 % der Thrombozyten mit den Leukozyten mitfiltriert. Hier ist eine strenge Nutzen-Risiko-Abwägung unerlässlich.
Im Normalfall wird auf die Einzelkomponenten des Vollblutes, dem Erythrozytenkonzentrat, dem Frischplasma sowie dem Thrombozytenkonzentrat zurückgegriffen.
Die Kombination dieser Einzelkomponenten entspricht nicht mehr der Wirksamkeit von Vollblut:
Erythrozyten
Die wichtigste Funktion der Erythrozyten beim Trauma liegt in der Aufrechterhaltung eines adäquaten globalen Sauerstoffangebots bei einer durch Schock eingeschränkten Mikrozirkulation. Darüberhinaus beeinflussen Erythrozyten jedoch auch die Gerinnung, so dass für eine suffiziente Hämostase auch ein ausreichender Hämatokrit notwendig ist.
Dieser Einfluss ist multifaktorieller Natur. Erythrozyten drängen die Thrombozyten an den Randstrom des Gefässsystems und damit näher an den Ort der Verletzung (Marginalisation). Darüberhinaus haben Erythrozyten einen direkt stimulierenden Effekt auf Thrombozyten: ADP-Freisetzung und Aktivierung von Faktor IX.
Ab einem Hämatokrit von < 20 ist immer mit einer klinisch relevanten Beeinträchtigung der Hämostase zu rechnen. Besteht gleichzeitig eine Thrombozytopenie wird dieser Effekt noch verstärkt.
Die Querschnittsleitlinien für Hämotherapie sehen einen restriktiven Einsatz von Erythrozytenkonzentraten beim normovolämen Patienten vor. In der akute Blutungssituation besteht aber eine Hypovolämie, so dass mit dem Hämatokrit alleine das Ausmaß des Erythrozytendefizits unterschätzt wird. Ein Hämatokrit von 30 sollte daher in der akuten Blutungssituation auch bei sonst gesunden Patienten gehalten werden.
Eine Alternative zur Transfusion von Fremd-Erythrozytenkonzentraten ist der Einsatz des Cell-Saver. Die Qualität der aufbereiteten Erythrozyten ist der von gelagerten Erythrozyten überlegen. Ein Wiederaufbereiten ist allerdings in Deutschland nur zulässig, wenn der OP-Situs nicht kontaminiert ist. Damit entfällt diese Option bei den meisten Traumata.
Antifibrinolytika
Eine systemische überschießende Aktivierung der Fibrinolyse wird als Hyperfibrinolyse bezeichnet und kann durch die Auflösung von gebildeten Gerinnseln und dem Verbrauch des Fibrinogens zu einer lebensbedrohenden Blutung führen. Die Hyperfibrinolyse scheint häufiger zu sein als bislang angenommen. Je schwerer das Verletzungsmuster ist (Injury Severity Score > 16), um so höher ist die Wahrscheinlichkeit einer Hyperfibrinolyse.
Die Thrombelastometrie (ROTEM®) stellt hier den Goldstandard für die Diagnostik dar. Klassische Laborparameter wie z. B. die D-Dimere sind ungeeignet.
Einziges Antifibrinolytikum ist zur Zeit die Tranexamsäure. Bereits bei dem Verdacht auf eine Hyperfibrinolyse sollte die nebenwirkungsarme Tranexamsäure eingesetzt werden. Sie sollte vor Faktorenkonzentraten bzw. Frischplasmen gegeben werden, da sonst bei einer Hyperfibrinolyse die Gerinnungsfaktoren umgehend wieder verbraucht werden.
Besonders wichtig ist der frühe Einsatz. Er sollte innerhalb der ersten drei Stunden nach dem Trauma, besser noch innerhalb der ersten Stunde erfolgen. Damit ist die Tranexamsäure ein Medikament bereits für die Präklinik bzw. den beweglichen Arzttrupp.
Fibrinogen
Fibrinogen (Faktor I) stellt die Endstrecke der Gerinnungskaskade dar, ermöglicht die Gerinnselbildung und gewährt dessen Stabilität. Hohe Fibrinogenspiegel haben eine protektive Wirkung auf das Ausmaß des Blutverlustes. Obwohl 90 % der Gesamtmasse der plasmatischen Gerinnungsfaktoren auf Fibrinogen entfallen, erreicht es im Rahmen einer Blutung oder Dilution seine kritische Konzentration früher als alle anderen Faktoren. Daher sollte frühzeitig mit der Substitution begonnen werden.
Hinzu kommt, dass die Fibrinpolymerisation durch die Gabe von kolloidalen Volumenersatzmitteln beeinträchtigt wird. Gelatine-Präparate besitzen hier offensichtlich Vorteile auch gegenüber HES-Präparaten der neueren Generation.
Grundsätzlich kann Fibrinogen durch Frischplasmen wie auch durch Fibrinogenkonzentrat substituiert werden. Mit dem Konzentrat gelingt dies effektiver und schneller. Die Gabe von Fibrinogen sollte erst nach der Applikation von Tranexamsäure erfolgen.
PPSB
Als Mehrfaktorenpräparat steht in Deutschland der Prothrombinkomplex (PPSB) zur Verfügung, Es enthält die Vitamin-K-abhängigen Faktoren II, VII, IX und X. Zusätzlich werden Gerinnungsinhibitoren wie Protein C, S, Z und AT zugesetzt. Ein wesentlicher Vorteil ist die rasche Verfügbarkeit und vergleichsweise gute Standardisierung des Produkts.
Mit Faktorenkonzentraten lässt sich das Gerinnungspotential effektiver, schneller und mit kleineren Volumina anheben als mit Gefrorenen Frischplasmen. Eine kontinuierliche Gabe per Perfusor ist der Bolusgabe vorzuziehen.
Mittels ROTEM-Messungen können Gerinnungsfaktoren (Fibrinogen, PPSB) so gezielt substitutiert werden, dass dabei teilweise ganz auf Frischplasmen verzichtet werden kann.
Für dieses Point-of-Care-basierte Konzept, das den Schwerpunkt nicht auf Frischplasmen sondern auf Faktorenkonzentrate setzt, konnte bislang noch kein Überlebensvorteil nachgewiesen werden. Es bestach jedoch mit einem deutlich niedrigeren Verbrauch an allogenen Blutprodukten sowie einer geringeren Rate an posttraumatischen Komplikationen.
Früher gefürchtete unerwünschte Ereignisse wie Thrombembolien sind bei den heutigen Präparaten auch bei Gabe größerer Mengen sehr unwahrscheinlich.
PPSB darf nicht mit Kryopräzipitat gleichgestellt werden, das in angelsächsischen Ländern eingesetzt wird. PPSB enthält kein Fibrinogen, keinen Faktor VIII und keinen vWillebrandfaktor.
Gefrorenes Frischplasma (GFP, auch FFP), Lyoplasma
FFP entspricht etwa einer 8 % Eiweisslösung und besteht hauptsächlich aus Wasser, Albumin (40 - 50 g/l), ~ 0,5g Fibrinogen und anderen Plasmaproteinen. Es enthält ein ausgewogenes Verhältnis von pro- und antikoagulatorischen Gerinnungsfaktoren. Schwankungen von 60 % bis 140 % des Normwertes kommen allerdings vor, da das Produkt aus einer Einzelblutspende gewonnen wird, so dass die Qualität vom jeweiligen Einzelspender abhängt.
Die Faktoren V und XI können nur mit FFP substituiert werden. Für diese beiden Faktoren existiert kein Konzentrat.
Gefrorenes Frischplasma steht seit mehr als 60 Jahren zur Verfügung und wurde anfänglich als reines Volumenersatzmittel eingesetzt. Mit der Einführung von Kolloiden veränderte sich die Therapie in Richtung Gerinnungsstörung. Auch heute ist die Gabe von FFP in den meisten Kliniken Standard zur Prophylaxe und Behandlung plasmatischer Gerinnungsstörungen. Die Effektivität bezüglich Reversierung einer klinisch relevanten Gerinnungsstörung und Verringerung des Blutverlusts konnte allerdings trotz jahrzehntelangen Einsatzes nicht nachgewiesen werden. Daher gibt es in zunehmenden Maße Diskussionen darüber, den Einsatz von FFP zugunsten der Faktorenpräparate zurückzunehmen. Die einzig wissenschaftlich belegbare Indikation für FFP liegt bei der Massivtransfusion (ab 10 EK/24h).
In welchem Verhältnis FFP zu Erythrozytenkonzentraten verabreicht werden sollten, ist seit langem in der Diskussion. Im Falle von Massivtransfusionen deutet viel auf den Vorteil eines hohen Verhältnisses von FFP : EK im Bereich von 1:1,5 hin. Die Erfahrungen der US-Streitkräfte aus dem IRAK-Krieg lassen ein nahezu ausgewogenes Verhältnis von EK zu FFP mit einer Letalitätsreduktion verbunden erscheinen.
Therapieschemata mit einem festen Verhältnis von 1 Erythrozytenkonzentrat, 1 FFP plus 1 Thrombozytenkonzentrat hatten ein schlechtes Patientenoutcome zum Ergebnis.
Um klinisch wirksam zu sein, müssen große Mengen FFP transfundiert werden: ~30 ml/kg KG. Selbst dann kann die Konzentration kritisch reduzierter Faktoren nur begrenzt zunehmen (auf etwa 15 – 20 %). Bei diesen Mengen besteht ein nicht unerhebliches Nebenwirkungsrisiko wie z. B. für eine transfusionsbedingte Lungenschädigung (TRALI), eine Infektion oder ein Multiorganversagen.
Die Rate unerwünschter Wirkungen scheint beim Einsatz AB0-identischer Frischplasmen geringer zu sein als bei AB0-kompatiblen Frischplasmen.
FFPs werden tiefgefroren gelagert und sind bei -30 bis -45 °C bis zu zwei Jahre haltbar. Im Auslandseinsatz sind sie aus logistischen Gründen nicht vorrätig. Hier wird das bei Raumtemperatur lagerbare Lyoplasma der Blutgruppe AB vorgehalten. Dabei handelt es sich um gefriergetrocknetes Einzelspenderplasma. Es ist bezüglich der Gerinnungsfaktoren in etwa mit dem Frischplasma gleichzusetzen. Die Indikationsstellung ist identisch.
Faktor XIII
Faktor XIII stabilisiert das Gerinnsel durch Quervernetzung der Fibrinfäden. Er wird durch die klassischen Gerinnungstests wie Quick und PTT nicht erfasst. Faktor XIII lasst sich durch FXIII-Konzentrat substitutieren.
Bleibt die Clotfestigkeit im ROTEM® unter anhaltender und ausreichender Fibrinogengabe bei suffizienter Thrombinbildung unzureichend, liegt der Schluss nahe, dass spezifisch die F XIII Aktivität kritisch vermindert ist.
Desmopressin (DDAVP)
DDAVP führt zu einer Verdreifachung der Konzentration des vWillebrand-Faktor sowie des Faktor VIII aus dem Endothel. Damit wird die Adhäsion und Aggregation der Thrombozyten verbessert, z. B. bei einer medikamentösen Thrombozytopathie durch Acetylsalicylsäure. Es wird in der Regel in Kombination mit Tranexamsäure eingesetzt.
Desmopressin wird als Kurzinfusion über 15 -30 Minuten infundiert und erreicht nach etwa 90 Minuten sein Wirkmaximum. Dies relativiert seinen Wert während des dynamischen Geschehens einer Traumaversorgung.
Desmopressin wirkt in vitro gegen eine hypothermiebedingte Thrombozytopathie.
Thrombozyten
Eine Thrombozytopenie stellt initial beim Trauma meist kein Problem dar, da Thrombozyten aus Milz, Leber und Knochenmark zusätzlich freigesetzt werden können.
Die Verfügbarkeit von Thrombozytenpräparaten ist begrenzt. Angesichts der kurzen Haltbarkeit von vier Tagen sind in vielen Blutbanken keine Thrombozytenkonzentrate (Pool- oder Apheresepräparate) vorrätig. Sie müssen erst zeitintensiv beim zuständigen Blutspendedienst angefordet werden.
Umso schwieriger ist die Versorgung im Auslandseinsatz. Zum Teil kann auf kryokonservierte Thrombozyten von Verbündeten zurückgegriffen werden. Die Qualität dieser Thrombozyten könnte allerdings durch die Kryokonservierung beeinträchtigt sein. Die Möglichkeit der Thrombozytapherese besteht im Auslandseinsatz nicht.
Umso wichtiger ist ein aggressives Gerinnungsmanagement, um einen massiven Abfall der Thrombozytenzahl zu vermeiden.
Die Thrombozytenzahl sollte bei polytraumatisierten Patienten zumindest 50 000/µl, besser 100 000/µl betragen. Für die individuelle Einschätzung der Substitutionsbedürftigkeit können ROTEM®-Messungen wertvolle Hinweise liefern (EXTEM/FIBTEM).
Rekombinanter Faktor VIIa
FVIIa macht im Plasma nur etwa 1 % der Gesamtmenge an FVII aus. Wird er in supraphysiologisch hohen Dosierungen zugeführt, bindet er Tissue Faktor auf Oberflächen aktivierter Thrombozyten, also dort wo eine Gewebeverletzung vorliegt. Über diesen Aktivierungsweg können große Mengen an Thrombin gebildet werden. Außerdem wird eine vorzeitige Lyse des Gerinnsels verhindert.
Der Einsatz von rFVIIa stellt im koagulopathischen Kontext einen off-label-use dar, kann aber in begründeten Einzelfällen lebensrettend sein. Bei Blutungen, die konventionell, chirurgisch oder interventionell radiologisch nicht behandelbar sind und/oder bei Versagen einer umfassend durchgeführten Gerinnungstherapie kann rFVIIa in Erwägung gezogen werden. Für eine erfolgreiche Therapie mit rFVIIa müssen allerdings einige Voraussetzungen erfüllt sein: Hb > 7 g %, Fibrinogen
> 1 g/dl, pH > 7,2, Thrombozyten > 50 000/µl. Auch bei Hypothermie kann der Einsatz erwogen werden, wenn auch unter Normothermie der Thrombinerhalt größer ist.
Im militärischen Setting kommt rFVIIa früher und häufiger zum Einsatz als im Inland.
Algorithmen/Massivtransfusionsprotokoll
Algorithmen sind für ein suffizientes Transfusions- und Gerinnungsmanagement unabdingbar (S3 Leitlinie Polytrauma 2011, European Trauma Guidelines 2013). Bei „blinder“ Therapie wird der Bedarf an Blutprodukten unterschätzt und unzureichend therapiert.
Es existieren verschiedene Algorithmen. Bei den konventionellen Therapieschemata liegt ein Schwerpunkt im großzügigen Einsatz von Frischplasmen. Allerdings existieren keine Zahlen zur Evidenz, obwohl seit Jahrzehnten mittels Frischplasmen Gerinnungsfaktoren substituiert werden. Durch den vermehrten Einsatz der Thrombelastometrie rückt die „goal-directed-therapy“ mit dem Schwerpunkt auf Gerinnungsfaktorenkonzentraten zunehmend in den Fokus.
Bislang existieren beide Therapiealgorithmen nebeneinander, ohne dass die Überlegenheit eines Verfahrens hätte gezeigt werden können. Allerdings wächst die Evidenz hinsichtlich eines bevorzugten Einsatzes von Gerinnungskonzentraten, der durch die Thrombelastometrie (ROTEM®) „goal-directed“ gesteuert wird.
Wehrmedizinische Relevanz
Algorithmen, die im Inland Gültigkeit haben, sollten nicht automatisch unverändert im Auslandseinsatz umgesetzt werden. Im Auslandseinsatz sind die Transportwege des Verwundeten länger und die Ressourcen insbesondere an allogenen Blutprodukten begrenzt. Dies betrifft vor allem Erythrozyten- sowie Thrombozytenkonzentrate. Bei der Traumaversorgung im Auslandseinsatz muss also präklinisch (z. B. beweglicher Arzttrupp) und innerklinisch aggressiver therapiert werden, um die begrenzten Ressourcen zu schonen. Der Einsatz von Faktorenkonzentraten wie Fibrinogen, PPSB, Faktor XIII, rFVIIa und Lyoplasma sollte als Goal-Directed Therapy mittels ROTEM® aggressiver als im Inland erfolgen. Diese Produkte stehen ausreichend zur Verfügung.
Zusammenfassung
Neue Erkenntnisse über die Pathophysiologie der traumainduzierten Koagulopathie haben in den letzten Jahren zu einer Veränderung in der Therapie von Traumapatienten geführt. Die frühe Diagnose und differenzierte Therapie der TIC ist inzwischen essentieller Bestandteil der modernen Traumaversorgung. Im Auslandseinsatz sind die Algorithmen mit dem Schwerpunkt von Einzelfaktorenkonzentraten und Lyoplasmen zu bevorzugen, da diese aus logistischen Gründen ausreichend vorhanden sind. Mittels des ROTEM® kann eine Goal-Directed Therapy durchgeführt werden. Keine der hämostaseologischen Interventionen ist jedoch in der Lage eine chirurgische Blutung alleine zu stoppen.
Literatur beim Verfasser.
Datum: 16.04.2013
Quelle: Wehrmedizin und Wehrpharmazie 2013/1