Einsatz extrakorporaler Lungen Unterstützungssysteme zur Therapie schwerer Gasaustauschstörungen
Eine Option für den Einsatz?
Aus der Abteilung für Anästhesiologie, Intensivmedizin, Notfallmedizin und Rettungsdienst (Ltd. Arzt: Flottenarzt M. Benker) des Bundeswehrkrankenhauses Berlin (Chefarzt: Flottenarzt Dr. K. Reuter)
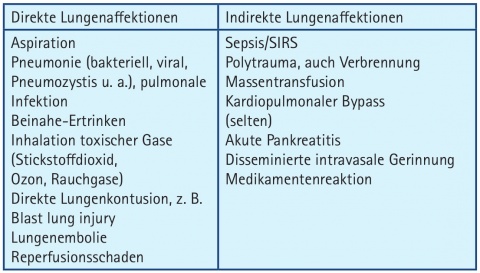
Die Bestandteile des respiratorischen Systems lassen sich vereinfacht in pulmonale und extrapulmonale Anteile unterscheiden. Störungen an jeweils einem oder auch die Kombination von Störungen beider Anteile können zur akuten respiratorischen Insuffizienz führen. Die unterschiedlichsten Ereignisse, sowohl direkte als auch indirekte Lungenaffektionen, können ein akutes Lungenversagen auslösen. Beispiele für die unterschiedlichsten Auslöser sind in Tabelle 1 dargestellt.
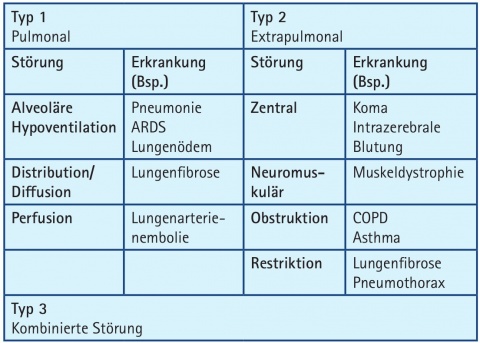
Das akute Lungenversagen wird in drei Typen unterteilt. Diese werden in Tabelle 2 dargestellt.
Beim Typ I steht die Hypoxämie im Vordergrund, da hier das Lungenparenchym geschädigt ist. Bei Typ 2, dem hyperkapnischen Lungenversagen, ist die
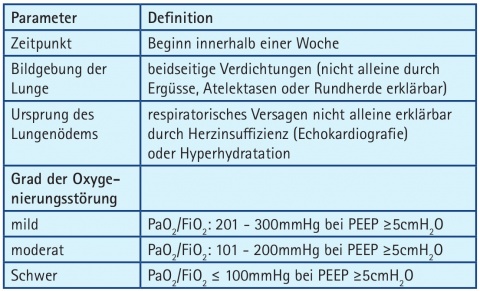
Atempumpe gestört und Typ 3 ist eine kombinierte Störung aus Typ 1 und 2, welche im klinischen Alltag sehr häufig anzutreffen ist [1].Die weitere Unterteilung des akuten Lungenversagens vom Typ 1 und 3 erfolgt nach der im Jahr 2012 publizierten Berlin-Definition in drei Schweregrade [2]. Entscheidend hierbei ist der Oxygenierungsindex (PaO2/FiO2) als Maß für die Schwere der Gasaustauschstörung in Bezug auf die Sauerstoffaufnahme. Ein PEEP[1] von 5cmH2O darf bei der Beurteilung gemäß der Berliner Definition nicht unterschritten werden. Näheres siehe Tabelle 3.
Das akute Lungenversagen gehört zu den wichtigsten intensivmedizinischen Krankheitsbildern [3].
Grundlegendes zur Therapie
Die Therapie des akuten Lungenversagens beinhaltet im wesentlichen fünf Aspekte, welche parallel behandelt werden müssen:• Kausale Therapie des Grundleidens gemäß den entsprechenden Leitlinien
• Beatmungsbehandlung (protektiv/ultraprotektiv)
• Volumenmanagement (Flüssigkeitsrestriktion nach Kreislaufstabilisierung)
• Lagerungstherapie
• Additive Maßnahmen (Surfactant, NO, Prostaglandine).
Aus Gründen der Übersichtlichkeit wird in dieser Arbeit vorrangig auf die Beatmungsbehandlung, deren mögliche Komplikationen und im Schwerpunkt auf den Einsatz des Interventional Lung Assist abgehoben, ohne die Wertigkeit der anderen Säulen abstufen zu wollen.
Grundzüge der Beatmungsbehandlung
Patienten im akuten Lungenversagen werden regelhaft beatmungspflichtig. Im Falle einer invasiven Beatmung wird ein künstlicher Atemweg, initial über
einen Orotrachealtubus, im weiteren Behandlungsverlauf auch oft über eine Trachealkanüle, z. B. nach Percutaner Dilatationstracheotomie, geschaffen.Nach den Empfehlungen des ARDS-Network orientiert sich die Höhe des applizierten PEEP an der erforderlichen inspiratorischen Sauerstoffkonzentration. International anerkannt ist das Ziel-Tidalvolumen für die Patienten mit 6 ml/kgKG [4]. Bezugsgröße ist hierbei das Ideale Körpergewicht, welches unter Umständen gravierend vom realen Körpergewicht abweichen kann [5].
Neuere Untersuchungen legen nahe, dass die o. g. Empfehlung jedoch nur einen initialen Anhalt für die Beatmungseinstellung darstellt. Eine individualisierte Festlegung des „Best-PEEP“ ist im intensivmedizinischen Kontext unerlässlich [1].
Im Zuge der Beatmungsbehandlung wird generell empfohlen, den Spitzendruck auf ≤ 30 cm H2O zu begrenzen.
Gerade vor dem Hintergrund der beatmungsassoziierten Lungenschäden (siehe unten) wird versucht, eine niedrige Druckamplitude bei der Respiratoreinstellung zu wählen (ΔP).
Unter diesen Beatmungseinstellungen treten häufig respiratorische Azidosen auf, die metabolisch nicht umgehend kompensiert werden. Bis zu welchem pH-Wert diese respiratorische Azidose toleriert werden kann, ist nicht abschließend geklärt. Derzeit gilt ein pH ≥ 7,2 als Zielgröße. Man spricht in diesem Zusammenhang auch vom Konzept der permissiven Hyperkapnie. Ein wichtiges ergänzendes Monitoringverfahren stellt nach Ansicht des Verfassers die bettseitige Echokardiographie dar, um frühzeitig Auswirkungen der azidosebedingten Widerstandserhöhung im kleinen Kreislauf auf den rechten Ventrikel zu detektieren.
Beatmungsassoziierte Lungenschäden
Zu den bekannten Komplikationen der invasiven Beatmungstherapie zählen im Wesentlichen Barotrauma, Volutrauma, Atelekttrauma sowie das
Biotrauma.Beim Barotrauma führt der hohe transpulmonale Druck (Alveolardruck minus Pleuradruck) zu Druckschäden an der Lunge und am interstitiellen Gewebe mit den möglichen Folgen z.B. eines Pneumothorax oder Pneumomediastinums.
Starke endexpiratorische Lungendehnung bedingt Alveolarschädigung, Erhöhung der epithelialen und endothelialen Permeabilität und verstärkte Flüssigkeitsfiltration mit der Folge eines Lungenödems. Dies wird unter Volutrauma zusammengefasst.
Beim Atelekttrauma resultieren die Schädigungen aus der raschen Aufeinanderfolge von Rekruitment und Derekruitment der unteren Atemwege. Die Öffnung erfordert relativ hohe Kräfte und entwickelt Scherstress mit der Folge der Epithelialzerreißung.
Infolge hoher Scherkräfte innerhalb der Alveole resultiert eine als Biotrauma benannte lokale Inflammationsreaktion im Grenzbereich zwischen belüfteten und kollabierten Alveolen.
Durch die Überdruckbeatmung kann der initiale Lungenschaden iatrogen aggraviert werden. Daher gelten die Konzepte der protektiven Beatmungsbehandlung auch im Hinblick auf die permissive Hyperkapnie zur Minimierung der Aggressivität und damit der negativen Folgen der Überdruckbeatmung.
Je kränker die Lunge, umso niedriger das applizierte Tidalvolumen!
Dies kann als Resultante des o. g. formuliert werden. Persistierende Hypoxämie/Hyperkapnie trotz Optimierung der Respiratoreinstellung können den Patienten gefährden. Ein möglicher Lösungsansatz könnte hier der frühzeitige Einsatz extrakorporaler Unterstützungssysteme darstellen. In einer Studie wurden diese Effekte untersucht [6]. Hier zeigte sich, dass in der Patientengruppe mit schwerem Lungenversagen die Kombination aus extrakorporaler Lungenunterstützung und ultraprotektiver Beatmung (Tidalvolumen 3 - 4 ml/kgKG) zu einem höheren Anteil an beatmungsfreien Tagen geführt hat.
Extrakorporale Lungenunterstützung im Bundeswehrkrankenhaus Berlin
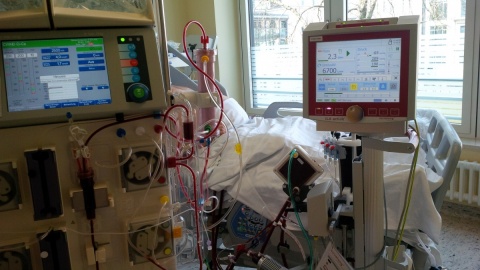
Auf der Intensivstation des Bundeswehrkrankenhauses Berlin wird seit 2008 regelmäßig das Lungenunterstützungssystem Interventional Lung Assist (iLA) des Herstellers Novalung® eingesetzt. Initial ausschließlich als sogenannte PECLA (pumpenlose extrakorporale Lungenunterstützung). Hierbei werden die Femoralarterie und -vene mit je einer speziellen Kanüle versorgt und der systemische arterielle Blutdruck ist entscheidend für den resultierenden Blutfluss über der Membran. Erreichbar sind hier Blutflüsse zwischen 0,8 und 1,5 l/min.
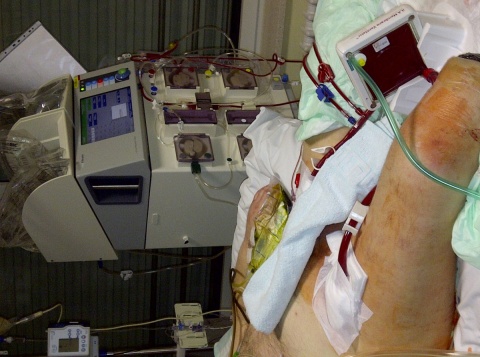
Seit 2015 setzen wir im Schwerpunkt die Weiterentwicklung des Membranventilators als pumpengetriebene Version iLA activve® ein. In Abhängigkeit von den verwendeten Kanülen sind hier wesentlich höhere Blutflüsse generierbar. Es werden ausschließlich große Venen punktiert und der Blutfluss wird über eine spezielle Pumpe hergestellt. Grundbestandteil bei beiden Systemen ist die Membran. Diese kann bei der iLA activve®-Konsole noch in der Größe variiert werden. Je höher der erreichbare Blutfluss, umso besser ist die Oxygenierungsunterstützung für die behandelten Patienten. Wie in den Abbildungen 1 und 2 zu sehen, können sowohl das pumpenlose- als auch das pumpengetriebene System mit einer Nierenersatztherapie kombiniert werden, ohne dass weitere Gefäße kanüliert werden müssen.
Funktionsbeschreibung des Membranventilators (Herstellerangaben)
Der iLA Membranventilator™ ist ein Lungenunterstützungssystem, welches den Austausch von Kohlendioxid und Sauerstoff durch Diffusion über eine
dichte Membran aus Polymethylpenten (PMP) ermöglicht. Alle Blutkontaktflächen des iLA Membranventilators™ sind mit dem Novalung® Coating versehen. Diese Beschichtung ist eine bioaktive, stabile, biokompatible und nicht thrombogene Oberfläche. Bestandteile dieser Beschichtung sind hochmolekulares Heparin aus Schweinemukosa welches kovalent und ionisch an immobilisiertes Polypeptid gebunden ist. Abhängig von Material und Oberflächeneigenschaften des Materials liegt die Heparinmenge des beschichteten Materials bei bis zu 0,3 μg/cm². Beim Gebrauch von beschichteten Systemen in extrakorporalen Kreisläufen wurde ein Auswaschen von Heparin bis zu 20 % beobachtet. Der iLA Membranventilator™ besitzt eine Gasaustauschmembran, deren Anordnung einen extrem niedrigen Widerstand auf der Blutseite erlaubt. Die Membran besteht aus Hohlfasern die zu Matten verwirkt sind. Die Matten sind jeweils im 90° Winkel angeordnet um bestmögliche Blut-Membrankontakte zu erreichen. Blut umströmt die Fasern während Gas durch die Hohlfasern geleitet wird. Gasaustausch durch die Hohlfaserwände findet auf Grund der Permeabilität für Gase statt. Treibende Kräfte sind die Partialdruckdifferenzen von Kohlendioxid und Sauerstoff im Blut und in der Gasphase. Die dichten Fasern ermöglichen eine sehr lange Betriebszeit ohne Plasmaübertritt aus dem Blut in die Gasphase.Typische Behandlungsindikationen für den Einsatz des Membranventilators
Zu den häufigsten Behandlungsindikationen für den Einsatz des Membranventilators auf der Intensivstation des Bundeswehrkrankenhauses Berlin zählen das hyperkapnische Lungenversagen und die Frühphase des hypoxämischen Lungenversagens unterschiedlicher Genese (Tabelle 1). Sehr gute Behandlungsergebnisse haben wir ebenfalls bei der Behandlung großer bronchopleuraler Fisteln, z. B. nach thoraxchirurgischen Eingriffen durch den unterstützenden Einsatz des Membranventilators erzielt.
Organisatorische Maßnahmen in Bezug auf den Einsatz des Membranventilators
Die Therapie mit dem Membranventilator ist durch eine entsprechende SOP (Standard Operating Procedure) für die Intensivstation abgebildet. Mehrere Ärztliche Kollegen haben Schulungen an der Nova Lung Academy besucht. Für das gesamte Team fanden und finden mehrere Einweisungsveranstaltungen statt. Durch die Firma Nova Lung erfolgte ein iLA-Klinik-Workshop für die Mitarbeiter der Intensivstation. Weiterhin ist der sehr gute Klinische Support der Firma (24/7) hervorzuheben. Auf der Internetplattform www.xenios-campus.com sind weiterführende Informationen abrufbar.
Wehrmedizinische Relevanz
Im Rahmen des erweiterten Aufgabenspektrums der Bundeswehr sind bei bewaffneten Auseinandersetzungen und/oder nach terroristischen Aggressionen auch Verwundete mit Lungenerkrankungen (Blast Lung Injury) durch den Sanitätsdienst der Bundeswehr zu versorgen. Aber auch der Zuwachs an Terrorakten in Zentraleuropa erhöhen die Wahrscheinlichkeit, dass in den Bundeswehrkrankenhäusern auch vermehrt Patienten mit stattgehabten Explosionstraumata zu versorgen sein werden.
Das Krankheitsbild „Blast Lung Injury“
Die Blast Lung gehört zu den primären Folgen des Explosionstraumas. Für die Überlebenden ist die pathophysiologische Veränderung in der Lunge, die durch die Druckwelle der Explosion ausgelöst wird, entscheidend. Es handelt sich um ein komplexes Lungentrauma, dass sich unmittelbar als Lungenversagen im Sinne eines ARDS[2] manifestiert. Dieses explosionstrauma-induziertes ARDS ist die häufigste Ursache für das sekundäre Versterben der Betroffenen [7,8].
Konsequenzen für die Behandlung der Verwundeten in den Sanitätseinrichtungen
Die Versorgung der Verwundeten verläuft in den Sanitätseinrichtungen der Bundeswehr standardisiert u. a. nach den Prinzipien von ATLS[3] und DCS[4]. Diese Prinzipien sind nicht Gegenstand dieser Arbeit. Für die weitere intensivmedizinische Stabilisierung mit dem Ziel der Herstellung der Verlegefähigkeit ist die Therapie des ARDS nach den aktuellen Standards mitentscheidend für das Outcome. Behandlungsrelevant ist das vermehrte Auftreten von Kombinationsverletzungen, die neben der Lunge auch häufig Kopfverletzungen beinhalten. Das Konzept der permissiven Hyperkapnie für die Beatmungsbehandlung beim Lungenversagen kann fatale Auswirkungen auf den intrakraniellen Druck bei Schädel-Hirn-Traumatisierten haben. Auch die Reduktion der beatmungsassoziierten Lungenschäden bei den Patienten mit Blast Lung stehen im Focus der Behandler. Eine flächendeckende Bevorratung mit extrakorporalen Assist-Systemen in den Einsatzgebieten ist jedoch aus nachvollziehbaren Gründen nicht praktikabel.
(Potentielle) Konsequenzen für STRATAIRMEDEVAC-Operationen
Im zivilen Bereich hat es sich bewährt, dass Patienten mit akutem Lungenversagen, die in ein ARDS-Zentrum verlegt werden sollen, noch im entsendenden Krankenhaus durch Spezialisten der ARDS-Zentren an eine mobile Lungenunterstützungseinheit angeschlossen werden. Dieses Vorgehen erhöht die Patientensicherheit während der Transporte und verkürzt die Zeit bis zum Beginn dieser effektiven Therapie.
Möglicherweise lässt sich dieses Vorgehen auch auf medizinische Verlegungen aus den Einsatzgebieten nach Deutschland für den Sanitätsdienst der Bundeswehr übertragen. Der Vorteil, gerade der PECLA besteht hierbei in dem sehr kompakten Aufbau und der einfachen Steuerung. Spezialisierte Teams aus den Bundeswehrkrankenhäusern könnten so bei STRATAIRMEDEVAC[5] das notwendige Equipment mitführen und im
Einsatzland den Anschluss des Verwundeten an das Lungenunterstützungssystem vornehmen. Die eigentliche Implantation ist wenig zeitaufwendig und der therapeutische Effekt mit Hilfe von arteriellen Blutgasanalysen gut zu überwachen. Somit wäre bereits während der mitunter mehrstündigen Verlegungen eine (ultra-)protektive Beatmung möglich. Umbauten in den Luftfahrzeugen, z. B. für Transportsicherungssysteme, sind beim Einsatz der PECLA nicht erforderlich. Der Membranventilator kann zwischen den Oberschenkeln fixiert werden. Die Sauerstoffzufuhr ist problemlos an der Patiententransporteinheit generierbar. Für Verwundete amerikanische Soldaten ist dieses Konzept bereits erfolgreich umgesetzt worden [9]. Die Behandlungsqualität kann somit weiter erhöht werden [10].
Zusammenfassung
Das akute Lungenversagen bedarf einer intensivmedizinischen Behandlung. Diese umfasst auch den frühzeitigen indikationsbezogenen Einsatz von extrakorporalen Lungenunterstützungsverfahren. Für den Sanitätsdienst der Bundeswehr steht mit dem iLA-Membranventilator eine vielversprechende Lösung, auch für den weltweiten mobilen Einsatz bei STRATAIRMEDEVAC-Operationen zur Verfügung.
Literatur beim Verfasser.
[1] PEEP Positiv endexpiratorischer Druck
[2] ARDS Acute Respiratory Distress Syndrome
[3] ATLS Advanced Trauma Life Support
[4] DCS Damage Control Surgery
[5] STRATAIRMEDEVAC Strategischer Luftverwundetentransport
Oberfeldarzt Dr. MED. Stefan Markoff
geb. am 13.05.1972 in Berlin
Anschrift des Verfassers:
Oberfeldarzt Dr. Stefan Markoff
Bundeswehrkrankenhaus Berlin
Abteilung X-Anästhesie, Intensivmedizin,
Notfallmedizin und Rettungsdienst
Scharnhorststr. 13
10115 Berlin
E-Mail: stefanmarkoff@bundeswehr.org
Dienstlicher Werdegang...
- 1992: Einberufung zum Grundwehrdienst
- 1993: Übernahme in das Dienstverhältnis eines SaZ
- 2005: Übernahme als Berufssoldat
- Studium der Humanmedizin und Promotion an der Humboldt-Universität zu Berlin
- Facharztausbildung und Zusatzweiterbildung am Bundeswehrkrankenhaus Berlin,
- Abteilung X
Derzeitige Verwendung...
- Interdisziplinäre Intensivstation am Bundeswehrkrankenhaus Berlin, Oberarzt
Auslandseinsätze...
- 2002: SFOR
- 2004: ISAF KDZ und FEY
- 2005: HumHiSOA Banda Aceh
- 2006: ISAF FEY
- 2007: ISAF KBL
- 2009: ISAF FEY
- 2009: ATALANTA
Datum: 29.08.2016
Quelle: Wehrmedizin und Wehrpharmazie 2016/2