EIN NASENSPRAY GEGEN PATHOLOGISCHE ANGSTZUSTÄNDE?
Die Furcht, die auch als Realangst bezeichnet wird, ist eine lebenswichtige Emotion, die es uns ermöglicht, bedrohliche Situationen zu erkennen und adäquat zu bewältigen. Treten jedoch über einen längeren Zeitraum quälende, diffuse Angstgefühle unabhängig von der Präsenz bedrohlicher Stimuli auf, leiden die davon Betroffenen unter pathologischer Angst.
Pathologische Angstzustände sind ein Symptom unterschiedlicher psychischer Erkrankungen, wie beispielsweise der Panikstörung oder der Posttraumatischen Belastungsstörung (PTBS). Wie die sogenannte Dunkelzifferstudie, eine gemeinsame wissenschaftliche Untersuchung des Sanitätsdienstes der Bundeswehr und der Technischen Universität Dresden, ergeben hat, entwickelten rund 2% aller Bundeswehrsoldaten, die im Jahre 2009 an einem Einsatz in Afghanistan teilgenommen hatten, das Vollbild einer PTBS [1]. Hinzu kommen noch diejenigen Soldaten, die nur einen Teil der PTBS-Diagnosekriterien erfüllen, aber dennoch aufgrund eines anhaltenden Leidensdrucks einer Therapie bedürfen. Davon abgesehen gibt es neben der PTBS, deren Hauptsymptome Nachhall- Erinnerungen (Flashbacks, Intrusionen) sowie eine nervöse Übererregbarkeit und eine ausgeprägte Vermeidungsangst sind, noch andere einsatzbezogene psychische Störungen, die mit Angstsymptomen einhergehen können.
Zur Behandlung krankhafter Angstzustände stehen neben störungsspezifischen Psychotherapieverfahren auch medikamentöse Therapieoptionen zur Verfügung. Für die Behandlung der Panikstörung und der PTBS gilt aktuell die Kombination von SSRI-Antidepressiva mit verhaltenstherapeutisch orientierten störungsspezifischen Psychotherapieverfahren als die Therapie der Wahl. Jedoch benötigen Antidepressiva bis zum Eintritt ihrer vollen Wirkung in der Regel einige Wochen und führen, insbesondere bei der PTBS, in vielen Fällen nicht zu einer Vollremission und in einigen Fällen nicht einmal zu einer Symptomreduktion [2]. Im Gegensatz zu Antidepressiva entfalten Benzodiazepine wie bspw. Valium zwar sehr rasch ihre effiziente angstlösende Wirkung, aber sind wegen ihres hohen Abhängigkeitspotentials nur zur Akuttherapie und nicht zur Langzeitbehandlung geeignet. Die Erforschung neuer rasch wirksamer Anxiolytika ist also dringend erforderlich.
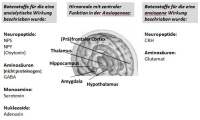
Die Entwicklung neuartiger angstlösender Medikamente erfordert zunächst die detaillierte Entschlüsselung der Molekularpathogenese der Angsterkrankungen, also das Verständnis der neurobiologischen Grundlagen der Entstehung krankhafter Angst. Es ist bereits seit längerem bekannt, u.a. aus fMRIStudien mit Hilfe derer man Aktivitäten einzelner Hirnregionen kernspintomographisch darstellen kann, dass Hirnregionen wie die Amygdala (Mandelkerne) und der Cinguläre Cortex eine wesentliche Rolle bei der Generierung von Furcht, Angst und damit auch von pathologischer Angst spielen [3]. Molekularanalysen ergaben, dass die Neurotransmitter Serotonin und Gamma-Aminohydroxybuttersäure (GABA) zentrale Funktionen bei der Entstehung pathologischer Ängste haben. Die bereits erwähnten, zur Langzeittherapie von bspw. Panikstörungen eingesetzten, SSRI-Antidepressiva erhöhen den Botenstoff Serotonin im synaptischen Spalt und die rasch anxiolytisch wirkenden Benzodiazepine docken an den neuronalen GABA-Rezeptoren an und wirken dort agonistisch. Neben diesen Neurotransmittern wurden noch andere angstlösende körpereigene neuronale Botenstoffe entdeckt - die sogenannten Neuropeptide. Neuropeptide entstehen, vom Prinzip her vergleichbar mit der Biosynthese von Insulin, durch enzymatische Abspaltung verschiedener Peptid-Vorstufen; sie werden im Hirngewebe sehr rasch abgebaut und haben daher kurze Halbwertszeiten. Für die Neuropeptide NPY und Oxytocin wurden angstlösende Wirkungen beschrieben [4]. NPY dockt an zahlreiche Rezeptoren an, was für die Entwicklung neuartiger Medikamente grundsätzlich eine ungünstige Voraussetzung darstellt und übt noch weitere Wirkungen aus, wie bspw. die der Förderung der Gewichtszunahme. Das Neuropeptid Oxytocin hat demgegenüber zwar den Vorteil, nur an einen einzigen Rezeptor zu binden, sein angstlösendes Potential ist jedoch beschränkt, da es vorwiegend Abbau sozialer Ängste fördert. Den aktuell interessantesten Kandidaten zur Entwicklung eines Neuropeptid-basierten Anxiolytikums stellt das Neuropeptide S (NPS) dar. Rainer Reinscheid und Kollegen von der Universität of California in Irvine entdeckten die beeindruckende angstlösende Wirkung von NPS, das wie Oxytocin günstigerweise nur an einen einzigen Rezeptor andockt, in Mäusen, denen die Wissenschaftler die Substanz in die Hirnventrikel bzw. direkt ins Hirngewebe spritzten [5]. Da diese Applikationsmethode für die wiederholte Anwendung beim Menschen selbstverständlich ungeeignet ist, suchte die Referentin nach Alternativen: Die intravenöse Applikation ist für die tägliche Anwendung zur Langzeitherapie sehr unpraktikabel und außerdem ist unklar, ob peripher injiziertes NPS in der Lage ist, die Blut-Hirn-Schranke zu überwinden. Die Verabreichung von Peptiden in Tablettenform erniedrigt deren Bioverfügbarkeit drastisch, da sie im Magen in kürzester Zeit durch Peptidasen abgebaut werden. Die erfolgreiche Anwendung eines anderen Neuropeptids (Vasopressin) als Nasenspray im Einsatz gegen den Diabetes insipidus, vor Augen, prüften wir daher die Eignung dieser einfach anzuwendenden nicht invasiven Applikationsmethode für NPS. Ob eine Substanz nach intranasaler Verabreichung in wirksamen Mengen das Gehirn erreicht, kann durch Analyse seiner Molekularstruktur zwar abgeschätzt, aber nicht sicher vorhergesagt werden. Unsere Hypothese bestätigte sich: Wir konnten u. a. an einem Mausmodell für Angsterkrankungen zeigen, dass die äußerst ängstlichen HAB (high anxiety behavior)-Mäuse, die nicht einmal auf Benzodiazepine reagieren, in bestimmten, international anerkannten Verhaltenstests, vier Stunden nach intranasaler Gabe von NPS deutlich weniger Angst zeigten [6]. Diese Ergebnisse in Mäusen stellen einen wichtigen Schritt in Richtung der Entwicklung NPS-basierter Anxiolytika zur Therapie von Angsterkrankungen des Menschen und eine wichtige Voraussetzung für die Durchführung entsprechender klinischer Studien dar. Die Nasen/Hirn-Schranke der Säugetiere und des Menschen ist sehr ähnlich aufgebaut. Man geht davon aus, dass Substanzen, die über die Nasenschleimhaut das Hirngewebe erreichen die Lamina cribrosa passieren und die Nervenscheiden des Nervus olfactorius und des Nervus trigeminus als Transportschienen benutzen, um sich auf diesem Wege rasch im Hirngewebe zu verteilen. Unsere Analysen ergaben, dass sich intranasal appliziertes NPS innerhalb von 30 Minuten im murinen Gehirn verteilt. Vier Stunden nach der Applikation konnten wir eine Reduktion des Angstverhaltens der Tiere beobachten.
Neben der Entwicklung einer neuen, auch am Menschen anwendbaren, Applikationsform für NPS haben unsere Experimente noch eine Reihe anderer neuer Erkenntnisse über die Wirkungsweise dieses kleinen angstlösenden Neuropeptids erbracht: Unter Zuhilfenahme von Fluoreszenzfarbstoff-gekoppeltem NPS konnten wir u.a. zeigen, dass intranasal verabreichtes NPS auch in Neuronen der Hirnregion Hippocampus aufgenommen werden kann, was die Bedeutung dieses Hirnareals in der zentralnervösen Regulationskaskade von Furcht und Angst hervorhebt. Zudem fanden wir heraus, dass NPS die Konzentration von Proteinen, die am zellulären Glutamatstoffwechsel beteiligt sind, verändert [6]. Es kann spekuliert werden, dass diese Stoffwechseleffekte dem anregenden und die Motorik stimulierenden Effekt von NPS zu Grunde liegen. Im Gegensatz zu NPS wirken Benzodiazpine eher sedierend.
Auf diesen Erkenntnissen werden weitere Untersuchungen aufbauen, die zum Ziel haben, die molekularen Wirkmechanismus von NPS exakt zu entschlüsseln. Klinische Studien werden Hinweise auf die Anwendbarkeit und am Menschen bringen und später auch klären, ob dieses körpereigenen Peptide sich zur Behandlung von einsatzbezogener psychischer Angst-Erkrankungen wie bspw. der PTBS und der Panikstörung, eignen.
Zusammenfassend haben wir an Mäusen eine Applikationsform des angstlösenden NPS entwickelt, die auch für die Anwendung am Menschen geeignet ist. Klinische Studien müssen nun zeigen, ob sich NPS-Nasenspray zur Behandlung von Angstsymptomen, die nicht nur bei der PTBS, sondern bei einer Reihe von einsatzbezogenen psychischen Erkrankungen auftreten, eignet.
Datum: 19.09.2012
Quelle: Wehrmedizin und Wehrpharmazie 2012/2