ZUR BEDEUTUNG DES ZECKEN-ÜBERTRAGENEN PATHOGENE ANAPLASMA PHAGOCYTOPHILUM UND CANDIDATUS NEOEHRLICHIA MIKURENSIS IN DEUTSCHLAND
Relevance of the tick-borne pathogens Anaplasma phagocytophilum and Candidatus Neoehrlichia mikurensis in Germany
Aus dem Lehrstuhl für Vergleichende Tropenmedizin und Parasitologie¹ (Kommissarischer Leiter: Prof. Dr. G. Sutter) der Ludwig-Maximilians-Universität München und dem Institut für Tierhygiene und Öffentliches Veterinärwesen² (Direktor: Prof. Dr. U. Truyen) der Universität Leipzig
Cornelia Silaghi¹ und Martin Pfeffer²
WMM, Jahrgang 58 (Ausgabe 4/2014; S. 123-128)
Zusammenfassung
Hintergrund: In Deutschland sind von den durch Zecken übertragenen Pathogenen vor allem das Virus der Frühsommer-Meningoenzephalitis (FSME) und die Spirochäten aus der Gruppe der Borrelien bekannt. Aber es gibt noch weitere Zoonoseerreger, die durch den gemeinen Holzbock Ixodes ricinus auf Mensch und Tier übertragen werden. Erstere sind aber bei den Ärzten wenig bekannt und so wird ihre Diagnostik entsprechend selten angefordert.
Methoden: Literaturrecherche in Pubmed unter Nutzung der unten angeführten Schlagworte und eigene Untersuchungen an Zecken und Nagetieren in Deutschland.
Ergebnisse: Es wird der aktuelle Kenntnisstand zur medizinischen Bedeutung von Anaplasma phagocytophilum und Candidatus Neoehrlichia mikurensis vorgestellt, über die in der ärztlichen Praxis noch wenig bekannt ist.
Schlussfolgerungen: Speziell bei beruflich und einsatzbedingter starker Zeckenexposition sollten auch seltenere Krankheitsbilder bekannt sein, um im Sinne des Arbeitsschutzes Aufklärung und präventive Maßnahmen ergreifen zu können.
Schlagworte: Ixodes ricinus, Anaplasma phagocytophilum, Candidatus Neoehrlichia mikurensis, Zecken, Arbeitsschutz
Summary
Background: Tick-borne encephalitis virus and the group of Borrelia spirochetes are the best known tick-borne pathogens In Germany. But there are other, less prominent zoonotic pathogens that are transmitted to man and animals by the sheep tick, Ixodes ricinus. Those are not well known among physician and consequently their diagnostic is not asked for.
Methods: Review of the relevant literature using keywords below as well as own studies in ticks and rodents from Germany.
Results: This review provides a comprehensive up-to-date knowledge of two of these, namely Anaplasma phagocytophilum and Candidatus Neoehrlichia mikurensis aiming at an enhanced awareness.
Conclusions: In situations with professional outdoor exposure to ticks the knowledge about rare tick-borne diseases should be present in terms of education, potential preventive measures and thus work safety.
Keywords: Ixodes ricinus, Anaplasma phagocytophilum, Candidatus Neoehrlichia mikurensis, ticks, work safety.
Einleitung
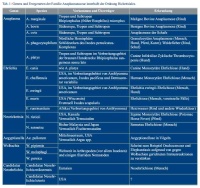
Zecken spielen in zunehmendem Maße eine entscheidende Rolle als Überträger von Pathogenen und sind somit von wachsender Relevanz für das öffentliche Gesundheitswesen. Besonders Menschen, die sich beruflich oder in ihrer Freizeit viel in der freien Natur aufhalten, sind gefährdet. Zu den von Zecken übertragenen Pathogenen gehören Viren, wie zum Beispiel das Virus der Frühsommer-Meningoenzephalitis (FSME), Bakterien wie Borrelia burgdorferi sensu lato und Protozoen (zum Beispiel Babesien), aber auch bestimmte Helminthenarten [1]. Von zunehmender Bedeutung sind in Mitteleuropa die intrazellulären und von Zecken übertragenen alpha-Proteobakterien aus der Ordnung Rickettsiales. 2001 schlugen Dumler und Kollegen [2] eine Reorganisation der Ordnung Rickettsiales auf Basis von Homologien im 16S rRNA Gen vor, die nun aus den Familien Rickettsiaceae und Anaplasmataceae besteht. Alle Stämme wurden aus der Ordnung entfernt. Die Familie Anaplasmataceae besteht derzeit aus den Genera Wolbachia, Ehrlichia, Neorickettsia, Aegyptianella and Anaplasma [2]. Mit Neoehrlichia wird wohl in naher Zukunft ein weiteres Genus in die Familie aufgenommen. Zu dieser Familie gehören viele human- und veterinärmedizinisch relevante intrazelluläre Krankheitserreger, die durch verschiedene blutsaugende Gliederfüßler (Vektoren) übertragen werden (Tab. 1). Medizinisch bedeutsam sind in Deutschland die neu aufkommenden und durch die Schildzecke Ixodes ricinus übertragenen Bakterien Anaplasma (A.) phagocytophilum und Candidatus Neoehrlichia mikurensis.
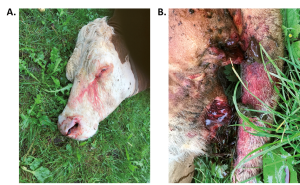
A. phagocytophilum wurde in der ersten Hälfte des 20. Jahrhunderts als Erreger des Weidefiebers bei Schafen in Schottland entdeckt und zunächst als Rickettsia phagocytophila klassifiziert. Aufgrund morphologischer Ähnlichkeiten wurde es wenig später in das Genus Cytocetes im Stamm Ehrlichia als Cytocetes phagocytophila aufgenommen und im weiteren Verlauf in Ehrlichia (E.) phagocytophila umbenannt [3]. Das spätere Genus Ehrlichia wurde in drei Genogruppen aufgeteilt. Die granulozytäre Gruppe enthielt E. phagocytophilum, E. equi und den Verursacher der Humanen Granulozytären Ehrlichiose (HGE). Nach der Reklassifikation des Genus Ehrlichia auf der Basis phylogenetischer Studien wurde die gesamte granulozytäre Ehrlichia-Gruppe zusammengefasst und in Anaplasma phagocytophilum umbenannt [2]. A. phagocytophilum gilt heute als das verursachende Agens der Humanen, Caninen, Equinen und Felinen Granulozytären Anaplasmose. Bei Wiederkäuern wird die Erkrankung traditionell weiter als Weidefieber bezeichnet [3].
Zwei Forschergruppen fanden Ende der 1990er Jahre in Ixodes-Zecken DNA-Sequenzen, die mit einer generischen DNA-Sonde für Ehrlichien hybridisierten, aber mit keiner der verwendeten Spezies-spezifischen DNA-Sonden für die damals bekannten Ehrlichia-Arten reagierten. Die erste publizierte Studie fand diese taxonomisch nicht gruppierbare Ehrlichien-DNA in gesaugten Ixodes (I.) ricinus von in Holland erlegten Rehen [4], die entsprechenden Erreger wurde nach dem Seniorautor als „Schotti-Variante“ bezeichnet [4]. 2001 wurden ähnliche Ergebnisse von im Baltikum gefangenen I. ricinus und I. persulcatus publiziert [5]. Zwischen 1998 und 2001 fand sich in I. ricinus-Zecken vom Körper asymptomatischer italienischer Patienten die DNA eines Erregers, für den der Name Candidatus Ehrlichia walkeri sp. nov. vorgeschlagen wurde [6]. Entsprechende DNA-Sequenzen wurden in I. ricinus 2003 auch in Deutschland erstmals beschrieben [7]. Es folgten erste Untersuchungen zu möglichen Reservoirwirten. Im Jahr 2003 wurde in drei Wanderratten (Rattus norwegicus) in Südchina mittels PCR und anschließender Sequenzierung ein Erreger nachgewiesen, der als „Rattus Variante“ bezeichnet wurde [8]. Ein Jahr später beschrieb eine japanische Arbeitsgruppe umfassend den Nachweis der DNA des „neuen“ Erregers in 7 von 15 auf der japanischen Insel Mikura gefangenen Wanderratten [9]. Der Erreger wurde in Laborratten passagiert, sodass erste Untersuchungen zur Ultrastruktur sowie weitergehende phylogenetische Analsyen möglich wurden. Diese, führten zu der derzeit gültigen taxonomischen Stellung und Bezeichnung Candidatus Neoehrlichia mikurensis (CNM). Die genetische Verwandschaft der 16S rRNA und groEL-Gene platziert CNM in die Familie Anaplasmataceae. Da es bisher nicht gelungen ist, CNM in vitro zu propagieren bleibt der Status „Candidatus“ nach wie vor erhalten.
Bekannte Eigenschaften der Erreger
A. phagocytophilum ist ein kleines (0,5 - 1,5 µm), gramnegatives obligat intrazelluläres alpha-Proteobakterium [2]. Es infiziert die neutrophilen Granulozyten von Säugetieren und zu einem geringeren Anteil auch die eosinophilen Granulozyten und Monozyten, wo es in zytoplasmatischen, aus der Zellmembran bestehenden, Vakuolen gefunden wird. Allerdings scheinen die neutrophilen Granulozyten nicht an der frühen Phase der Erkrankung beteiligt zu sein. A. phagocytophilum wird in den ersten 24 Stunden des Zeckenbisses übertragen. Zu dieser Zeit des Saugaktes der Zecke sind die Blutgefäßwände noch intakt und so können die Neutrophilen nicht ins Blutsystem zurück und damit zur Verbreitung des Bakteriums in Organismus beitragen. Möglicherweise ist hier das mikrovaskuläre Endothel involviert [10].
Aufgrund seiner intrazellulären Lebensweise lässt sich A. phagocytophilum nur in Zellkulturen anzüchten, wie zum Beispiel in der humanen promyelotischen Zelllinie HL-60 und in Zeckenzelllinien, zum Beispiel IDE8 [3].
Bei CNM handelt es sich ebenfalls um ein obligat intrazelluläres, gram-negatives Bakterium, das endothelialen Zelltropismus zeigt. Da sich CNM bisher nicht in gängigen Zellkultursystemen oder mit anderen Methoden außerhalb von Wirtstieren vermehren lässt, ist darüber hinaus noch nicht viel über dessen Eigenschaften bekannt. Zumindest zu drei (Anaplasma, Ehrlichia, Neorickettsia) der fünf Genera innerhalb der Familie Anaplasmataceae existieren keine serologischen Kreuzreaktionen [9].
Vektoren und Wirte
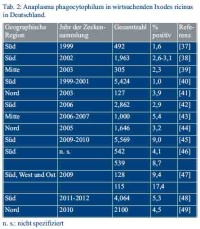
A. phagocytophilum wird von Schildzecken des I. persulcatus-Komplexes übertragen. Der Hauptvektor in Europa ist I. ricinus (Holzbock); in den östlichen USA I. scapularis (Hirsch- oder Rehzecke); in den westlichen USA I. pacificus (Western black-legged tick), und in Asien I. persulcatus (Taigazecke) [3]. A. phagocytphilum wird in stark schwankenden Prävalenzraten in Zecken in Europa, USA und in Asien gefunden. In den USA reichen die Prävalenzen in I. scapularis von 0,2 % bis zu 50 % in einzelnen Untersuchungen, in I. pacificus von 0,8 % - 9,9 % und ein DNA-Nachweis wurde zum Beispiel auch in Amblyomma americanum, und Dermacentor (D.) variabilis und D. occidentalis erbracht [3]. In Europa wurde A. phagocytophilum in wirtssuchenden Zecken (hauptsächlich I. ricinus, aber auch I. persulcatus etc.) in über 25 Ländern gefunden, beispielsweise mit Befallsraten von 0,4 - 17,1 % in Norwegen, 3 - 6,5 % in Estland, 2,5 - 19,2 % in Polen, 1,1 - 8,3 % in der Slowakei, 0,4 - 15 % in Frankreich, und 3,7 - 20,5 % in Spanien [3]. Eine detaillierte Übersicht über die Nachweisraten in I. ricinus in Deutschland gibt Tabelle 2. In Asien wurde A. phagocytophilum bisher in wirtssuchenden I. persulcatus, I. ovatus, I. nipponenis, D. silvarum, Haemaphysalis (H.) megaspinosa, H. longicornis und H. douglasii nachgewiesen, dabei schwanken die Prävalenzen beispielsweise von 0,8 % - 21,6 % in I. persulcatus [3].
Eine transovarielle Übertragung wurde bisher nicht in Ixodes-Zecken nachgewiesen. Somit ist zum jetzigen Wissensstandpunkt ein Wirbeltierwirt nötig, um den Lebenszyklus von A. phagocytophilum in der Natur aufrecht zu erhalten. In Europa, Asien und Amerika wurde A. phagocytophilum in mehreren Wildwiederkäuerspezies gefunden. Die Prävalenzraten im Weißwedelhirsch in den USA betragen von 3,1 - 46,6 %, im Reh in Europa von 9,6 - 98,9 %. A. phagocytophilum wurde unter anderem auch in Rotwild, Damwild, Sikawild sowie in Gämsen und Steinböcken nachgewiesen. Auch hier schwankten die Prävalenzen sehr stark zwischen 1,5 - 87,5 % [3]. In Europa gehört das Reh zu den Hauptwirten von adulten Zecken und kann zu einem schnellen Anstieg von Zeckenpopulationen beitragen [11].
Die zweite große Gruppe, in denen A. phagocytophilum in endemischen Ländern gefunden wird, sind Kleinsäuger wie Nagetiere und Insektenfresser. Diese Tiere stellen ebenfalls wichtige Wirte besonders für die Entwicklungsstadien von Zecken dar [12]. So wurden in Europa A. phagocytophilum Befallsraten von <1 - 15 % in Gelbhalsmäusen (Apodemus flavicollis), von <1 - 11 % in Waldmäusen (Apodemus sylvaticus) und von 5 - 19,2 % in Rötelmäusen (Myodes glareolus) gefunden. In England wird außerdem die Feldmaus (Microtus arvalis) als Reservoir diskutiert [13]. Jedoch gibt es auch viele Studien in Europa, in denen keine DNA von A. phagocytophilum in Nagetieren nachgewiesen werden konnte, und die Reservoirstellung dieser Tiergruppe weiterhin nicht vollständig geklärt ist [3]. Die Weißfußmaus in den östlichen und in der Mitte der USA gilt als einer der Hauptwirte für die humanpathogene Variante (siehe unten) von A. phagocytophilum. Der Erreger wurde auch in weiteren Kleinsäugern in den USA gefunden wie in verschiedenen Maus- und Wühlmausspezies sowie in Hörnchenarten wie Backenhörnchen oder Grauhörnchen. In der Buschratte (Neotoma fuscipes), die im Westen der USA vorkommt, wurden Prävalenzen von 1.8 % - 88,4 % festgestellt. In Asien wird die Brandmaus (Apodemus agrarius) als einer der Hauptwirte für A. phagocytophilum aufgrund von Befallsraten bis zu 23,6 % diskutiert. Obwohl verschiedene Insektenfresser wie beispielsweise Spitzmausarten zum Teil hohe Prävalenzen bis zu 63,3 % aufwiesen und die durchschnittlichen Prävalenzen in Insektenfressern laut verschiedener Studien um die 20 % betrugen, ist deren Reservoirpotenzial nach wie vor nicht geklärt [3].
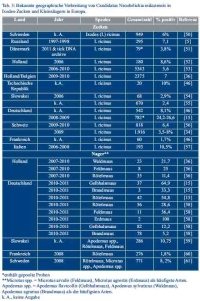
CNM wurde bislang ausschließlich in Zecken der Gattung Ixodes gefunden [14]. Dabei erstreckt sich das bisher bekannte Verbreitungsgebiet von Japan im äußersten Osten Asiens über den nördlichen Teil des asiatischen Kontinentes bis nach Italien und Frankreich in Europa. In Europa selbst wurde CNM nun in weiten Teilen von Süd nach Nord und Ost nach West nachgewiesen. Die Prävalenzen schwanken meist zwischen 1 und 11 %, allerdings gibt es fokal auch höhere Prävalenzraten mit über 25 % [15] (Tab. 3). Im Pool archivierter Zecken, die bereits 1969 in Moldavien geflaggt worden waren, ließ sich CNM-spezifische DNA in einer von 126 Ix. ricinus nachweisen, [16]. Untersuchungen potenzieller Reservoirwirte ergaben teils hohe Befallsraten in verschiedenen Nagetierspezies, ganz besonders in Gelbhalsmäusen und Rötelmäusen, bislang allerdings keinen Nachweis von CNM in Insektenfressern (Tab. 3). Aus Afrika, Australien und Südamerika sind keinerlei Nachweise von CNM bekannt. Aus Nordamerika wurde allerdings aus Waschbären ein naher Verwandter des CNM mit dem Namen Candidatus Neoehrlichia lotoris beschrieben [17].
Medizinische Bedeutung
Anaplasma phagocytophilum
Die Humane Granulozytäre Anaplasmose (HGA), ausgelöst durch A. phagocytophilum, zeigt sich häufig als unspezifische fieberhafte Erkrankung: Sie kann sich auch als asymptomatische Infektion oder tödlich verlaufende Krankheit entwickeln [18]. Die unspezifischen Symptome beinhalten nach der Inkubationszeit von 7 - 10 Tagen das akute Eintreten von Fieber, Kopfschmerzen, Unwohlsein und Myalgien. Weniger häufig sind Nausea, abdominale Schmerzen, Diarrhoe und Husten. Hämatologische Befunde wie Leukopenie, Lymphopenie und Thrombozytopenie werden ebenfalls häufig beobachtet sowie Anämie mit etwas geringerer Häufigkeit. Des Weiteren treten milde bis moderate Leberschäden auf, die zu einer erhöhten Aspartat- und Alanin-Aminotransferaseaktivität im Serum führen [19, 20]. Die meisten Symptome klingen nach circa 30 Tagen selbst ohne Behandlung ab. Allerdings können aufgrund der Leukopenie und Lymphopenie opportunistische Erreger wie zum Beispiel Candida albicans sekundäre Infektionen auslösen. Obwohl insgesamt die Letalität bei unter 1 % liegt, können verschiedene Komplikationen wie ein septischer oder toxischer Schock auftreten, ebenso Atembeschwerden, Rhabdomyolysis, Pancarditis, akutes Nierenversagen und Hämorrhagien, die sowohl Tage nach der Erkrankung aber auch viel später auftreten können [18].
Die HGA wurde erstmals 1990 in den USA beobachtet und seitdem auch in Europa und Asien beschrieben. In den USA ist die HGA eine der wichtigsten durch Zecken übertragenen Infektionen. Die höchsten Fallzahlen werden im Nordosten und im Mittleren Westen beschrieben [19]. Die Anzahl der dem Center for Disease Control (CDC) in Atlanta gemeldeten Fälle sind seit der Einführung der Meldepflicht kontinuierlich angestiegen. So waren es im Jahr 2000 348 Fälle und im Jahr 2010 schon 1 761 Fälle. Die jährliche Inzidenz betrug im Jahr 2000 1,4 Fälle/1 Million Einwohner. Im Jahr 2010 lag die Inzidenz schon bei 6,1 Fälle/1 Million Einwohner. Die Sterberate blieb allerdings unter 1 % (www.cdc.gov/anaplasmosis). Die Seroprävalenz in den USA schwankt von 0,6 - 14,9 % in den endemischen Gebieten [18]. In den USA wurden 3,5 % der Blutspender positiv getestet [18]. Die klinisch manifeste Infektion erfordert in 36 % der Fälle eine stationäre Behandlung, davon 7 % der Fälle auf einer Intensivstation [20].
Der erste Anaplasmose-Fall in Europa wurde Mitte der 1990er Jahre beschrieben. Seither sind rund 100 Fälle aus Kroatien, der Slowakei, Österreich, Lettland, den Niederlanden, Norwegen, Polen, Spanien, Frankreich und Schweden bekannt [21]. Es gibt bisher keinen nach Richtlinien des CDC bestätigten Fall aus Deutschland. Seroprävalenzstudien zeigen jedoch, dass die deutsche Bevölkerung ebenfalls exponiert ist. Daher ist wohl davon auszugehen, dass die HGA unterdiagnostiziert wird. In Deutschland schwanken die Seroprävalenzraten zwischen 1,9 % - 16 % je nach zum Beispiel Anamnese, Zeckenbefall und Alter der Patienten [22, 23, 24, 25].
Seroprävalenzraten in anderen europäischen Ländern schwanken in der gleichen Größenordnung und generell steigt der Anteil der seropositiven Personen mit dem Alter und ist höher in Populationen mit Zeckenkontakt. Forstarbeiter, Fieberpatienten nach Zeckenbefall und Soldaten, die Outdoor-Training nachgehen, zeigen Seroprävalenzen von 11,4 - 14,9 % in verschiedenen europäischen Ländern [22, 25, 26].
Aus Asien wurden ebenfalls in jüngster Zeit HGA-Fälle berichtet. Beispielsweise wurde in China erstmal 2006 ein Fall berichtet. Die 50-jährige Patientin starb und neun weitere Patienten aus ihrem Umfeld wurden ebenfalls positiv diagnostiziert [27].
Oft wird eine A. phagocytophilum-Infektion zusammen mit einer anderen durch Zecken übertragenen Erkrankung gefunden. So werden oft Antikörper gegen Anaplasma und Borrelia zusammen gefunden. Beispielsweise hatten in der Tschechischen Republik 9,9 % der Patienten mit einem durch FSME verursachten Krankenhausaufenthalt auch Antikörper gegen A. phagocytophilum [28]. Es ist bisher unklar, welche Pathomechanismen zu welcher Krankheitsausprägung führen. Zunächst nahm man an, dass die Schwere der Erkrankung mit der aufgenommenen Menge des Erregers zusammenhing, allerdings wurde dies in späteren Studien widerlegt. Die pathologischen Befunde deuteten eher auf das Potenzial eines Zytokin- oder immuninduzierten Prozesses hin [20]. So wurde unter anderem in Patienten festgestellt, dass weit mehr Leukozyten zerstört werden, als es sich durch die direkte Zerstörung durch die Infektion mit A. phagocytophilum erklären lässt.
Das Medikament der Wahl bei einer HGA sind Tetrazykline. Doxycyclin ist effektiv in der Behandlung von HGA Fällen und führt gewöhnlich in 24 - 48 Stunden zu einer klinischen Verbesserung [21].
Candidatus Neoehrlichia mikurensis
Lange galt der Nachweis von Candidatus Neoehrlichia mikurensis (CNM) aus Zecken und Nagern als durchaus interessanter Nebenbefund, allerdings wurde diesem Erreger keinerlei medizinische Bedeutung beigemessen. Wie bei vielen Infektionskrankheiten, sollte sich dies schon sehr schnell als Irrtum herausstellen. 2010 wurden zwei Fälle aus Deutschland publiziert: im Jahr 2007 ein 69-jähriger Mann mit immunsuppressive Therapie nach Verdacht auf chronisch-entzündliche demyelinisierende Polyneuropathy und im Jahr 2008 ein 57-jähriger Patient mit intrazerebralen und subarachnoidalen Blutungen und einem Aneurisma an der Carotis interna. Letzterer Patient hat trotz Intensivtherapie und Operation nicht überlebt [29]. Zwischen 2008 und 2009 wurden zwei Fälle in der Tschechischen Republik diagnostiziert: eine splenektomierte 55-Jährige mit Mantelzelllymphom und Chemotherapie und ein 58-Jähriger, ebenfalls splenektomiert, der sich aufgrund einer sklerotisierenden Cholangitis drei Jahre zuvor einer Lebertransplantation unterzogen hatte [30]. 2009 wurde CNM bei einem 77-Jährigen in Schweden diagnostiziert, Er war zwei Jahre zuvor nach autoimmun-induzierter Thrombozytopenie und autoimmuner Anämie auf Grund chronischer B-Zell-lymphozytärer Leukämie splenektomiert worden [31]. Ebenfalls 2009 wurde in der Schweiz ein 61-Jähriger sechs Wochen nach einer Bypass-Operation und Mitralklappenrekonstruktion mit einer Neoehrlichiose diagnostiziert [32].
Bis zum Oktober 2012 waren diese sechs Fälle die einzigen labordiagnostisch bestätigten humanen Neoehrlichiosen und sie alle litten an einer Grunderkrankung. Dass keine besondere Disposition vorliegen muss, zeigte ein Bericht aus China. In einer Studie bei 7 von 622 Fieberpatienten im Nordosten des Landes wurde CNM im Blut mittels PCR nachgewiesen [33]. Die Autoren betonen, dass es sich durchweg um sonst gesunde Personen handelte und nicht wie bislang um Menschen, die an einer schweren Hintergrunderkrankung und/oder Immunsuppression litten. Die letzten zwei Fallberichte stammen aus der Schweiz, wo nach entsprechender Doxycyclin-Behandlung beide Patienten schnell fieberfrei wurden und eine restitutio ad integrum gelang [34]. Mit zunehmender Zahl an Berichten über CNM sowohl in Zecken, Nagern als auch Menschen in den letzten 3 Jahren [35, 36] wird sich in naher Zukunft das Bild über die Verbreitung und Häufigkeit von CNM weiter vervollständigen und dann das Gefährdungspotenzial dieses Erregers für die menschliche Gesundheit besser einschätzbar sein.
Schlussfolgerungen
Im Hinblick auf die Humane Granulomatöse Anaplasmose bleibt nach wie vor unklar, warum wir Fälle bei Tieren sehen und den Erreger regelmäßig in Zecken nachweisen können, aber im Gegensatz zu Amerika bislang keine humanen Fälle in Deutschland identifizieren konnten. Die Gründe hierfür sind nicht bekannt, könnten aber in einer fehlenden Diagnoseanforderung der Ärzteschaft auf Grund fehlender Kenntnis der Erkrankung und ihrer Symptome liegen. Eine alternative Arbeitshypothese könnte dies durch verschieden-pathogene Stämme oder auch unterschiedliche Kreisläufe in der Natur erklären. Für beide Szenarien sind ein weiteres Bekanntmachen von Anaplasma phagocytophilum erste Schritte zum Erkenntnisgewinn. Eine entsprechende Charakterisierung von Stämmen aus Deutschland und ein Vergleich mit nordamerikanischen Stämmen sind ebenfalls indiziert.
Bezüglich Candidatus Neoehrlichia mikurensis haben wir ein grobes Bild von der Prävalenz in Deutschland, jedoch ist die gesundheitspolitische Bedeutung dieses Erregers noch schwer abzuschätzen. Hier besteht dringender Forschungsbedarf hinsichtlich der In-vitro-Kultivierung von CNM, um Antigen zu gewinnen, welches über ein serologisches Screening die tatsächliche Exposition und Infektionsraten bei verschiedenen Berufsgruppen zu bestimmen. Auch hier muss weiter über den Erreger informiert werden, damit die Diagnostik bei Verdachtsfällen angefordert wird und entsprechende Therapien initiiert werden können.
Beide Erreger sind in Deutschland in Zecken wiederholt und teilweise auch mit einer bemerkenswerten Prävalenz nachgewiesen worden, so dass hier auch eine wehrmedizinische Bedeutung besteht. Dies gilt bei entsprechenden Übungen im In- wie auch im Ausland und erfordert entsprechende Präventionsmaßnahmen durch Aufklärung der Truppenärzte sowie der konsequenten Verwendung von entsprechend imprägnierter Feld- und Einsatzbekleidung.
Literatur
- Dobler G, Fingerle V, Hagedorn P, Pfeffer M, Silaghi C, Tomaso H, Henning K, Niedrig M: Gefahren der Übertragung von Infektionskrankheiten durch Schildzecken in Deutschland. Bundesgesundheitsbl-Gesundheitsforsch-Gesundheitsschutz 2013; im Druck.
- Dumler JS, Barbet AF, Bekker CP, Dasch GA, Palmer GH, Ray SC, Rikihisa Y, Rurangirwa FR. Reorganization of genera in the families Rickettsiaceae and Anaplasmataceae in the order Rickettsiales: unification of some species of Ehrlichia with Anaplasma, Cowdria with Ehrlichia and Ehrlichia with Neorickettsia, descriptions of six new species combinations and designation of Ehrlichia equi and ‘HGE agent’ as subjective synonyms of Ehrlichia phagocytophila. Int J Syst Evol Microbiol 2001;51(Pt 6):2145-65.
- Stuen S, Granquist EG, Silaghi C: Anaplasma phagocytophilum - a widespread multi-host pathogen with highly adaptive strategies. Front Cell Infect Microbiol 2013; 3: 31.
- Schouls LM, Van De Pol I, Rijpkema SG, Schot CS: Detection and identification of Ehrlichia, Borrelia burgdorferi sensu lato, and Bartonella species in Dutch Ixodes ricinus ticks. J Clin Microbiol 1999; 37: 2215-2222.
- Alekseev AN, Dubinina HV, Van De Pol I, Schouls LM: Identification of Ehrlichia spp. and Borrelia burgdorferi in Ixodes ticks in the Baltic regions of Russia. J Clin Microbiol 2001; 39:2237-2242.
- Sanogo YO, Parola P, Shpynov S et al.: Genetic diversity of bacterial agents detected in ticks removed from asymptomatic patients in northeastern Italy. Ann N Y Acad Sci 2003; 990:182-190.
- von Loewenich FD, Baumgarten BU, Schröppel K, Geissdörfer W, Röllinghoff M, Bogdan C: High diversity of ankA sequences of Anaplasma phagocytophilum among Ixodes ricinus ticks in Germany. J Clin Microbiol 2003; 41:5033-5040.
- Pan HUA, Liu S, Ma Y, Tong S, Sun Y: Ehrlichia-like Organism Gene Found in Small Mammals in the Suburban District of Guangzhou of China. Annals New York Acad Sci 2003; 990:107-111.
- Kawahara M, Rikihisa Y, Isogai E et al.: Ultrastructure and phylogenetic analysis of ‘Candidatus Neoehrlichia mikurensis’ in the family Anaplasmataceae, isolated from wild rats and found in Ixodes ovatus ticks. Intern J Syst Evol Microbiol 2004; 54:1837-1843.
- Herron MJ, Ericson ME, Kurtti TJ, Munderloh UG. The interactions of Anaplasma phagocytophilum, endothelial cells, and human neutrophils. Ann N Y Acad Sci 2005;1063: 374-82.
- Medlock JM, Hansford KM, Bormane A, Derdakova M, Estrada-Peña A, George JC, Golovljova I, Jaenson TG, Jensen JK, Jensen PM, Kazimirova M, Oteo JA, Papa A, Pfister K, Plantard O, Randolph SE, Rizzoli A, Santos-Silva MM, Sprong H, Vial L, Hendrickx G, Zeller H, Van Bortel W. Driving forces for changes in geographical distribution of Ixodes ricinus ticks in Europe. Parasit Vectors. 2013; 2;6:1.
- Kiffner C, Vor T, Hagedorn P, Niedrig M, Rühe F. Factors affecting patterns of tick parasitism on forest rodents in tick-borne encephalitis risk areas, Germany. Parasitol Res. 2011;108(2): 323-35.
- Bown KJ, Begon M, Bennett M, Woldehiwet Z, Ogden NH. Seasonal dynamics of Anaplasma phagocytophila in a rodent-tick (Ixodes trianguliceps) system, United Kingdom. Emerg Infect Dis. 2003; 9(1): 63-70.
- Richter D, Kohn C, Matuschka FR: Absence of Borrelia spp., Candidatus Neoehrlichia mikurensis, and Anaplasma phagocytophilum in questing adult Dermacentor reticulatus ticks. Parasitol Res 2013; 112: 107-111.
- Silaghi C, Woll D, Mahling M, Pfister K, Pfeffer M: Candidatus Neoehrlichia mikurensis in rodents in an area with sympatric existence of the hard ticks Ixodes ricinus and Dermacentor reticulatus, Germany. Parasit Vectors 2012; 5:285.
- Movila A, Toderas I, Uspenskaia I, Conovalov J: Molecular detection of tick-borne pathogens in Ixodes ricinus from Moldova collected in 1960. Ticks Tick-Borne Dis 2013; 4:359-361.
- Yabsley MJ, Murphy SM, Luttrell MP, Wilcox BR, Ruckdeschel C: Raccoons (Procyon lotor), but not rodents, are natural and experimental hosts for an ehrlichial organism related to “Candidatus Neoehrlichia mikurensis”. Vet Microbiol 2008; 131:301-308.
- Jin H, Wei F, Liu Q, Qian J. Epidemiology and control of human granulocytic anaplasmosis: a systematic review. Vector Borne Zoonotic Dis 2012;12(4):269-74.
- Dumler JS, Choi KS, Garcia-Garcia JC, Barat NS, Scorpio DG, Garyu JW, Grab DJ, Bakken JS. Human granulocytic anaplasmosis and Anaplasma phagocytophilum. Emerg Infect Dis 2005;11(12): 1828-34.
- Dumler JS. The biological basis of severe outcomes in Anaplasma phagocytophilum infection. FEMS Immunol Med Microbiol. 2012; 64(1):13-20.
- Silaghi C: Studies on the epidemiology of tick-borne infectious agents. VVB Laufersweiler Verlag, Giessen 2012.
- Fingerle V, Goodman JL, Johnson RC, Kurtti TJ, Munderloh UG, Wilske B: Human granulocytic ehrlichiosis in southern Germany: increased seroprevalence in high-risk groups. J Clin Microbiol 1997; 35: 3244-3247.
- Von Loewenich FD, Stumpf G, Baumgarten BU, Röllinghoff M, Dumler JS, Bogdan C: Human granulocytic ehrlichiosis in Germany: evidence from serological studies, tick analyses, and a case of equine ehrlichiosis. Ann N Y Acad Sci 2003; 990: 116-117.
- Woessner R, Gaertner BC, Grauer MT, Weber K, Mueller-Lantzsch N, Hunfeld KP, Treib J: Incidence and prevalence of infection with human granulocytic ehrlichiosis agent in Germany. A prospective study in young healthy subjects. Infection 2001; 29: 271-273.
- Lillini E, Macri G, Proietti G, Scarpulla M: New findings on anaplasmosis caused by infection with Anaplasma phagocytophilum. Ann N Y Acad Sci 2006; 1081: 360-370.
- Zhang L, Liu Y, Ni D, Li Q, Yu Y, Yu XJ, Wan K, Li D, Liang G, Jiang X, Jing H, Run J, Luan M, Fu X, Zhang J, Yang W, Wang Y, Dumler JS, Feng Z, Ren J, Xu, J: Nosocomial transmission of human granulocytic anaplasmosis in China. JAMA 2008; 300: 2263-2270.
- Zeman P, Pazdiora P, Chmelik V, Januska J, Sedivy K, Guglielmone AA, Iriarte JA, Medkova Z: Epidemiological survey of tick-borne encephalitis virus and Anaplasma phagocytophilum co-infections in patients from regions of the Czech Republic endemic for tick-borne diseases. Wien Klin Wochenschr 2007; 119: 538-543.
- von Loewenich FD, Geissdorfer W, Disque C, Matten J, Schett G, Sakka SG, Bogdan C.: Detection of "Candidatus Neoehrlichia mikurensis" in two patients with severe febrile illnesses: evidence for a European sequence variant. J Clin Microbiol 2010; 48:2630-2635.
- Peková S, Vydra J, Kabicková H et al.: Candidatus Neoehrlichia mikurensis infection identified in 2 hematooncologic patients: benefit of molecular techniques for rare pathogen detection. Diagn Microbiol Infect Dis 2011; 69: 266-270.
- Welinder-Olsson C, Kjellin E, Vaht K, Jacobsson S, Wenneras C: First case of human "Candidatus Neoehrlichia mikurensis" infection in a febrile patient with chronic lymphocytic leukemia. J Clin Microbiol 2010; 48: 1956-1959.
- Fehr JS, Bloemberg GV, Ritter C et al.: Septicemia caused by tick-borne bacterial pathogen Candidatus Neoehrlichia mikurensis. Emerg Infect Dis 2010; 16: 1127-1129.
- Li H, Jiang JF, Liu W et al.: Human infection with Candidatus Neoehrlichia mikurensis, China. Emerg Infect Dis 2012; 18: 1636-1638.
- Maurer FP, Keller PM, Beuret C et al.: Close geographic association of human neoehrlichiosis and tick populations carrying Candidatus Neoehrlichia mikurensis in Eastern Switzerland. J Clin Microbiol 2013; 51: 169-176.
- Rar V, Golovljová I: Anaplasma, Ehrlichia, and "Candidatus Neoehrlichia" bacteria: Pathogenicity, biodiversity, and molecular genetic characteristics, a review. Infect Genet Evol 2011; 11: 1842-1861.
- Jahfari S, Fonville M, Hengeveld P et al.: Prevalence of Neoehrlichia mikurensis in ticks and rodents from North-west Europe. Parasit Vectors 2012; 5: 74.
- Fingerle V, Munderloh UG, Liegl G, Wilske B: Coexistence of ehrlichiae of the phagocytophila group with Borrelia burgdorferi in Ixodes ricinus from Southern Germany. Med Microbiol Immunol 1999; 188: 145-149.
- Oehme R, Hartelt K, Backe H, Brockmann S, Kimmig P: Foci of tick-borne diseases in southwest Germany. Int J Med Microbiol 2002; 291 Suppl 33: 22-29.
- Hildebrandt A, Schmidt KH, Fingerle V, Wilske B, Straube E: Prevalence of granulocytic Ehrlichiae in Ixodes ricinus ticks in Middle Germany (Thuringia) detected by PCR and sequencing of a 16S ribosomal DNA fragment. FEMS Microbiol Lett 2002; 211: 225-230.
- Hartelt K, Oehme R, Frank H, Brockmann SO, Hassler D, Kimmig P: Pathogens and symbionts in ticks: prevalence of Anaplasma phagocytophilum (Ehrlichia sp.), Wolbachia sp., Rickettsia sp., and Babesia sp. in Southern Germany. Int J Med Microbiol 2004; 293 Suppl 37: 86-92.
- Pichon B, Kahl O, Hammer B, Gray JS: Pathogens and host DNA in Ixodes ricinus nymphal ticks from a German forest. Vector Borne Zoonotic Dis 2006; 6: 382-387.
- Silaghi C, Gilles J, Höhle M, Fingerle V, Just FT, Pfister K: Anaplasma phagocytophilum infection in Ixodes ricinus, Bavaria, Germany. Emerg Infect Dis 2008; 14: 972-974.
- Hildebrandt A, Kramer A, Sachse S, Straube E: Detection of Rickettsia spp. and Anaplasma phagocytophilum in Ixodes ricinus ticks in a region of Middle Germany (Thuringia). Ticks Tick Borne Dis 2010; 1: 52-56.
- Schicht S, Junge S, Schnieder T, Strube C: Prevalence of Anaplasma phagocytophilum and Coinfection with Borrelia burgdorferi Sensu Lato in the Hard Tick Ixodes ricinus in the City of Hanover (Germany). Vector Borne Zoonotic Dis. 2011; 11: 1595-1597.
- Schorn S, Pfister K, Reulen H, Mahling M, Manitz J, Thiel C, Silaghi C: Prevalence of Anaplasma phagocytophilum in Ixodes ricinus in Bavarian public parks, Germany. Ticks Tick Borne Dis 2011; 2: 196-203.
- Richter D, Matuschka FR: "Candidatus Neoehrlichia mikurensis," Anaplasma phagocytophilum, and lyme disease spirochetes in questing european vector ticks and in feeding ticks removed from people. J Clin Microbiol 2012; 50: 943-947.
- Silaghi C, Woll D, Hamel D, Pfister K, Mahling M, Pfeffer M: Babesia spp. and Anaplasma phagocytophilum in questing ticks, ticks parasitizing rodents and the parasitized rodents - Analyzing the host-pathogen-vector interface in a metropolitan area. Parasites & Vectors 2012a; 5: 191.
- Overzier E, Pfister K, Thiel C, Herb I, Mahling M, Silaghi C: Anaplasma phagocytophilum in Questing Ixodes ricinus Ticks: Comparison of Prevalences and Partial 16S rRNA Gene Variants in Urban, Pasture, and Natural Habitats. Appl Environ Microbiol 2013; 79: 1730-1734.
- Tappe J, Strube C: Anaplasma phagocytophilum and Rickettsia spp. infections in hard ticks (Ixodes ricinus) in the city of Hanover (Germany): Revisited. Ticks Tick Borne Dis 2013; 4: 432-438.
- Andersson M, Bartkova S, Lindestad O, Raberg L: Co-infection with 'Candidatus Neoehrlichia Mikurensis' and borrelia afzelii in ixodes ricinus ticks in southern Sweden. Vector Borne Zoonotic Dis 2013; 13: 438-442.
- Fertner ME, Molbak L, Boye Pihl TP, Fomsgaard A, Bodker R: First detection of tick-borne "Candidatus Neoehrlichia mikurensis" in Denmark 2011. Euro Surveill 2012; 17:(8) pii=20096.
- van Overbeek L, Gassner F, van der Plas CL, Kastelein P, Nunes-da Rocha U, Takken W: Diversity of Ixodes ricinus tick-associated bacterial communities from different forests. FEMS Microbiol Ecol 2008; 66: 72-84.
- Coipan EC, Jahfari S, Fonville M, Maassen CB, van der Giessen J, Takken W, Takumi K, Sprong H: Spatiotemporal dynamics of emerging pathogens in questing Ixodes ricinus. Frontiers in Cellular and Infection Microbiology 2013; 3: 36.
- Špitalská E, Boldis V, Kostanová Z, Kocianová E, Stefanidesová K: Incidence of various tick-borne microorganisms in rodents and ticks of central Slovakia. Acta Virol 2008; 52: 175-179.
- Pangracova L, Derdakova M, Pekarik L, Hviscova I, Vichova B, Stanko M, Hlavata H, Petko B: Ixodes ricinus abundance and its infection with the tick-borne pathogens in urban and suburban areas of Eastern Slovakia. Parasit Vectors 2013; 6: 238.
- Lommano E, Bertaiola L, Dupasquier C, Gern L: Infections and co-infections of questing Ixodes ricinus ticks by emerging zoonotic pathogens in Western Switzerland. Appl Environ Microbiol 2012; 78: 4606-4612.
- Capelli G, Ravagnan S, Montarsi F et al.: Occurrence and identification of risk areas of Ixodes ricinus-borne pathogens: a cost-effectiveness analysis in north-eastern Italy. Parasit Vector 2012; 5: 61.
- Krücken J, Schreiber C, Maaz D, Kohn M, Demeler ., Beck S, Schein E, Olias P, Richter D, Matuschka FR, Pachnicke S, Krieger K, Kohn B, von Samson-Himmelstjerna G: A novel high-resolution melt PCR assay discriminates Anaplasma phagocytophilum and "Candidatus Neoehrlichia mikurensis". J Clin Microbiol 2013; 51: 1958-1961.
- Vichova B, Majlathova V, Novakova M, Stanko M, Hviscova I, Pangracova L, Chrudimsky T, Curlik J, Petko B: Anaplasma infections in ticks and reservoir host from Slovakia. Infect Genet Evol. 2013; June 11: epub.
- Vayssier-Taussat M, Le Rhun D, Buffet JP et al. : Candidatus Neoehrlichis mikurensis in bank voles, France. Emerg Infect Dis 2012 ; 12: 2063-2065.
- Andersson M, Raberg L : Wild Rodents and Novel Human Pathogen Candidatus Neoehrlichia mikurensis, Southern Sweden. Emerg Infect Dis 2011 ; 17: 1716-1718.
Datum: 01.07.2014
Quelle: Wehrmedizinische Monatsschrift 2014/4