ANTIBIOTIKA RESTRIKTIV VERORDNEN
Erste Wahl bei akuten Bronchitiden und Sinusitiden: Sekretolyse mit Zusatzeffekten
Obwohl 90 % der Atemwegsinfekte durch Viren verursacht sind, werden häufig Antibiotika verordnet. Mit Blick auf deren mangelnde Wirksamkeit bei viralen Erkrankungen, Nebenwirkungen, Kosten und Resistenzentwicklung wird allerdings eine symptomatische Behandlung empfohlen.
Nachweislich gut geeignet ist das mukolytisch, sekretolytisch und sekretomotorisch wirksame Myrtol®* (GeloMyrtol® forte). Dessen klinischer Nutzen ist bei Atemwegsinfekten umfassend belegt, aktuell in einer GCP-konformen Studie bei akuter Bronchitis. Dieses Fazit zogen Pneumologen, HNO-Ärzte und Allgemeinmediziner bei einem Expertengespräch** in Hamburg.
Statt einer Antibiose ist nach Ansicht der Experten bei Atemwegsinfekten eine symptomatische Therapie indiziert mit dem vorrangigen Ziel, den Schleim zu lösen und die natürlichen Reinigungsmechanismen zu aktivieren. „Die Schleimbeschaffenheit muss verbessert und die Zilienschlagfrequenz erhöht werden“, erläuterte die Allgemeinmedizinerin Dr. Petra Sandow, Berlin. Außerdem sollte die Entzündung gehemmt und eine Abschwellung der Schleimhäute erzielt werden. Erreichen lässt sich dies mit Substanzen wie dem Phytotherapeutikum GeloMyrtol® forte, das mukolytisch, sekretolytisch und sekretomotorisch wirkt. Der zähe Schleim wird gelöst, das Sekret verflüssigt und das Abhusten gefördert. Zusätzlich konnten für Myrtol® entzündungshemmende, antimikrobielle und bronchospasmolytische Effekte gezeigt werden. Mit Blick auf das Konzept der „United Airways“, also der funktionellen Einheit der oberen und unteren Atemwege, sollte eine kombinierte therapeutische Strategie zur Behandlung der oberen und unteren Atemwege angewandt werden. Gut dafür geeignet ist Myrtol®, da es für beide Indikationen explizit zugelassen ist.
Umfassende Datenlage für Myrtol®
Zu den Wirkeigenschaften von GeloMyrtol® forte bei akuter und chronischer Bronchitis und Sinusitis liegen derzeit 27 klinische Studien vor. Das Phytotherapeutikum führt bei 90 % der Bronchitis-Patienten bereits nach einer Woche zu einer Heilung, bzw. verbessert ihre Symptomatik deutlich. Zu diesem Ergebnis kommt aktuell eine multizentrische, randomisierte, doppelblinde, plazebokontrollierte klinische Studie (Gillissen A et al. Drug Research, 2013; 63:19-27).
Abb. 1
Methodisch hochwertig
In die Parallelgruppenuntersuchung wurden 413 erwachsene Patienten mit akuter Bronchitis eingeschlossen. Als Therapie erhielten die Patienten entweder täglich vier Weichkapseln à 300 mg Myrtol® (n=202) oder vier Plazebo-Weichkapseln (n=211). Der Verlauf der Erkrankung wurde nach sieben, zehn u
Abb. 2
Hustenanfälle signifikant im Vergleich zu Plazebo reduziert
Bereits nach einer Woche hatte sich die Häufigkeit der Hustenanfälle, des Hauptsymptoms der akuten Bronchitis, unter Myrtol® signifikant im Vergleich zu Plazebo reduziert. Ebenfalls nach einer Woche zeigte sich ein Heilungsvorsprung von Myrtol® gegenüber Plazebo von drei Tagen (Abb. 1). „GeloMyrtol® forte reduziert die Erkrankungszeit hochsignifikant“, erläuterte Autor Prof. Dr. Adrian Gillissen, Kassel, das Ergebnis. Schon nach sieben Tagen zeigt sich ein deutlicher Heilungsvorsprung von drei Tagen gegenüber Plazebo. Auch zahlreiche sekundäre Studienparameter besserten sich deutlich gegenüber Plazebo: In der Myrtol®-Gruppe zeigte sich
- eine signifikant geringere Hustenfrequenz,
- ein signifikanter Rückgang der täglichen Hustenanfälle,
- ein signifikant leichteres Abhusten,
- eine signifikante Reduktion der Hustenanfälle in der Nacht.
Die Verträglichkeit des Phytopharmakons war gut, unerwünschte Ereignisse traten in Verum- und Plazebo-Gruppe gleich häufig auf.
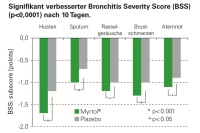
Signifikante Verbesserung des Bronchitis- Severity-Scores
Der Bronchitis-Severity- Score (BSS) verbesserte sich unter Myrtol® rasch und wies ebenfalls bei jeder Arztvisite signifikant niedrigere Werte auf als in der Plazebo-Gruppe (Abb. 2). Dies traf auch auf die einzelnen BSS-Subscores zu, wie Husten, Sputummenge, Rasselgeräusche, Brustschmerzen und Dyspnoe (Abb. 2). Gillissen, A. et al., A Multi-centre, Randomised, Double-blind, Placebo controlled Clinical Trial on the Efficacy and Tolerability of GeloMyrtol® forte in Acute Bronchitis, Drug Research, 2013; 63:19-27.
Myrtol®, eingetragene Marke von Pohl-Boskamp Destillat aus einer Mischung von rektifiziertem Eukalyptusöl, rektifiziertem Süßorangenöl, rektifiziertem Myrtenöl und rektifiziertem Zitronenöl (66:32:1:1) ** Expertengespräch „Nutzen und Risiken von Antibiotika in der Therapie von akuten Atemwegsinfekten“ am 15. Juni 2013 in Hamburg
GeloMyrtol® forte. Zur Schleimlösung und Erleichterung des Abhustens bei akuter und chronischer Bronchitis. Zur Schleimlösung bei Entzündungen der Nasennebenhöhlen (Sinusitis). Wirkstoff: Destillat aus einer Mischung von rektifiziertem Eukalyptusöl, rektifiziertem Süßorangenöl, rektifiziertem Myrtenöl und rektifiziertem Zitronenöl (66:32:1:1). Zus.: 1 magensaftresist. Weichkps. enth. 300 mg Destillat aus einer Mischung von rektifiziertem Eukalyptusöl, rektifiziertem Süßorangenöl, rektifiziertem Myrtenöl und rektifiziertem Zitronenöl (66:32:1:1). Hilfsst.: Raffiniertes Rapsöl, Gelatine, Glycerol 85 %, Sorbitol-Lösung 70 % (nicht kristallisierend), Hypromelloseacetatsuccinat, Triethylcitrat, Natriumdodecylsulfat, Talkum, Dextrin, Glycyrrhizinsäure, Ammoniumsalz. Gegenanz.: Nicht anwenden bei entzündl. Erkr. i. Bereich Magen- Darm u. d. Gallenwege, schweren Lebererkr., bek. Überempfindlichkeit gegen einen d. Bestandt. des Arzneim., bei Säuglingen und Kindern unter 6 Jahren; Nebenw.: häufig: Magen- oder Oberbauchschmerzen, gelegentlich: allergische Reaktionen (wie Atemnot, Gesichtsschwellung, Nesselsucht, Hautausschlag, Juckreiz), Entzündung der Magenschleimhaut oder der Darmschleimhaut, Übelkeit, Erbrechen, Durchfall oder andere Verdauungsstörungen, Geschmacksveränderungen, Kopfschmerzen oder Schwindel, sehr selten: In-Bewegung- Setzen von vorhandenen Nieren- und Gallensteinen, Häufigkeit nicht bekannt: schwere anaphylaktische Reaktionen. G. Pohl-Boskamp GmbH & Co. KG, 25551 Hohenlockstedt (01/10)
Datum: 05.11.2013
Quelle: Wehrmedizin und Wehrpharmazie 2013/3