Untersuchungen an humanen induzierten pluripotenten Stammzellen – strahleninduzierte elektrophysiologische -Effekte und Genexpressionsveränderungen in Kardiomyozyten
¹Institut für Radiobiologie der Bundeswehr, München
²Institut für Pharmakologie und Toxikologie der Bundeswehr, München
³Abteilung für Elektrophysiologie der Medizinischen Klinik II der Universitätsklinik Bonn
Einleitung
In der täglichen Arbeit des medizinischen A-Aufklärungs- und Diagnosetrupps der Task Force Medizinischer ABC-Schutz stellt die Identifikation und Behandlung von Patienten mit einer akuten Strahlenkrankheit eine besondere Herausforderung dar. Das Auftreten von strahleninduzierten Herzrhythmusstörungen ist hierbei ein bekanntes Phänomen. Die Veränderungen treten meist Wochen bis Jahre nach Exposition [1], jedoch auch kurzfristig nach Bestrahlung [2, 3] auf. Diese kurzfristigen Veränderungen gehen nicht nur mit Implikationen für die akute Therapie einher, sondern werfen auch die Frage nach der Notwendigkeit einer kardialen Überwachung der Patienten während einer möglichen Latenzphase des akuten Strahlensyndroms auf. Besonders bei einem Massenanfall von Strahlenverletzten sollte hierbei auch eine Abwägung im Hinblick auf eine mögliche Ressourcenknappheit erfolgen. Aufgrund der schlechten Datenlage bezüglich dieser Problematik durch die allgemein schwierige Untersuchung von strahleninduzierten biologischen Prozessen in vivo, bei nur eingeschränkt zur Verfügung stehenden Patientenproben, fällt eine allgemeine Empfehlung diesbezüglich momentan jedoch schwer. Moderne radiobiologische Ansätze könnten hier Abhilfe schaffen. Dazu gehören Untersuchungen an humanen induzierten pluripotenten Stammzellen (hiPSC), die vielfältige Möglichkeiten eröffnen, um organspezifische Effekte im humanen Modell ohne relevante ethische Implikationen zu evaluieren [4]. In dieser Studie haben wir an hiPSC-Kardiomyozyten mit endogener Schrittmacheraktivität kurzfristige Änderungen des elektrophysiologischen Verhaltens sowie Alterationen der Genexpressionssignatur mittels „Next Generation Sequencing“ nach Röntgenstrahlenexposition untersucht. Ziel war es, Schwellendosen für das Auftreten von strahleninduzierten Rhythmusstörungen sowie mögliche Ursachen auf Genebene zu identifizieren.
Methoden
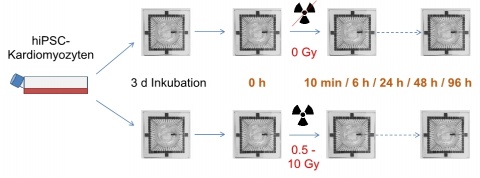
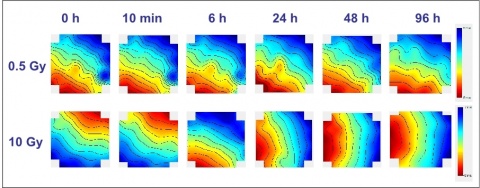
PSC-Kardiomyozyten mit spontaner Schrittmacheraktivität (Cor4U©, Axiogenesis, Cologne, Germany) wurden als Monoschicht auf einem Ein-Well Multielektrodenarray mit jeweils 60 Einzelelektroden (MCS, Reutlingen, Germany) kultiviert. Nach Exposition mit 0, 0,5, 1, 2, 5 bzw. 10 Gy Röntgenstrahlung wurden die elektrophysiologischen Änderungen im Zeitverlauf untersucht (Abbildung 1).Auch die räumliche Erregungsausbreitung im Zellverband konnte mit diesem System erfasst werden. Um die Reaktion der Zellen auf Röntgenstrahlung bezüglich Viabilität zu überprüfen wurde ein Zellviabilitätsassay (CellTiter 96® Aqueous, Promega Corporation, Madison, USA) mit korrespondierenden Dosen und Zeitpunkten bis 120 h nach Exposition durchgeführt. Die differentielle Genexpression konnte nach Hochdurchsatz--RNA-Sequenzierung analysiert werden (Sequenzierung auf NextSeq500 (Illumina, San Diego, CA, USA) mit 75 bp paired-end reads). Zur Auswertung der Daten wurden verschiedene bioinformatische Werkzeuge verwendet („bcltofastq“, „salmon“, „tximport“, „DESeq2“).
Ergebnisse
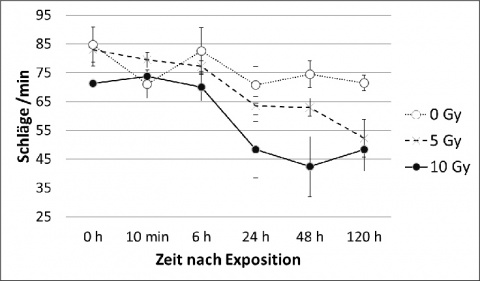
Die verwendeten hiPSC-Kardiomyozyten zeigten, analog zu primären humanen Kardiomyozyten, eine hohe Expression klassischer kardialer Gene, wie HCN4 und ACTC1, sowohl in der unbestrahlten Kontrollgruppe als auch nach Exposition gegenüber Röntgenstrahlung. Differentiell fand sich nach Bestrahlung besonders eine Herunterregulation von Genen, die mit dem Zellzyklus in Verbindung stehen.
Diskussion/Fazit
Insgesamt eröffnen humane induzierte pluripotente Stammzellen hervorragende neue Möglichkeiten für die Erforschung von organspezifischen Veränderungen nach Exposition gegenüber ionisierender Strahlung. Dies ist in der Radiobiolgie von immensem Interesse, da Patientenproben nur sehr begrenzt zur Verfügung stehen, und Übertragungen aus dem Tiermodell bei großer Interspeziesvariabilität nur bedingt möglich sind. Das vorgestellte Modell bietet zudem den Vorteil flexibler Differenzierung, was bislang nur mit embryonalen Stammzellen und allen hiermit verbundenen Einschränkungen und ethischen Implikationen möglich war. Außerdem können durch die Kombination mit modernen molekulargenetischen Verfahren, wie der hier vorgestellten Genexpressionsanalyse mittels „Next Generation Sequencing“, Veränderungen des Genoms und Epigenoms mit enormer Auflösung nachgewiesen werden. Eine zielgerichtete Übertragung der Ergebnisse in die klinische Versorgung von Patienten erscheint damit zukünftig möglich.
Literatur:
- Senkus-Konefka E, Jassem J: Cardiovascular effects of breast cancer radiotherapy. Cancer treatment reviews 2007; 33: 578 - 593.
- Lagrange J-L, Darcourt J, Benoliel J, Bensadoun R-J, Migneco O: Acute cardiac effects of mediastinal irradiation: Assessment by radionuclide angiography. International Journal of Radiation Oncology* Biology* Physics 1992; 22: 897 - 903.
- Larsen RL, Jakacki RI, Vetter VL, Meadows AT, Silber JH, Barber G: Electrocardiographic changes and arrhythmias after cancer therapy in children and young adults. The American journal of cardiology1992; 70: 73 - 77.
- Germanguz I, Sedan O, Zeevi-Levin N et al.: Molecular characterization and functional properties of cardiomyocytes derived from human inducible pluripotent stem cells. Journal of cellular and molecular medicine 2011; 15: 38 - 511.
Oberstabsarzt Dr. Benjamin V. Becker
E-Mail: benjamin3becker@bundeswehr.org
Der Vortrag wurde mit dem 1. Preis ausgezeichnet.
Datum: 13.12.2017
Quelle: Wehrmedizinische Monatsschrift 12/2017