Closed Loop Medication Management und Unit-Dose in der klinischen Arzneimittelversorgung
Ein Meilenstein der Arzneimitteltherapiesicherheit
O. Zube, A. Steinbeck
Arzneimitteltherapiesicherheit im Krankenhaus
Der Verordnungs- und Stellprozess von Arzneimitteln ist mit hohen Risiken für die Arzneimitteltherapiesicherheit behaftet. Schätzungen gehen davon aus, dass 5–15 % der stationär behandelten Patienten in Deutschland unerwünschte Arzneimittelwirkungen (UAW) erleiden. Laut dem „Krankenhaus-Report 2014“ fallen in Deutschland 1,8 Mio. zusätzliche Krankenhaustage aufgrund von UAW an. Mögliche Ursachen hierfür sind laut einer Auswertung des Berichtssystems für Medikationsfehler des Bundesverbands Deutscher Krankenhausapotheker e. V. (ADKA) aus dem Jahre 2006 vielfältig. Bis zu insgesamt 50 % entfallen demnach auf Dosierungsfehler, Verordnungen eines falschen Arzneimittels sowie Doppelverordnungen und Applikationsfehler.
Eine Vielzahl von Organisationen und Verbände engagieren sich seit Jahren für eine Reduktion dieser Risiken. Dazu zählen das Bundesministerium für Gesundheit, der Gemeinsame Bundesausschuss wie auch die Standesvertretungen der Gesundheitsberufe. Zu erwähnen ist hier zudem das Aktionsbündnis Patientensicherheit. Seinen Zielsetzungen sehen sich auch die Bundeswehrkrankenhäuser (BwKrhs) verpflichtet. Es ist mittlerweile gut belegt, dass computergestützte Verordnungs- und Entscheidungssysteme Medikationsfehler signifikant reduzieren. Ein in sich geschlossener Medikationsprozess (Closed Loop Medication Management – CLMM) kann durch Nutzung dieser Systeme effektiv unterstützt werden. Hier spielen klinisch tätige ApothekerInnen im Rahmen der pharmazeutischen Patientenbetreuung eine wichtige Rolle.
Die Aufgaben reichen dabei von der Arzneimittelanamnese über die Arzneimittelversorgung bis hin zum Entlassmanagement. ApothekerInnen werden so zum unverzichtbaren Mitglied eines interprofessionellen therapeutischen Teams. Ein wesentlicher Bestandteil des CLMM-Prozesses ist die sogenannte Unit-Dose Versorgung. In der Apotheke werden dabei für die PatientInnen direkt und automatisiert für einen Einnahmezeitpunkt einzeln in Blister verpackte Arzneimittel bereitgestellt und in die medizinischen Abteilungen geliefert. Dieser Bereitstellungsprozess ist laut Arzneimittelgesetz (AMG) als Herstellungsschritt zu betrachten.
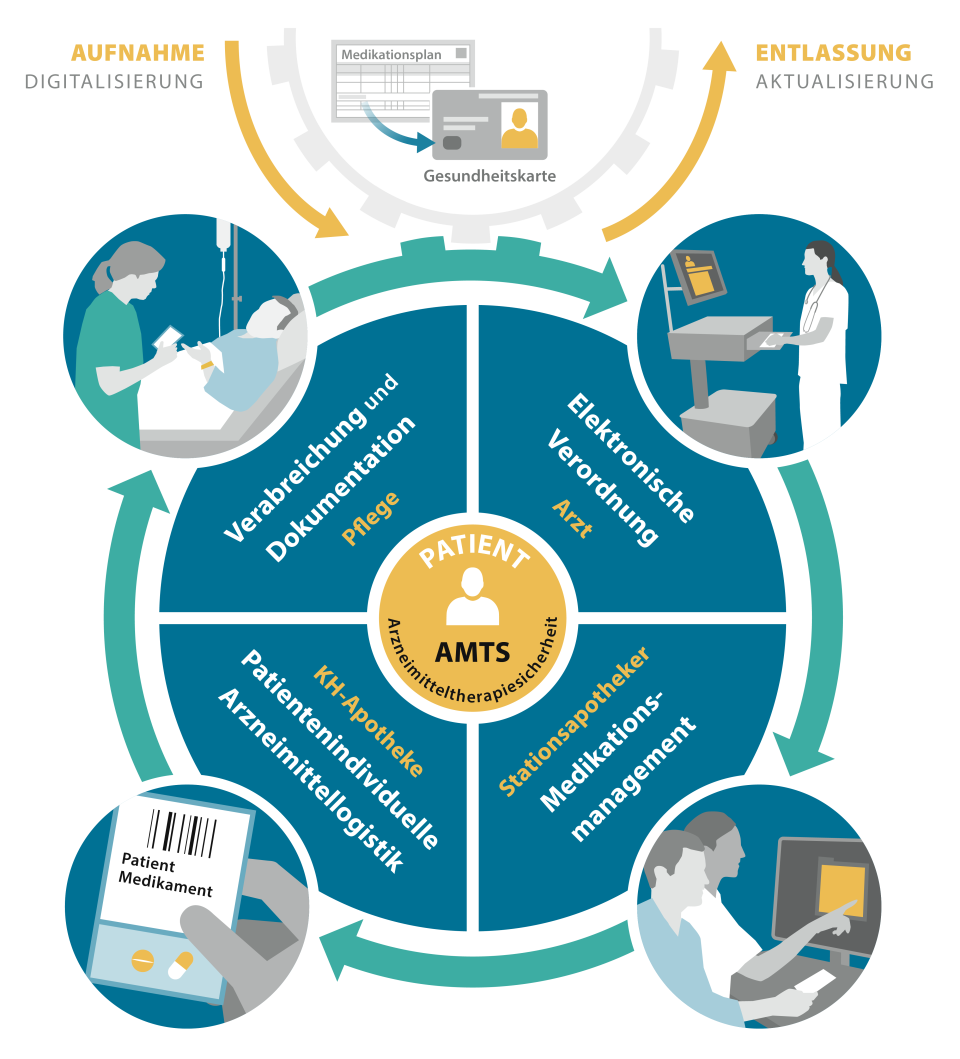
Closed Loop Medication Management
Nicht zuletzt seit dem 2020 in Kraft getretenen Krankenhauszukunftsgesetz befindet sich das Medikationsmanagement in deutschen Kliniken im Umbruch. Der ADKA hat daher bereits in seinem Zielpapier 2014 (fortgeschrieben als Ziele 2021) mit der „7-R-Regel“ (richtiger Patient, richtiges Arzneimittel, richtige Dosierung, richtige Arzneiform, richtiger Applikationsweg, richtiger Zeitpunkt und richtig informieren und dokumentieren) gefordert, den Medikationsprozess entsprechend zu gestalten.
Ein CLMM ist nach Meinung aller bisher genannten Akteure ein Muss für Krankenhäuser, die im Sinne einer verbesserten Arzneimitteltherapiesicherheit und damit einer Erhöhung der Patientensicherheit zukunftsfähig sein wollen. Er umfasst im wesentlichen folgende Prozessschritte: die elektronische Verordnung durch eine ÄrztIn, das interprofessionelle und validierte Medikationsmanagement durch eine ÄrztIn sowie eine klinische ApothekerIn, die patientenindividuelle Arzneimittellogistik als Unit-Dose durch die Krankenhausapotheke und die Verabreichung und Dokumentation der Arzneimittel durch Pflegepersonal mit der barcodegestützten Verifizierung „richtiger Patient – richtiges Arzneimittel“.
Grundvoraussetzung für alle Prozessschritte ist die Einführung und Nutzung einer elektronischen Patientenakte mit einem EDV-gestütztem Verordnungssystem nicht nur für Arzneimittel, sondern für alle therapeutischen Leistungen von der Aufnahme über den Stationsaufenthalt bis zur Entlassung. Im interprofessionellen Medikationsmanagement prüft die klinische ApothekerIn die elektronische ärztliche Verordnung im selben System. Dabei können Optimierungen (z. B. nach Prüfung auf Interaktionen) digital vorgeschlagen werden, die wiederum ärztlich zu prüfen sind und gegebenenfalls zu einer Anpassung der Verordnung führen. Die schließlich freigegebene Verordnung wird online in die Krankenhausapotheke gesendet. Hier erfolgt die automatisierte patientenindividuelle Verblisterung der peroralen Arzneimittel mittels Unit-Dose-Automat.
Auf diesen Prozessschritt wird im nachfolgenden Abschnitt detaillierter eingegangen. Die u. a. mit einem Barcode zur Patientenidentifizierung versehenen, einzeln verpackten Arzneimittelblister werden in die medizinischen Abteilungen geliefert. Dort ermöglicht dieser Barcode mit den Patientendaten eine Verifizierung – richtiges Arzneimittel/richtiger Patient – am „Point of Care“, bevor die Arzneimittel durch die MitarbeiterInnen des Pflegedienstes verabreicht werden. Der „Loop“ ist somit geschlossen. Anschließend wird die Applikation in der elektronischen Patientenakte dokumentiert.
Aus pharmazeutischer Sicht stellt neben den fachlich-beratenden Tätigkeiten der klinisch eingebundenen ApothekerInnen die Unit-Dose-Versorgung das Kernstück im CLMM dar. Diese Art der Versorgung soll automatisiert ablaufen, indem für definierte Einnahmezeitpunkte individuell gestellte Arzneimittel in einzeln verpackte Blister zur Verfügung gestellt werden.

Rechtlicher Rahmen
Das patientenindividuelle Verblistern ist gemäß den Begriffsbestimmungen der Apothekenbetriebsordnung (ApBetrO) die auf Einzelanforderung vorgenommene und patientenbezogene manuelle oder maschinelle Neuverpackung von Fertigarzneimitteln für bestimmte Einnahmezeitpunkte des Patienten in einem nicht wieder verwendbaren Behältnis. Diese Tätigkeit erfüllt die Definition der Herstellung im AMG, sodass hierfür grundsätzlich eine behördliche Herstellungserlaubnis (§ 13 Abs. 1 AMG) mit der Erfüllung aller daran gebundenen rechtlichen Anforderungen erforderlich ist. Ausgenommen von dieser Erlaubnispflicht sind unter anderem Krankenhausapotheken, wenn sie Arzneimittel im Rahmen des üblichen Apothekenbetriebs herstellen. Dies gilt beispielsweise für die Versorgung von PatientInnen der eigenen Klinik mit aufgrund einer ärztlichen Verordnung eigens für diese angefertigten Arzneimitteln (sogenannte Rezepturherstellung nach § 7 ApBetrO). Für innerhalb einer Krankenhausapotheke im Rahmen der Rezeptur patientenindividuell verblisterte Arzneimittel besteht zudem keine Zulassungspflicht nach dem AMG. Das maschinelle Verblistern ist jedoch bei der zuständigen Aufsichtsbehörde, in der Bundeswehr dem Arzneimittelüberwachungsbeauftragten der Bundeswehr, entsprechend anzuzeigen. Weiterhin sind u. a. folgende Richtlinien und Empfehlungen zu betrachten: das Aide-mémoire 07120201 „Maschinelles patientenindividuelles Verblistern von Arzneimitteln“ der Arbeitsgruppe Arzneimittel-, Apotheken-, Transfusions- und Betäubungsmittelwesen der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten, die ADKA-Leitlinie „Anforderungen an eine Unit-Dose Versorgung in der Krankenhausapotheke“ und die Leitlinie der Bundesapothekerkammer „Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Einnahmezeitpunkte“.
An das Verblistern knüpft die ApBetrO besondere qualitative, räumliche, personelle und hygienische Rahmenbedingungen. So ist der Apothekenleiter verpflichtet, in einem Qualitätsmanagementsystem detaillierte Festlegungen zum Herstellungsverfahren zu treffen. Das Personal muss ausreichend qualifiziert sein und regelmäßig geschult werden. Es muss eine schriftliche Herstellungsanweisung vorliegen. Darüber hinaus ist für das maschinelle Verblistern ein separater Raum erforderlich, welcher ausschließlich diesem Zweck dienen darf und dessen Zugang über eine Schleuse erfolgt.
Zu der im Zusammenhang mit der apothekenüblichen Rezepturherstellung in der Apotheke durchzuführenden Plausibilitätsprüfung gehört im Falle der Herstellung patientenindividueller Blister neben der Prüfung der Verordnung auch die Beurteilung der grundsätzlichen Eignung eines Arzneimittels, über einen Automaten verblistert werden zu können. Dabei müssen verschiedene fachliche Aspekte berücksichtigt werden. So führt es gegebenenfalls zu einem Ausschluss, wenn das Arzneimittel ein hohes sensibilisierendes Potenzial hat, es ein Hormon, Antibiotikum oder Zytostatikum ist, es hygroskopisch, oxidationsempfindlich, lichtempfindlich, bruch- oder abriebempfindlich ist oder wenn seine Kompatibilität mit dem verwendeten Verpackungsmaterial nicht gegeben ist.
Die produzierten Unit-Dose-Blister müssen entsprechend den Vorgaben der ApBetrO mit Angaben zur eindeutigen Identifizierbarkeit des Patienten (z. B. Name, Geburtsdatum, Fallnummer, Zimmernummer – sinnvoll barcodegestützt), Bezeichnung des verwendeten Fertigarzneimittels und dessen Chargenbezeichnung, Verfalldatum und Chargenbezeichnung des neuverpackten Arzneimittels, Einnahmehinweisen, gegebenenfalls zu berücksichtigenden Lagerungshinweisen (da Herstellung) und Name sowie Anschrift der abgebenden Apotheke. gekennzeichnet werden. Um den Kennzeichnungsvorgaben hinsichtlich des Beifügens der Packungsbeilage zu entsprechen, kann auch ein QR-Code mit der digitalen Verknüpfung zu dieser auf den Blister aufgebracht werden.
Zahlreiche Studien kommen zu dem Ergebnis, dass eine Automatisierung des Verblisterungsprozesses, verbunden mit einer hundertprozentigen, ebenfalls automatisierten Überprüfung der hergestellten Blister, zu einer Fehlerquote an falsch verblisterten Arzneimitteln von unter 0,01 % führen. Aus der Literatur sind Fehlerquoten beim Dispensieren von Arzneimitteln durch das Pflegepersonal von zum Teil deutlich über einem Prozent bekannt.
Ausblick
Im Mai 2019 wurde das BwKrhs Hamburg durch den vom Kommandeur Gesundheitseinrichtungen gezeichneten Befehl Nr. 1 mit der „Einführung einer Unit-Dose Versorgung im Rahmen des Geschlossenen Medikationsmanagements“ beauftragt. Schnell war dem beauftragten Team klar, dass es sich dabei nicht allein um die Beschaffung eines geeigneten Verblisterungsautomaten für die Krankenhausapotheke handelt. Vielmehr bedeutet die Einführung eines CLMM ein herausforderndes Veränderungsmanagement, in dessen Mittelpunkt die Einführung einer elektronischen Patientenakte stehen muss. Voraussetzung für eine erfolgreiche Umsetzung ist das gemeinsame Agieren eines interdisziplinären Teams aus Krankenhausleitung, Krankenhausinformationssystem-Administration, Pflegedienstleitung, ärztlichen und pflegerischen MitarbeiterInnen der Pilotstation, S6-Abteilung, Krankenhausapotheke und nicht zuletzt die Unterstützung der übergeordneten Führung. Letztere ist insbesondere notwendig, um Fragestellungen wie die Ausbringung von WLAN in den BwKrhs, die Einführung von mobilen Visitenwagen sowie vor allem die Einführung einer elektronischen Patientenakte bewältigen zu können.
Eine stringente Digitalisierung aller Prozesse wird letztlich den beabsichtigten Erfolg der Erhöhung der Arzneimitteltherapiesicherheit bringen. Damit wird nicht zuletzt auch das Pflegepersonal im Stell- und Verabreichungsprozess unterstützt, da diese durch die Closed-Loop-Prozesse validiert werden. Das Stellen der Medikation entfällt weitgehend und der Verblisterungsprozess gewährleistet die Richtigkeit der Verabreichung.
Alle angesprochenen Akteure engagieren sich seit der Befehlsgebung auch unter der parallelen Bewältigung einer Pandemie fortlaufend mit dem Aufbau einer Unit-Dose Versorgung mit dem Ziel des CLMM. Gemeinsames Ziel aller Anstrengungen ist es, mit jedem einzelnen Projektschritt die Patienten- und Arzneimitteltherapiesicherheit am BwKrhs Hamburg stetig zu verbessern. Das BwKrhs Hamburg hat den Auftrag, die Grundlagen für eine Einführung des CLMM in allen anderen BwKrhs in Pilotfunktion zu erarbeiten. Ziel ist es, erste Erfolge in 2023 sichtbar zu machen.
Wehrmedizin und Wehrpharmazie 1/2023
Oberstapotheker O. Zube
Bundeswehrkrankenhaus Hamburg
Lesserstraße 180
22049 Hamburg
E-Mail: [email protected]