EVALUATION EINES TIERVERSUCHSFREIEN IN-VITRO-TESTVER-FAHRENS ZUR IDENTIFIZIERUNG POTENZIELLER KONTAKTALLERGENE
Aus der Abteilung für Innere Medizin (Leitender Arzt: Oberstarzt Dr. U. Baumgarten) des Bundeswehrkrankenhauses Berlin (Chefarzt: Oberstarzt Dr. W. Düsel), Akademisches Lehrkrankenhaus der Charité – Universitätsmedizin Berlin
von Maximilian Schreiner*
Zusammenfassung
Einleitung:
Die Kontaktallergie ist eine der häufigsten Erkrankungen des menschlichen Immunsystems und als häufige berufsbedingte Erkrankung von volkswirtschaftlicher und wehrmedizinischer Bedeutung.
Die prädiktive Identifizierung von potenziellen Kontaktallergenen und deren Restriktion im Alltag und im Berufsleben kann die Prävalenz dieser Erkrankung senken. Derzeit bestehen die zu diesem Zweck validierten und von Behörden anerkannten Tests ausnahmslos in Tierversuchen. Die Entwicklung einer tierversuchsfreien Alternative ist ethisch wünschenswert. Ziel war hier die Evaluation eines neuartigen In-vitro-Testverfahrens zur Identifizierung potenzieller Kontaktallergene.
Methoden:
Das Testsystem basiert auf dem Einsatz von Kokulturen humaner Keratinozyten aus Epidermisresten nach plastischen Operationen und Monozyten aus Blutspenden. Die Monozyten wurden durch Hinzugabe von Zytokinen (GM-CSF, TGF-b und IL-4) zu „Langerhans-Zell-ähnlichen Zellen“ der Haut differenziert und nach 48-stündiger Inkubation mit der zu testenden Substanz geerntet. Das Ausmaß der durchflusszytometrisch gemessenen CD86-Expression zeigt an, ob und wie stark die getestete Substanz als Kontaktallergen wirken kann.
Ergebnisse:
Zur Evaluation des Testsystems wurden 6 bekannte Kontaktallergene getestet, darunter Inhaltsstoffe von Deodorants (Isoeugenol, a-Hexylzimtaldehyd) und Haarfärbemitteln (Paraphenylendiamin). Alle getesteten Allergene riefen eine vermehrte Expression von CD86 auf den Langerhans-Zell-ähnlichen Zellen hervor.
Schlussfolgerungen:
Die erste Evaluation des tierversuchsfreien In-vitro-Testverfahrens zur Identifizierung potenzieller Kontaktallergene war vielversprechend. Alle getesteten Kontaktallergene wurden korrekt durch Bestimmung der Hochregulation von CD86 erkannt. Über das Ausmaß der CD86-Expression konnte auch eine Stärkeeinteilung der Kontaktallergene vorgenommen werden, die bis auf eine Ausnahme (a-Hexylzimtaldehyd) mit den bekannten Daten aus Tierversuchen übereinstimmte.
Evaluation of an animal-free in vitro-assay for identification of potential contact allergens
Summary
Introduction:
Contact allergy is one of the most common autoimmune disorders. As a frequent occupational disease, it is of economic and military medical concern. Predictive identification of potential contact allergens and their subsequent restriction in everyday life and occupational environment can lower the prevalence of this disease. Currently, all validated and approved assays for this purpose are based on animals. Development of animal- free alternatives is ethically desirable. The aim was to evaluate a novel in vitro-assay for identification of potential contact allergens.
Methods:
This assay is based on a co-culture of human keratinocytes from removed epidermis during plastic surgery and monocytes from blood donors. Monocytes were differentiated to cells resembling Langerhans cells of the skin after treatment with cytokines (GMCSF, TGF-b und IL-4) and were harvested after 48 hours of treatment with a test compound. Levels of CD86 expression as measured by flow cytometry indicate classification of a tested chemical as a contact allergen and, if applicable, its strength.
Results:
The assay was evaluated with six known contact allergens including fragrants (isoeugenol, a-hexyl cinnamaldehyde) and hair dyes (para-phenylenediamine). All tested contact allergens increased CD86 expression on Langerhans cell related cells.
Conclusions:
First evaluation of this in vitro-assay was promising: all of the six substances were correctly assessed as contact allergens by up-regulation of CD86. Intensity of CD86 expression allowed for classification of relative strength, which corresponded (except for a-hexyl cinnamaldehyde) with published data from animal trials.
1. Einführung
Die allergische Kontaktdermatitis ist eine der häufigsten Erkrankungen des menschlichen Immunsystems mit einer Prävalenz in der Bevölkerung westlicher Industrieländer von 19,5 % [1]. Insbesondere in der Arbeitsmedizin – und somit auch in der Wehrmedizin – hat sie eine hohe Relevanz. In Deutschland gingen bei den Berufsgenossenschaften 2008 insgesamt 19 126 Meldungen auf Verdachtsfälle einer berufsbedingten Hauterkrankung ein [2]. Auch wenn die Statistik hier nicht näher aufschlüsselt, weiß man auf europäischer Ebene, dass von den berufsbedingten Hauterkrankungen circa 10 % auf das Krankheitsbild der allergischen Kontaktdermatitis zurückgehen – mit einer steigenden Tendenz [3].
Die allergische Kontaktdermatitis ist eine Hypersensitivitätsreaktion vom Typ IV. Im Gegensatz zu den Typen I bis III, die Antikörper-vermittelt sind (zum Beispiel über IgE wie bei Typ I), ist der Pathomechanismus bei der Typ IV-Allergie über zytotoxische T-Zellen vermittelt [4]. Es wird zwischen einer Sensibilisierungs- und einer Effektorphase unterschieden. Die Sensibilisierungsphase läuft stumm ab und wird vom Patienten nicht bemerkt. Frühestens ab dem zweiten Kontakt mit einem Allergen kann das eigentliche klinische Erscheinungsbild der Kontaktdermatitis in Form der Effektorphase in Erscheinung treten.
In der Sensibilisierungsphase erfolgt die Bildung des immunologischen Gedächtnisses. Nach Penetration des Stratum corneum trifft ein potenzielles Allergen in der Epidermis auf Langerhans- Zellen als Antigen-präsentierende Zellen der Haut. Die Mehrheit der Allergene besitzt nur ein geringes Molekulargewicht und ist von sich aus nicht in der Lage, eine Immunantwort zu provozieren. Diese sogenannten Haptene müssen eine Bindung mit körpereigenen Proteinen eingehen, um einen Komplex zu bilden, der von Langerhans- Zellen phagozytiert und auf ihrer Oberfläche präsentiert werden kann. Während der anschließenden Wanderung zu den lokalen Lymphknoten machen die Langerhans-Zellen eine Reifung durch, wobei unter anderem MHC-II und kostimulatorische Moleküle für T-Zellen wie CD80 und CD86 hochreguliert werden. Im Lymphknoten wird dann eine klonale Expansion von naiven T-Helfer-Zellen mit der Bildung von Gedächtnis-T-Zellen, sowie eine Polarisierung in Th1-Richtung provoziert.
Die prädiktive Identifizierung von möglichen Kontaktallergenen kann einen Beitrag zur Primärprävention der allergischen Kontaktdermatitis leisten, indem solche Substanzen nicht mehr verwendet, durch ungefährlichere Stoffe ersetzt, oder – falls beides nicht möglich ist – persönliche Schutzmaßnahmen ergriffen werden. Seit vielen Jahrzehnten existieren für diesen Zweck ausschließlich auf Tierversuchen basierende Tests. Die beiden am häufigsten verwendeten sind der Guinea Pig Maximization Test (GPMT) [5] und der Local Lymph Node Assay (LLNA) in Mäusen [6].
Für die Entwicklung von tierversuchsfreien Tests sprechen ethische und praktische Argumente. In der Europäischen Union ist 2007 die Chemikalien- Verordnung „REACH“ (Registration, Evaluation, Authorisation and Restriction of Chemicals) in Kraft getreten. Sie legt unter anderem fest, dass bis zum 01.06.2018 für alle Substanzen, die in einer Menge von = 1 Tonne/Jahr in der EU hergestellt werden beziehungsweise in die EU importiert werden, eine toxikologische Risikobewertung vorliegen muss. Die Frage nach der Eigenschaft eines Stoffes als Kontaktallergen („Skin sensitization“) zählt hierbei zur Immuntoxikologie und muss zwingend für alle Substanzen beantwortet werden.
Für die genaue Anzahl dieser Substanzen gibt es bislang nur Schätzungen, sie reichen von etwa 30 000 bis 120 000 [7]. Nur für einen sehr kleinen Teil sind bereits Daten vorhanden. Zu bedenken ist, dass der LLNA, der von den regulatorischen Behörden als bevorzugter Test auserkoren wurde, mindestens 20 Mäuse zur Testung einer Substanz benötigt. Dies hat einen sehr hohen Bedarf an Versuchstieren zur Folge und stellt ein tierschutzethisches Problem dar. Da andere für REACH benötigte toxikologische Tests noch intensiver im „Verbrauch“ von Tieren sind, wurde die Entwicklung von tierversuchsfreien In-vitro-Tests vom Gesetzgeber begünstigt. Sobald diese Tests für eine Fragestellung ausreichend validiert sind, darf der entsprechende Tierversuch nicht mehr angewandt werden.
Für den Bereich der Kosmetika gilt in der EU ab dem 11.03.2013 ein generelles Verbot von Tierversuchen, sodass sich gerade für diesen Bereich interessante Perspektiven für In-vitro-Testverfahren auftun.
Neben ethischen oder rechtlichen Beschränkungen hat der Verzicht auf Tierversuche auch praktische Vorteile. So entfallen die hohen materiellen und personellen Aufwendungen für die artgerechte Haltung von Tieren und die umständlichen Genehmigungsverfahren. Im nachfolgend vorgestellten Testverfahren soll eine Simulation der Sensibilisierungsphase einer Kontaktallergie erfolgen. Die entscheidende Frage ist, ob die untersuchte Substanz in der Lage wäre, eine Immunreaktion auszulösen, die zur Bildung eines immunologischen Gedächtnisses führen könnte. Zu diesem Zweck wurde in der Zellkultur eine stark vereinfachte Simulation der menschlichen Epidermis geschaffen, welche zwei Arten von Zellen beinhaltet: die eigentlichen Epithelzellen („Keratinozyten“) und „Langerhans- Zell-ähnliche Zellen“ als Vertreter des Immunsystems.
2. Methoden
Nähere Einzelheiten zu den Verfahren und den verwendeten Materialien können der diesem Artikel zugrunde liegenden Dissertation und den zu dieser kumulativen Dissertation zugehörigen Artikeln entnommen werden: [8- 10].
2.1 Gewinnung von menschlichen Zellen
Es wurden menschliche Keratinozyten aus überschüssiger Haut von freiwilligen Spendern verwendet, die im Rahmen plastischer Operationen entfernt wurde. Fett und subkutanes Gewebe wurden vor der Weiterverarbeitung abpräpariert. Die Haut wurde in circa 5 mm dicke Streifen geschnitten und über Nacht im Kühlschrank bei 4 °C in einer Lösung mit 2 U/ml Dispase I in phosphatgepufferter Salzlösung (phosphate buffered saline, PBS; pH 7,4) inkubiert, um die Verbindung zwischen Dermis und Epidermis aufzutrennen. Am nächsten Morgen wurde die Epidermis abpräpariert und die Dermis verworfen. Die Epidermis wurde weiter in etwa 5 x 3 mm große Stücke zertrennt und für 30 min im Brutschrank bei 37 °C in einer 0,25 %igen Trypsin- und 0,01 %igen DNAse-Lösung in PBS inkubiert. Anschließend wurde durch Pipettieren eine Einzelzellsuspension gewonnen, die in einem Keratinozyten-selektiven Medium (keratinocyte growth medium-2, Promocell, Heidelberg) in Plastik-Zellkulturflaschen eingesät wurde. Nach Erreichen der Konfluenz wurden die Zellen abgelöst und für die spätere Verwendung in flüssigem Stickstoff eingefroren.
Da die Isolierung von Langerhans-Zellen aus menschlicher Haut sehr aufwendig ist und Langerhans- Zellen in Kultur rasch absterben, wurden hier ersatzweise Monozyten benutzt. Letztere wurden durch Zytokine zu „Langerhans- Zell-ähnlichen Zellen“ differenziert [11]. Dazu wurden Monozyten aus der Leukozytenmanschette („buffy coat“) zentrifugierter Blutspenden gewonnen. Der buffy coat wurde über einen Dichtegradienten zentrifugiert, welcher aufgrund seiner physikalischen Eigenschaften die „mononukleären Zellen“ des peripheren Blutes (hauptsächlich Lymphozyten und Monozyten) zurückhält. Nach Zugabe von mit Eisen-Nanopartikeln markierten Antikörpern gegen das Monozyten-Antigen CD14 wurden die Monozyten durch einen Magneten isoliert und in flüssigem Stickstoff kryokonserviert.
2.2 Kokultur von Keratinozyten und „Langerhans- Zell-ähnlichen Zellen“
Die Keratinozyten wurden in 12-Loch-Zellkulturplatten ausgesät. Nach Erreichen der halben Konfluenz, üblicherweise nach zwei Tagen, erfolgte die Zugabe von Monozyten direkt auf den Keratinozytenrasen.
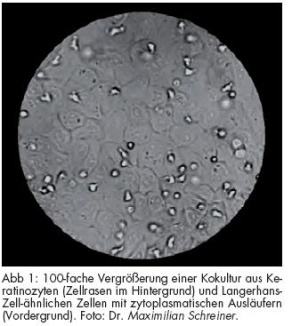
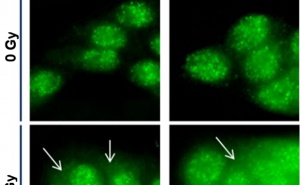
Die so entstandenen Kokulturen wurden mit einem Cocktail aus Granulozyten-/Makrophagen- Kolonie-stimulierenden Faktor (GM-CSF), Interleukin-4 (IL-4) und transformierendem Wachstumsfaktor-b1 (TGF-b1) behandelt. Innerhalb von zwei Tagen entwickelten sich die Monozyten zu Langerhans- Zell-ähnlichen Zellen. Dies ist morphologisch an der Ausbildung von zytoplasmatischen Ausläufern ähnlich den Langerhans- Zellen in vivo zu erkennen (Abb 1). Molekularbiologisch kommt es analog zu einer Veränderung des Profils der Oberflächenantigene. Zu diesen Kokulturen wurden Allergene, Positiv- uxnd Negativkontrollen hinzugegeben. Für nicht wasserlösliche Substanzen wurden Dimethylsulfoxid oder Ethanol als Vehikel benutzt. In diesen Fällen waren auch die Vehikel alleine als Kontrollen zu messen.
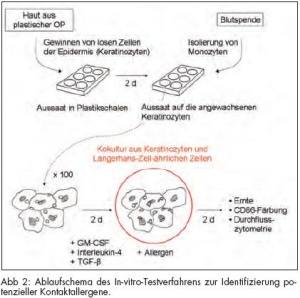
Nach 48 Stunden wurden die Langerhans- Zell-ähnlichen Zellen geerntet, indem sie von den fest auf dem Plastikboden der Zellkulturschale haftenden Keratinozyten heruntergespült wurden. Das Oberflächenantigen CD86 diente in diesem Test als Gradmesser für die Aktivierung der Langerhans-Zell-ähnlichen Zellen und somit als Surrogatparameter für die Fähigkeit einer Substanz, eine Sensibilisierung hervorzurufen. Die Zellen wurden dazu mit fluoreszierenden anti-CD86-Antikörpern gefärbt und anschließend in einem Durchflusszytometer (FACS Calibur, BD, Heidelberg) gemessen. Der Quotient aus der mittleren Fluoreszenzintensität (MFI) behandelter Zellen und der MFI der korrespondierenden Negativ- beziehungsweise Vehikelkontrolle wurde gebildet, was dem relativen Anstieg von CD86 entspricht. Die Methode ist schematisch in Abbildung 2 zusammengefasst
3. Ergebnisse
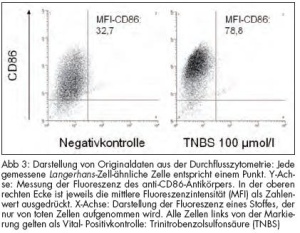
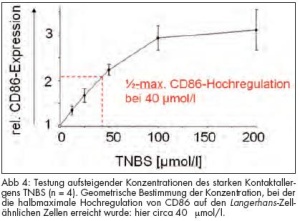
Abbildung 3 zeigt Originaldaten von Lan gerhans-Zell-ähnlichen Zellen. Die Stärke der Fluoreszenz des anti-CD86- Anti körpers wurde als Zahlenwert ausgedrückt (MFI). Der relative Anstieg der CD86-Expression nach Zugabe des starken Kontaktallergens Trinitrobenzolsulfonsäure (TNBS) in einer Konzentration von 100 mmol/l betrug hier 78,8 / 32,7 = 2,41. Es wurden unterschiedliche Konzentrationen von TNBS getestet, womit eine lineare Dosis-Wirkungs- Beziehung bis zum Erreichen eines Plateaus demonstriert werden konnte (Abb 4). Um verschiedene Allergene miteinander vergleichen zu können, wurde – wie in Abbildung 4 demonstriert – die Konzentration bestimmt, bei welcher die halbmaximale Hochregulation von CD86 erfolgt ist. Je niedriger dieser Wert, desto stärker wird das Allergen eingeschätzt, da bereits bei kleinen Konzentrationen eine signifikante Hochregulation von CD86 hervorgerufen wird.
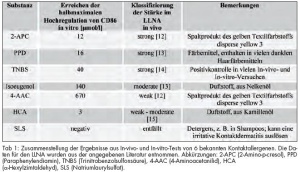
In Tabelle 1 werden die Ergebnisse von 6 getesteten bekannten Kontaktallergenen zusammengefasst, welche alle eine positive Reaktion unterschiedlicher Stärke auslösten. Vergleichend wurde aus der Literatur die im Tierversuch (LLNA) ermittelte Stärke des Allergens hinzugefügt. Zusätzlich wurde die Substanz Natriumlaurylsulfat (Sodium Lauryl Sulfate, SLS) getestet, welche das der allergischen Kontaktdermatitis ähnliche Krankheitsbild der irritativen Kontaktdermatitis auslöst. Im Gegensatz zur allergischen Kontaktdermatitis wird hierbei jedoch kein immunologisches Gedächtnis gebildet. Erwartungsgemäß konnte SLS in diesem Test keine Hochregulation von CD86 verursachen. Die vorausgesagte relative Stärke der Kontaktallergene (anhand der halbmaximalen Hochregulation von CD86) korreliert mit den Daten des Tierversuchs, mit Ausnahme von α-Hexylzimtaldehyd (HCA). Während HCA im Tierversuch nur als schwach bis mäßig starkes Allergen klassifiziert wurde, rief es im hier dargestellten In-vitro-Test die stärkste aller gemessenen Reaktionen hervor.
4. Diskussion und Schlussfolgerungen
Die erste Evaluation des In-vitro-Test verfahrens zur Identifizierung potenzieller Kontaktallergene war vielversprechend. Alle sechs getesteten Kontaktallergene wurden korrekt durch die Bestimmung der Hochregulation von CD86 erkannt. Wie in der Einführung beschrieben, ist der Verzicht auf Tierversuche ethisch wünschenswert und in manchen Bereichen sogar gesetzlich vorgeschrieben. Die für diesen In-vitro-Test benötigten menschlichen Zellen können vergleichsweise einfach und für Spender wenig belastend gewonnen werden: zum einen als Abfallmaterial von Operationen (Epidermis), zum anderen aus leicht zugänglichem Gewebe (Blut). Nach Gewinnung können die Zellen eingefroren werden und sind somit flexibel zu einem anderen Zeitpunkt oder an einem anderen Ort einsetzbar.
Da die Identität der Hautspender aus Datenschutzgründen nicht bekannt war, waren die Spender von Keratinozyten und Monozyten folglich nicht identisch. Da in dem Zellkultursystem jedoch keine Zellen des adaptiven Immunsystems, wie T-Zellen, enthalten sind, waren keine unspezifischen Reaktionen zu erwarten. Wie die Ergebnisse gezeigt haben, war bei den Negativkontrollen die Expression von CD86 auch durchweg so niedrig, dass nach Zugabe von Kontaktallergenen eine signifikante Hochregulation von CD86 gemessen werden konnte.
Der Vergleich mit den Ergebnissen des LLNA in Mäusen zeigt eine gute Korrelation der in vitro und in vivo gewonnenen Resultate. Die einzige Ausnahme war der Duftstoff HCA: im Tierversuch LLNA wurde er als schwaches bis mäßiges Kontaktallergen klassifiziert, im In-vitro- Test rief er jedoch die stärkste Reaktion aller getesteten Allergene hervor. Eine mögliche Erklärung könnte die unterschiedlich gute Penetration von Allergenen durch die Haut sein. In diesem In-vitro- Test ist, anders als im Tierversuch, keine Penetration durch die Haut notwendig. Die Stoffe können ohne vorgeschaltete Barriere mit den Zellen interagieren. Möglicherweise ist eine schlechte Hautpenetration von HCA die Erklärung für die schwache Reaktion im Tierversuch. Hier sind weitere Untersuchungen notwendig.
Das paradoxe Ergebnis für HCA offenbart eine potentielle Schwachstelle dieses In-vitro-Tests: der Prozess der Penetration eines Allergens durch die obersten Hautschichten ist im Gegensatz zum Tierversuch nicht Teil dieses Testsystems. Um zu einer realistischen Abschätzung des Gefahrenpotenzials eines Kontaktallergens zu kommen, müssten zusätzliche Daten zur Hautpenetration gewonnen werden. Da dreidimensionale In-vitro- Modelle der menschlichen Haut bereits kommerziell erhältlich sind, könnte prinzipiell auch hier auf Tierversuche verzichtet werden.
Realistischerweise muss man davon ausgehen, dass nicht ein In-vitro-Testverfahren alleine den LLNA als Tierversuch ersetzen kann. Wahrscheinlich wird erst die Zusammenschau der Ergebnisse mehrerer In-vitro-Tests, welche verschiedene Stufen der Sensibilisierungsphase wie Hautpenetration und Aktivierung von Langerhans-Zellen nachbilden, eine realistische Einschätzung des Risikopotenzials einer allergenen Substanz ermöglichen.
Die Notwendigkeit für eine solche Risikoabschätzung ergibt sich aus der hohen Prävalenz der allergischen Kontaktdermatitis in der allgemeinen Bevölkerung und aus den zahlreichen gemeldeten Verdachtsfällen einer berufsbedingten Ursache für dieses Krankheitsbild. Insbesondere Soldaten sind eine besondere berufliche Risikogruppe für die allergische Kontaktdermatitis. Wie eine Studie der israelischen Streitkräfte beschreibt, sind häufige Quellen Öle, Fette, Treibstoffe und ihre Additive. Es wurden jedoch auch Kontaktallergien gegen Textilfarbstoffe und Imprägnierungen von Uniformen gefunden [16]. Um krankheitsbedingte Ausfälle oder gar Dienstunfähigkeit zu vermeiden, sollten die allergenen Eigenschaften von Chemikalien, die in Betriebsstoffen, Uniformen und Ausrüstungsgegenständen der Bundeswehr verwendet werden, bekannt und getestet sein.
Literatur:
- Thyssen JP, Linneberg A, Menné T, Johansen JD: The epidemiology of contact allergy in the general population-prevalence and main findings. Contact Dermatitis 2007; 57: 287-299.
- Bundesministerium für Arbeit und Soziales (Hrsg.): Sicherheit und Gesundheit bei der Arbeit 2008. Dortmund/Berlin/Dresden 2010: 93.
- European Agency for Safety and Health at Work (Hrsg.): Occupational skin diseases and dermal exposure in the European Union (EU-25): policy and practice overview. Luxemburg 2008: 20.
- Cavani A, De Luca A: Allergic contact dermatitis: novel mechanisms and therapeutic perspectives. Curr Drug Metab 2010; 11(3): 228-233.
- Magnusson B, Kligman AM: The identification of contact allergens by animal assay. The guinea pig maximization test. J Invest Dermatol 1969; 52(3): 268-276.
- Kimber I, Weisenberger C: A murine local lymph node assay for the identification of contact allergens. Assay development and results of an initial validation study. Arch Toxicol 1989; 63(4): 274-282.
- Rovida C, Hartung T: Re-evaluation of animal numbers and costs for in vivo tests to accomplish REACH legislation requirements for chemicals - a report by the transatlantic think tank for toxicology (t4). ALTEX 2009; 26(3): 187-208.
- Schreiner M: Evaluation und Weiterentwicklung eines in vitro Testverfahrens zur Bestimmung des sensibilisierenden Potenzials von Kontaktallergenen. Dissertation. Berlin 2010. Online: www.diss.fu-berlin.de/diss/receive/FUDISS_thesis_000000016939
- Schreiner M, Peiser M, Briechle D, Stahlmann R, Zuberbier T, Wanner R: A new dendritic cell type suitable as sentinel of contact allergens. Toxicology 2008; 249(2-3): 146-152.
- Schreiner M, Peiser M, Briechle D, Stahlmann R, Zuberbier T, Wanner R: A loose-fit coculture of activated keratinocytes and dendritic cell-related cells for prediction of sensitizing potential. Allergy 2007; 62(12): 1419-1428.
- Geissmann F, Prost C, Monnet JP, Dy M, Brousse N, Hermine O: Transforming growth factor beta1, in the presence of granulocyte/macrophage colony-stimulating factor and interleukin 4, induces differentiation of human peripheral blood monocytes into dendritic Langerhans cells. J Exp Med 1998; 187: 961-966.
- Stahlmann R, Wegner M, Riecke K, Kruse M, Platzek T: Sensitising potential of four textile dyes and some of their metabolites in a modified local lymph node assay. Toxicology 2006; 219(1-3): 113-123
- Basketter DA, Gerberick F, Kimber I: The local lymph node assay and the assessment of relative potency: status of validation. Contact Dermatitis 2007; 57(2): 70-75.
- Smith CK, Hotchkiss SAM: Allergic Contact Dermatitis––Chemical and Metabolic Mechanisms. London and New York: Taylor & Francis 2001.
- Gerberick GF, Ryan CA, Dearman RJ, Kimber I: Local lymph node assay (LLNA) for detection of sensitization capacity of chemicals. Methods 2007; 41(1): 54-60. 16. Wolf R, Orion E, Matz H: Contact dermatitis in military personnel. Clin Dermatol 2002; 20(4): 439-444.
Datum: 24.06.2011
Quelle: Wehrmedizinische Monatsschrift 2011/4