DER EINFLUSS VON KOMORBIDITÄTEN UND ÄTIOLOGIEN AUF DEN ERFOLG DER EXTRAKORPORALEN SCHOCKWELLENTHERAPIE BEI CHRONISCHEN WEICHTEILVERLETZUNGEN: ERGEBNISSE NACH MITTELLANGER LAUFZEIT*
The Influence of Co-morbidities and Etiologies on the Success of extracorporeal Shock Wave Therapy for chronic Soft Tissue Wounds:midterm Results*
Aus dem Heeresspital - Wien (Kommandant: Oberstarzt Prim. Dr. G. Mooseder)¹ am Militärmedizinischen Zentrum (Kommandant: Brigadier MR Dr. E. Gallent), der Abteilung für Radiologie (Leiter: o. Univ. Prof. Dr. C. Herold)², der Abteilung für Gefäßchirurgie (Leiter: o. Univ. Prof. Dr. P. Polterauer)³, dem Zentrum für Anatomie und Zellbiologie (Leiter: o. Univ. Prof. Dr. M. Pavelka)⁴ an der Medizinischen Universität Wien (Rektor: Univ. Prof. Dr. W. Schütz), der Abteilung für Chirurgie (Leiter: Univ. Prof. Dr. M. S. Gnatyuk)⁵ an der Medizinischen Staatsuniversität TERNOPIL (Rektor: Univ. Prof. L. Y. Kovalchuk) und aus dem Unfallkrankenhaus Meidling (Leiter: Univ. Prof. Dr. C. Fialka)⁶
Klaus S. Wolff¹, Andreas G. Wibmer², Michael Pusch⁶, Alexander M. Prusa³,
Michael Pretterklieber⁴, Harald Teufelsbauer³,⁵ und Wolfgang Schaden⁶
* Original in englischer Sprache erschienen in: Ultrasound in Med & Biol 2011; 37 (7): 1111–1119, mit freundlicher Genehmigung des Elsevier Verlages.
Hintergrund: Mögliche Einflüsse von Komorbiditäten und verschiedenen Wundätiologien auf den Erfolg der Therapie mit extrakorporalen Schockwellen (ESWT) bei chronischen Weichteilwunden wurden untersucht.
Methoden: Von September 2003 bis Februar 2007 wurden 282 Patienten, die vorher mehr als einen Monat lang vergeblich behandelt worden waren, in die Studie aufgenommen. Die Behandlung bestand aus der ESWT, die zu bestimmten Intervallen erfolgte. Bei jeder Behandlungssitzung wurde eine Wundbettbewertung (wound bed score, WBS) durchgeführt, ebenso wurden bei der Erstpräsentation eine ausführliche Anamnese und Angaben über die Wundätiologie erhoben. Die erhobenen Komorbiditäten wurden nach den Kapiteln des ICD-10 Systems gepoolt.
Ergebnisse: 258 Patienten (91,49 %) wurden analysiert und für einen Median von 31,8 Monaten weiterverfolgt. Wundverschluss erfolgte bei 191 Patienten (74,03 %) nach median zwei Behandlungssitzungen. Keine Wunde trat an derselben Stelle wieder auf. Ein multivariates logistisches Regressionsmodell zeigte überraschenderweise, dass die gepoolten Komorbiditäten und die Wundätiologie keinen statistisch signifikanten Einfluss auf den Erfolg der ESWT hatte.
Schlussfolgerungen: Komorbiditäten und die Wundätiologie haben keinen signifikanten Einfluss auf den Erfolg von ESWT. Lediglich die lokalen Wundeigenschaften – wie durch den WBS repräsentiert – sind relevant, wenn es sich um den Heilungserfolg handelt.
Summary
Background: Possible effects of co-morbidities and of different wound etiologies on the success of extracorporeal shock wave therapy (ESWT) of chronic soft tissue wounds were investigated.
Methods: From September 2003 until February 2007, 282 patients, being previously treated unsuccessfully were enrolled. Treatment consisted of ESWT occurring at defined intervals. At each treatment session a wound bed score was recorded, also at initial presentation a detailed patient history and wound etiology. Observed co-morbidities were pooled according to the chapters of the ICD-10 system.
Results: 258 patients (91.49 %) were analyzed and underwent follow-up for a median of 31.8 months. Wound closure occurred in 191 patients (74.03 %) by a median of two treatment sessions. No wound reappeared at the same location. A multivariate logistic regression model showed that pooled co-morbidities and wound etiologies did not have a significant influence on success.
Conclusions: Co-morbidities and wound etiologies have surprisingly no significant influence on the success of ESWT. Only local wound properties – as represented by the wound bed score – matter, when successful wound healing is concerned.
1. Einleitung
Chronische Weichteilwunden stellen sowohl für Patienten als auch für Ärzte ein großes Problem dar und werden in fast allen medizinischen Spezialgebieten von der Dermatologie (1), über die Innere Medizin (2), die Chirurgie (3), die Gefäßchirurgie (4) und die Unfallchirurgie (5) bis hin zur Kriegschirurgie (6) angetroffen.
Das Hauptziel in der Behandlung chronischer Weichteilwunden ist es, einen Wundverschluss zu erzielen. Üblicherweise wird das nekrotische Gewebe débridiert, um das volle Ausmaß des Gewebeschadens beurteilen zu können, tiefer liegende Abszesse oder andere Pathologien, die für die verzögerte Wundheilung verantwortlich sind, zu identifizieren. Feuchte Verbände (wet-to-wet dressings) werden hauptsächlich verwendet, um einen Heilungsprozess anzustoßen. Als zweite Behandlungsoption, um einen Wundverschluss zu erzielen, werden Spezialverbände wie semipermeable Filme, Hydrogele, Hydrokolloide oder Kalziumalginate aufgebracht. Diese Verbände werden mit langandauernder konservativer Therapie und der Entwicklung von allergischen Reaktionen bei längerer Anwendung assoziiert (7). Eine weitere Behandlungsoption ist der Einsatz eines Vakuum assistierten Wundverschlusses oder der Spalthaut beziehungsweise von Schwenklappen nach dem Scheitern des nicht-operativen Behandlungsansatzes. Unglücklicherweise scheitern bei einer limitierten Anzahl von Patienten alle drei Behandlungsregime.
Die Anwendung extrakorporaler Schockwellen für klinische Zwecke wurde vor mehr als zwei Jahrzehnten vorgestellt (8). Die extrakorporale Schockwellentherapie (ESWT) wird heutzutage in den Sonderfächern Urologie, Orthopädie (9) und Unfallchirurgie (10) angewandt. Extrakorporale Schockwellen werden mit der Induktion der Neovaskularisation und mechanischen Stimulation, die die Proliferation einer großen Anzahl von Zellen – inklusive der Osteoblasten (11) – bewirkt, in Verbindung gebracht. Die biologischen Effekte der extrakorporalen Schockwellen auf menschliche Zellen werden gegenwärtig an mehreren Zentren weltweit erforscht (11, 12, 13). Pioniere in der Ultraschallforschung, die sowohl die Möglichkeiten des Ultraschalls als auch dessen Bioeffekte über die letzten Jahrzehnte beschrieben waren Dunn und andere (14, 15, 16, 17, 18, 19).
Die Erfahrung unserer Forschungsgruppe mit der ESWT in der Unfallchirurgie und die unerwartete Beobachtung, dass nicht nur das unfallchirurgische Problem – die Nichtheilung der Bruchstelle (20) – sondern auch das umliegende Weichgewebe einen positiven Heilungsverlauf nach ESWT zeigten, veranlasste uns, verstärkt die Effekte der ESWT auf die Weichteilwunden zu untersuchen. Erste Resultate, die einen signifikanten Einfluss des Alters, der Wundgröße/-oberfläche und des Andauerns der chronischen Wunde als positive Prädiktoren einer kompletten Wundheilung postulierten, wurden bereits früher veröffentlicht (21). In der gegenständlichen retrospektiven Studie identifizierten wir die bestehenden Komorbiditäten und die Ätiologie der chronischen Weichteilwunde eines jeden Patienten, der mit ESWT behandelt wurde, und beobachteten über die Zeit, ob diese Faktoren einen Einfluss auf das Ergebnis der Wundheilung der chronischen Weichteilwunde hatten.
2. Methoden
2.1 Patientenkollektiv
Von September 2003 bis Februar 2007 wurden 282 Patienten beiderlei Geschlechts und älter als 18 Jahre in diese retrospektive Analyse unserer ESWT-Studie aufgenommen (Clinical Trials.gov number, NCT00545896), wenn sie zum Zeitpunkt der Erstvorstellung an einer chronischen Weichteilwunde litten, die zumindest länger als 30 Tage bestand. Während dieser mindestens 30 Tage vor der Erstpräsentation mussten etablierte Behandlungskonzepte wie vornehmlich chirurgisches Débridement und feuchte Verbände, Hydrokolloide, Kalziumalginate oder Vakuum -assistierter Wundverschluss am Behandlungswerber vergeblich eingesetzt worden sein. Alle möglichen Ursachen als Auslöser der chronischen Weichteilwunden wurden in die Studie eingeschlossen außer die eine Zirkumferenz-umfassenden Verbrennungen zweiten oder höheren Grades an den oberen und unteren Extremitäten.
2.2 Studiendesign
Das Studiendesign war eine Einzelgruppenuntersuchung, einarmig, offen und prospektiv, um den Effekt der ESWT auf chronische Wunden zu untersuchen. Definierte primäre Endpunkte waren die Gesamtletalität (30 Tage Sterblichkeit nach der letzten ESWT- Sitzung). Ursprünglich definierte sekundäre Beobachtungen waren die komplette Wundverschlussrate und die Anzahl der hierzu benötigten ESWT- Sitzungen, die Rate der nicht heilenden Wunden und die Anzahl der ESWT- Sitzungen bis zum erfolglosen Ausscheiden. Der Einfluss der Komorbiditäten des Patienten und der Ätiologie der chronischen Wunde auf den Behandlungserfolg wurde retrospektiv analysiert.
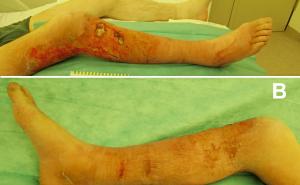
Der Zustand jeder chronischen Weichteilwunde wurde durch eine Wundbettbewertung (wound bed score, WBS) bei jeder Sitzung und am Ende der Behandlung beurteilt. Jedes Mal erfolgte eine Fotodokumentation der Wunde. Die ESWT wurde wöchentlich abgehalten. Nach der zweiten ESWT-Sitzung wurden das Behandlungsintervall üblicherweise auf zwei Wochen ausgedehnt. Wenn nach 10 Sitzungen, das heißt, nach zirka 105 bis 120 Tagen kein Fortschritt beobachtet werden konnte, wurde die ESWT abgebrochen. Die Behandlungen wurden ambulant im Traumazentrum durchgeführt. Vor der erstmaligen Anwendung der extrakorporalen Schockwelle wurde die Wunde gründlich débridiert. Während und unmittelbar nach jeder Behandlung wurden die Patienten auf Nebenwirkungen der Therapie überprüft. Beginnend mit der letzten ESWT-Sitzung wurden die Patienten für mindestens ein Jahr nachgesorgt, um die mittelfristigen Heilungseigenschaften der ESWT beurteilen zu können. Die ESWT- Nachsorge erfolgte durch Telefoninterviews der Forschungsgruppenmitglieder mit dem Patienten oder mit Personen aus dessen Haushalt ( 24-Stunden-Pflege, Partner, Kinder).
Diese Studie wurde von den Mitgliedern der Forschungsgruppe initiiert. Die Daten wurden durch die Forschungsgruppe kompiliert, analysiert und verifiziert. Das Manuskript wurde in allen Stadien nur durch die Autoren/Forschungsgruppe geschrieben und überwacht. Die Anbieter/Hersteller des extrakorporalen Schockwellengeräts orthowave 180 C TM (Tissue Regeneration Technologies – TRT, Atlanta, Georgia, USA) hatten keinen Einfluss auf das Forschungsprojekt, keinen Zugang zu den erhobenen Daten, und zu keinem Zeitpunkt die Möglichkeit, das Manuskript vor der Einreichung einzusehen. Patienteneinwilligungserklärungen wurden von allen Patienten eingeholt. Das Projekt wurde vom AUVA Institutional Review Board des AUVA Unfallkrankenhauses Meidling genehmigt.
2.3 extrakorporale Schockwellentechnologie
Ein spezieller Ultraschallgenerator orthowave 180 C TM der nicht fokusierte planare Schockwellen emittiert, wurde in diesem Forschungsprojekt verwendet (21). Nach sorgfältigem Débridement der chronischen Weichteilwunde wurde die Wunde mit sterilem Ultraschallgel aufgefüllt und darüber eine chirurgische Abdeckfolie platziert, um Luftblasen zu vermeiden und bessere Übertragungsbedingungen zu schaffen. Nach Kalibrierung des orthowave 180 C TM und Einstellung des Energiebereichs auf 0.1 mJ/mm2 und der Frequenz auf 5 Impulse/Sekunde wurde der parabolische Reflektor (= Schallkopf) auf die abgedeckte Wunde gesetzt. Abhängig von der Wundgröße wurde eine mediane Anzahl von 167 Impulsen/cm2 Wundoberfläche (Interquartilabstand Q1 – Q3: 100 – 300; Bereich 2,7 –
2 400) appliziert. Die Wundversorgung und Verbandstrategie vor einer ESWT blieben unverändert und wurden nach jeder ESWT-Sitzung fortgeführt.
2.4 Wundbettbewertung (wound bed score)
Um eine einheitliche und reproduzierbare Bewertung der chronischen Weichteilwunden zu erreichen, nutzten wir die Wundbettbewertung (wound bed score, WBS) von Falanga (22). Der Vorteil dieses Bewertungssystems war, dass der WBS auch in sich selbst einen prädiktiven Wert bezüglich des Wundheilungserfolges darstellen sollte. Dieses Wundbettbewertungssystem berücksichtigt die folgenden klinischen Parameter:
- heilende Ränder,
- Gegenwart von Nekrose,
- größte Wundtiefe/Präsenz von Granulationsgewebe,
- Exsudatmenge und Ödem,
- Periwunddermatitis,
- Periwundkallus/-fibrose und
- rosa/rotes Wundbett.
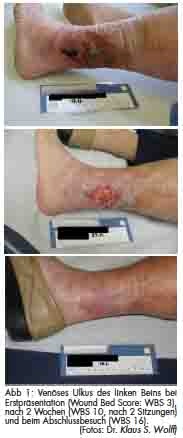
Alle Einzelparameter werden zwischen 0 und 2 bewertet und dann addiert. Jede chronische Wunde kann daher im WBS einen Wert von 16 (bestmögliche Bewertung) bis 0 (schlechtestmögliche Bewertung) erzielen. Die chronische Wunde wurde vor jedem ESWT-Sitzungsbeginn mit dem WBS beurteilt (Abb 1).
2.5 Komorbititäten und Wundätiologie
Bei der allerersten Beurteilungssitzung zur Abklärung der Studienteilnahme wurde die Anamnese eines jeden Patienten dokumentiert und die mögliche Ursache für die chronische Weichteilwunde erhoben. Erwartungsgemäß präsentierte sich eine beachtliche Zahl von Patienten mit einer oder mehreren Komorbiditäten. Die multifaktorielle Komponente chronischer Weichteilwunden, die Schwierigkeit den Schweregrad der jeweiligen Komorbidität objektiv zu gewichten, zum Beispiel Krebs mit Chemotherapie versus obstruktive Herzerkrankung, und die Vielzahl an verschiedenen Pathologien – dokumentiert mit dem ICD-10 Code – zwangen uns, die Komorbiditäten nach den 21 Kapiteln des ICD-10-Systems zusammenzufassen, um eine statistische Analyse zu ermöglichen.
Die chronischen Wunden wurden gemäß ihrer Ätiologie in sieben Subgruppen eingeteilt
- postoperative Wunden (teilweise oder komplette Wundheilungsstörung nach primärem chirurgischem Wundverschluss),
- posttraumatische Wunden (chronische Weichteilwunden als Resultat eines direkten penetrierenden oder stumpfen Traumas mit damit verbundener Nekrose epithelialer und nicht -epithelialer extraskeletärer Strukturen),
- venöse Ulzera,
- Dekubitalulzera, Gipsdruckstellen,
- arterielle Insuffizienzulzera,
- Verbrennungswunden (nicht die Zirkumferenz umfassende tiefe Verbrennungen 2. und/oder 3. Grades).
Patienten, die sich mit diesen Verbrennungswunden präsentierten, wurden trotz der 30-Tage-Regel wegen der Chronizität ihrer Wunden in die Studie aufgenommen.
2.6 Überwachung unerwünschter Nebenwirkungen und Nachsorge
Sporadische Berichte assoziierten Ultraschallwellen mit möglichen Blutungen nach Nierensteinbehandlungen (23, 24) und generell mit mikrovaskulären Schäden (25). Als eine Konsequenz dessen wurden die ESWT-Patienten nach jeder ambulanten Sitzung für 60 Minuten unter genauer Überwachung weiter beobachtet. Manche Patienten klagten über Schmerzen während der Behandlung; letztere wurden durch eine sofortige Reduktion der Frequenz berücksichtigt, aber nicht festgehalten. Nach jeder ESWT-Sitzung wurden die Patienten befragt, ob sie eine Schwellung, Schmerzen, „schwere Beine” oder Kurzatmigkeit verspürten. Falls sie dies bestätigten, wurde das Ereignis festgehalten und die entsprechenden diagnostischen und kurativen Maßnahmen eingeleitet. Im Zuge der Nachsorge wurden die Patienten telefonisch gezielt nach Blutungen, Thrombosen oder Lungenembolien befragt.
2.7 Statistische Analyse
Für die Datenanalyse wurde die SAS Software, Version 9.1 (SAS Institute Inc., Cary, North Carolina, USA) verwendet. Das Cut-off-Datum für die Datenbeschaffung in diesem laufenden Forschungsprojekt war der 27. Februar 2007, um eine theoretische Nachsorgeperiode von mindestens einem Jahr zu gewährleisten. Patienten, die zu den vereinbarten ESWT-Sitzungen nicht erschienen oder die Kooperation während der Nachsorgeperiode verweigerten, wurden aus der Studie ausgeschlossen. Ein multivariates logistisches Regressionsmodell wurde angewandt, um mögliche positive oder negative Faktoren mit Einfluss auf den Erfolg der ESWT beim Wundverschluss zu identifizieren. Der Signifikanzwert, um in das logistische Regressionsmodell einzutreten oder im Modell zu verbleiben, betrug p < 0,01. Erfolg wurde definiert als vollständiger Wundverschluss oder zumindest ein abschließender WBS von 14 oder höher. Die Gesamtletalität und auf ESWT bezogene Todesfälle innerhalb von 30 Tagen nach der letzten ESWT-Sitzung wurden analysiert. Alle p-Werte waren zweiseitig, Odd-ratios wurden kalkuliert. P-Werte von < 0,01 wurden als statistisch relevant gewertet.
3. Ergebnisse
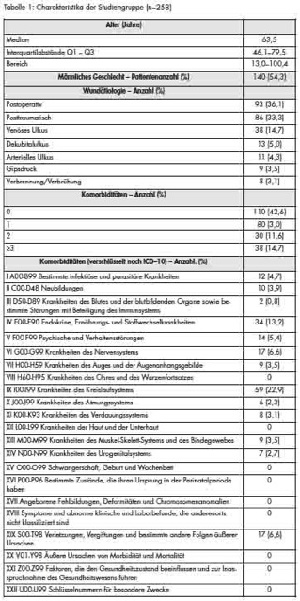
Vierundzwanzig (8,51 %) von 282 rekrutierten Patienten gingen im Zuge der Nachsorge verloren. Die verbleibenden 258 Patienten wurden analysiert. Das mediane Alter bei der Erstvorstellung war 63,5 Jahre (Interquartilabstand Q1 - Q3: 46,1 – 79,5 Jahre), die mediane Nachsorgezeit betrug 31,8 Monate (Interquartilabstand Q1 – Q3: 24,0 – 38,0 Monate). Kein Patient verstarb innerhalb von 30 Tagen nach ESWT an möglichen mit der Behandlung assoziierten Nebenwirkungen (hämorrhagischer Schock, Lungenembolie, ischämischer Hirninfarkt). Hingegen wurden sieben nicht anlassbezogene Todesfälle (2,71 %) registriert. Weitere Analysen der Grunddaten werden in Tabelle 1 präsentiert.
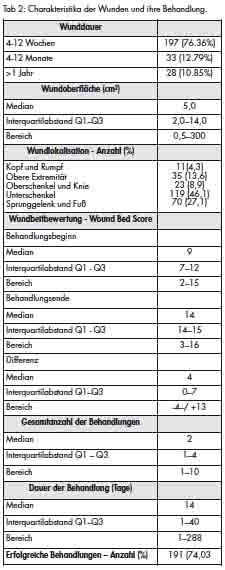
Eine Übersicht der Wundcharakteristiken und der Behandlungsdetails findet sich in Tabelle 2.
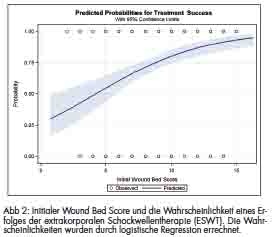
Eine erfolgreiche Behandlung konnte in 191 Patienten (74,03%) mit einer medianen Behandlungsserie von zwei ESWT Sitzungen erzielt werden. Ein multivariates logistisches Regressionsmodell, das die Einflüsse der Komorbiditäten, der Wundätiologie, des initialen WBS, des Geschlechts und der bereits identifizierten Faktoren Alter, Dauer der chronischen Wunde und Wundgröße analysierte, wurde eingesetzt. Tabelle 3 bietet sowohl einen Überblick über die drei statistisch relevanten Parameter in diesem Modell wie initialer WBS (p < 0,001), Wunddauer (p < 0,001) und Wundoberfläche in cm2 (p < 0,001), als auch Informationen bezüglich der Wundätiologie und der Komorbiditäten. Chronische Wunden, die vor der Erstpräsentation zur ESWT 4 bis 12 Wochen dauerten, zeigten eine Erfolgsrate von 82,23 %. Monatelang dauernde Wunden (4 – 12 Monate) hatten eine Erfolgsrate von 63,64 % und jahrelang dauernde Wunden (> 1 Jahr) eine Rate von 28,57 %. Abbildung 2 zeigt den prädiktiven Wert des initialen WBS zum Zeitpunkt der Erstpräsentation des Patienten.
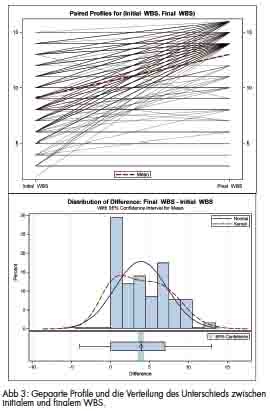
Ein medianer positiver Unterschied zwischen dem initialen und finalen WBS von +4 wurde beobachtet (Interquartilabstand Q1: 0, Q3: +7, Bereich
-4 bis +13). Gepaarte Profile sowohl für den initialen und finalen WBS als auch die Verteilung des Unterschieds zwischen initialem und finalem WBS werden in Abbildung 3 veranschaulicht.
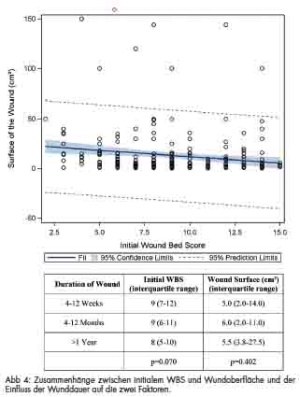
Ein signifikanter Zusammenhang (p < 0,0051) bestand zwischen dem initialen WBS und der Wundoberfläche. Je größer die Wundoberfläche war, desto höher war der initiale WBS (Abb 4). Abbildung 4 informiert ferner über das Verhältnis sowohl zwischen dem initialen WBS und der Wunddauer als auch zwischen der Wundoberfläche und Wunddauer. Hier konnte keine statistische Signifikanz entdeckt werden.
4. Diskussion
Chronische Weichteilwunden sind für den behandelnden Arzt in vielen medizinischen Sonderfächern eine Herausforderung. Sie entspringen einer großen Gemengelage, wobei die ambulante Behandlung, die Behandlungskosten und -dauer sowie die Patienten-/Pflegemitarbeit bei der extramuralen Wundversorgung die drei Hauptprobleme bilden.
Das Problem der ambulanten/extramuralen Behandlung kann nicht durch den involvierten Arzt allein gelöst werden, vielmehr resultiert es als Produkt aus der Chronizität der Wunde und aus den einschränkenden, externen Entscheidungsfaktoren wie der Reduktion der Spitalsbetten, dem Tagessatz der Liegegebühren und dem Leistungsumfang der jeweiligen Krankenkasse. All dies führt zur frühen Entlassung nach versuchter primärer Behandlung. Schlussendlich richtet sich daher das Hauptaugenmerk in der Behandlung chronischer Weichteildefekte darauf die Kosten und Behandlungsdauer zu senken und die Behandlungsregime im extramuralen/ambulanten Bereich zu vereinfachen.
Vor allem durch die letztgenannte Maßnahme und die damit einhergehende bessere Patientenmitarbeit werden die Kosten wieder eingedämmt. In den letzten zwei Jahrzehnten entwickelte Methoden waren der Vakuum assistierte Wundverschluss (26), topische Anwendung von aus rekombinanten humanen Thrombozyten gewonnenem Wachstumsfaktor BB (27) und die Verwendung einer nicht zellulären Matrix als Hautersatz (28). Alle diese Methoden zeigten eine signifikante Verkleinerung der Wundgröße und eine Beschleunigung des Heilverhaltens, aber es fehlte immer noch die komplette Epithelialisierung.
Ein anderer Ansatz zur Behandlung chronischer Weichteilwunden, der in den letzten zehn Jahren vorgestellt wurde, war die hyperbare Sauerstofftherapie. Sie ergab im Verhältnis zu konventionellen Behandlungsmethoden signifikant bessere Heilungserfolge, wurde aber nur bei speziell definierten Patientenkollektiven angewandt und ihre Erfolge waren nicht immer reproduzierbar (29, 30).
In einer früher veröffentlichten Arbeit waren wir in der Lage zu zeigen, dass die extrakorporale Schockwelle die Fähigkeit besitzt, einen Wundverschluss und eine komplette Epithelialisierung zu erreichen, obwohl der Heilungsmechanismus bis dato ungeklärt ist (21).
Unsere Arbeitshypothese war, dass durch die lokale Energieanwendung eine Neovaskularisierung angeregt wurde. Dieses theoretische Modell erhielt durch vier jüngere Forschungsbeiträge mehr Unterstützung (31, 32, 33). Von besonderem Interesse sind die Erkenntnisse von Kuo (34). Diese Gruppe analysierte den Effekt von ESWT auf Wunden bei diabeteskranken Ratten. Es wurde eine erhöhte Expression von VEGF, eNOS und PCNA beobachtet. Man könnte daher eine neoangiogenetische Eigenschaft der extrakorporalen Schockwelle behaupten. Besonders die letztgenannte Publikation unterstützt unser gegenwärtiges Forschungsprojekt, dass die lokalen, durch ESWT induzierten Wundheilungsprozesse – sogar bei mittellangen Beobachtungszeiträumen – nicht durch Komorbiditäten beeinträchtigt werden. Es scheint daher legitim zu erklären, dass durch die lokale Anwendung von gepulster Energie eine lokale Neoangiogenese erzielt wird, die die negativen generalisierten Aspekte von zum Beispiel metabolischen und ernährungsbedingten Erkrankungen lokal aufhebt.
Keine der beschriebenen unerwünschten Nebenwirkungen nach extrakorporaler Schockwellenbehandlung wie Organperforation (35), hämorrhagischer Schock (24) und Gewebeschädigung durch Gasbläschenbildung oder inerte Hohlraumbildung (36, 37) wurde bei unseren Patienten beobachtet. Die Zerstörung von Nervengewebe (38) konnte nicht überprüft werden, aber die klinische Untersuchung und Nachsorge lieferten keinen Anhalt für diese Annahme. Andere Veröffentlichungen unterstützen unsere Resultate (39). Auch unsere Bedenken, durch Plättchenaktivierung und Gefäßwandzerstörung mit folgender Aktivierung der Gerinnungskaskade ein thrombotisches Geschehen auszulösen, konnte nicht beobachtet werden.
Der Erfolg der ESWT scheint unabhängig von bestehenden Komorbiditäten der Patienten zu sein, da keine der beobachteten Komorbiditäten einen statistischen Einfluss auf die Behandlungserfolgwahrscheinlichkeit hatte.
Zusätzlich hängt der Behandlungserfolg augenscheinlich nicht von der Wundätiologie ab. Chronisch posttraumatische oder postoperative Weichteilwunden stellten die Mehrzahl in dieser Arbeit. Die ESWT venöser und arterieller Ulzera, aber auch Wunden anderer Ätiologie beeinflussten nicht die Wundverschlussrate, wie die multivariate Analyse beweist. Wenn man in unserem Patientenkollektiv die drei mengenmäßig größten Gruppen des ICD 10- Systems – Erkrankungen des Kreislaufsystems, mentale Störungen und Krankheiten des Nervensystems und endokrine-, ernährungsbedingte und metabolische Erkrankungen – mit den drei Wundätiologiegruppen venöse, arterielle Ulzera und Dekubitalulzera vergleicht, würde man erwarten, dass Komorbiditäten einen Einfluss auf die Wundheilung haben. Wenn weiters 47,1 % der Patienten (n = 70) mit Komorbiditäten an exakt diesen drei Wundätiologieentitäten leiden und auch eine hypothetische Korrelation mit diesen drei Ulkustypen, das heißt, 24 % der nach der Wundätiologie anlysierten Patienten (n = 62), aufweisen, hätten wir einen derartigen Einfluss der Komorbiditäten auf den ESWT-Behandlungserfolg erwartet.
Dass dieser von unserem Team erwartete Einfluss auf den Erfolg der ESWT nicht bewiesen werden konnte, liegt zu einem Großteil an den bis jetzt noch nicht verstandenen Wundheilungsmechanismen der extrakorporalen Schockwelle. Die oben angeführten wissenschaftlichen Arbeiten scheinen die Ansicht zu unterstützen, dass die ESWT systemische Effekte lokal außer Kraft setzt. Dies ist vergleichbar mit einer femoro-poplitealen Bypassoperation, die das lokale Zirkulationsproblem behebt, während der Patient weiterhin an der arteriellen Verschlusskrankheit leidet.
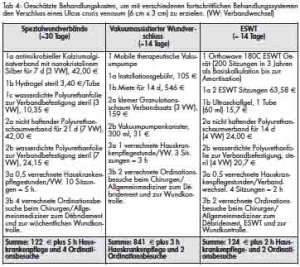
Die ESWT in Kombination mit einem Wundbettbewertungssystem stellt eine wirtschaftlich vertretbare Behandlungsoption dar (Tab 4). Da der Erfolg signifikant durch die Wunddauer und den initialen WBS beeinflusst wird, empfehlen wir ein rechtzeitiges Beginnen und eine Dokumentation des initialen WBS. Sollte nach einem frühen Behandlungsbeginn und nach im Mittel zwei ESWT-Sitzungen kein Anstieg des WBS beobachtbar sein, kann man die ESWT als erfolglos betrachten und die Suche nach anderen Behandlungsoptionen wäre angebracht. Durch die Anwendung der Kombination von ESWT und Wundbettbewertung können unnötige Ambulanzbesuche, Spitals-/Klinikkapazitäten und Arbeitsstunden des medizinischen Personals reduziert werden. Andererseits kann, wenn ein positiver Trend der Wundbettbewertung beobachtet werden würde, in relativ kurzer Zeit (mittlere Dauer der ESWT in erfolgreich behandelten Patienten: 14 Tage oder zwei ESWT-Sitzungen, siehe Tab 2) – verglichen mit der Dauer der chronischen Weichteilwunde vor dem ESWT-Beginn – ein Wundverschluss erzielt werden.
Ein Manko unserer Studie ist das einarmige, nicht randomisierte und nicht verblindete Studiendesign. Aber das Ziel dieser Arbeit war es, all jene Fälle chronischer Weichteilwunden zu behandeln und zu analysieren, die vor ihrer individuellen ESWT erfolglos mit konservativen und chirurgischen Methoden behandelt worden waren. Daher boten wir ESWT allen Patienten, bei denen die konventionellen Behandlungsmethoden mehr als einen Monat gescheitert waren, als allerletzte therapeutische Alternative an.
In der nahen Zukunft werden zusätzliche Phase-2-Forschungsarbeiten nötig sein, um die Heilungsmechanismen der extrakorporalen Schockwelle auf menschliches Gewebe zu erforschen. Parallel dazu bedarf es Einzel- oder multizentrischer Studien, die sich auf eine Komorbidität oder eine Wundätiologie und ihren Einfluss auf den Erfolg der ESWT unter gleichzeitigem Einschluss einer großen Anzahl von freiwilligen Patienten konzentrieren.
Hierfür primäre Untersuchungskandidaten wären Patienten mit metabolischen Erkrankungen und Erkrankungen des Kreislaufsystems.
5. Schlussfolgerungen
Zusammenfassend lässt sich feststellen: Komorbiditäten und die Wundätiologie haben überraschender Weise keinen signifikanten Einfluss auf den Erfolg von ESWT. Lediglich die lokalen Wundeigenschaften – wie durch den WBS repräsentiert – sind relevant, wenn es sich um den Heilungserfolg handelt.
Literatur
- Panuncialman J, Falanga V: The science of wound bed preparation. Surg Clin North Am 2009; 89: 611-626.
- Sanchez-Vazquez R, Briseno-Rodriguez G, Cardona-Munoz EG, Galvez - Gastelum FJ, Totsuka - Sutto SE, Garcia - Benavides L: Isosorbide dinitrate spray as therapeutic strategy for treatment of chronic venous ulcers. Angiology 2008; 59: 64-71.
- Golinko MS, Joffe R, de Vinck D, et al.: Surgical pathology to describe the clinical margin of debridement of chronic wounds using a wound electronic medical record. J Am Coll Surg 2009; 209: 254-260 e1.
- Pappas PJ, Lal BK, Ohara N, Saito S, Zapiach L, Duran WN: Regulation of matrix contraction in chronic venous disease. Eur J Vasc Endovasc Surg 2009; 38: 518-529.
- Wright EH, Khan U:. Serum complement-reactive protein (CRP) trends following local and free-tissue reconstructions for traumatic injuries or chronic wounds of the lower limb. J Plast Reconstr Aesthet Surg 2009.
- Wolff KS, Prusa AM, Bulwas S, et al.: Cluster bomb vs. antipersonnel mine related injuries. An experience from the Kuwaiti-Iraqi border from June 1998 to November 2000. Eur Surg 2007; 39: 111-117.
- Davey RB, Sparnon AL, Byard RW: Unusual donor site reactions to calcium alginate dressings. Burns 2000;26:393-398.
- Demling L, Seuberth K, Riemann JF: A mechanical lithotripter. Endoscopy 1982; 14: 100-101.
- Metzner G, Dohnalek C, Aigner E:. High-energy Extracorporeal Shock-Wave Therapy (ESWT) for the treatment of chronic plantar fasciitis. Foot Ankle Int. 2010; 31: 790-796.
- Biedermann R, Martin A, Handle G, Auckenthaler T, Bach C, Krismer M: Extracorporeal shock waves in the treatment of nonunions. J Trauma 2003; 54: 936-942.
- Martini L, Giavaresi G, Fini M, Borsari V, Torricelli P, Giardino R: . Early effects of extracorporeal shock wave treatment on osteoblast-like cells: a comparative study between electromagnetic and electrohydraulic devices. J Trauma 2006; 61: 1198-1206.
- Nishida T, Shimokawa H, Oi K, et al.: Extracorporeal cardiac shock wave therapy markedly ameliorates ischemia-induced myocardial dysfunction in pigs in vivo. Circulation 2004; 110: 3055-3061.
- Wang FS, Yang KD, Chen RF, Wang CJ, Sheen-Chen SM: Extracorporeal shock wave promotes growth and differentiation of bone-marrow stromal cells towards osteoprogenitors associated with induction of TGF-beta1. J Bone Joint Surg Br 2002; 84: 457-461.
- Dunn F, Lohnes JE, Fry FJ: Frequency dependence of threshold ultrasonic dosages for irreversible structural changes in mammalian brain.J Acoust Soc Am. 1975; 58: 512-514.
- ter Haar GR, Robertson D. Tissue destruction with focused ultrasound in vivo. Eur Urol. 1993; 23 Suppl 1: 8-11.
- Fry FJ, Sanghvi NT, Foster RS, Bihrle R, Hennige C: Ultrasound and microbubbles: their generation, detection and potential utilization in tissue and organ therapy--experimental. Ultrasound Med Biol. 1995; 21: 1227-1237.
- Dalecki D, Child SZ, Raeman CH, Cox C, Carstensen EL: Ultrasonically induced lung hemorrhage in young swine. Ultrasound Med Biol. 1997; 23: 777-781.
- Nyborg WL: Ultrasound, contrast agents and biological cells; a simplified model for their interaction during in vitro experiments. Ultrasound Med Biol. 2006; 32: 1557-1568.
- Miller DL, Dou C, Wiggins RC: Glomerular capillary hemorrhage induced in rats by diagnostic ultrasound with gas-body contrast agent produces intratubular obstruction. Ultrasound Med Biol. 2009; 35: 869-877.
- Schaden W, Fischer A, Sailler A:.Extracorporeal shock wave therapy of nonunion or delayed osseous union. Clin Orthop Relat Res 2001; 90-94.
- Schaden W, Thiele R, Kolpl C, et al.: Shock wave therapy for acute and chronic soft tissue wounds: a feasibility study. J Surg Res 2007; 143: 1-12.
- Falanga V, Saap LJ, Ozonoff A: Wound bed score and its correlation with healing of chronic wounds. Dermatol Ther 2006; 19: 383-390.
- Pastor Navarro H, Carrión López P, Martínez Ruiz J, Pastor Guzmán JM, Martínez Martín M, Virseda Rodríguez JA: Renal hematomas after extracorporeal shock-wave lithotripsy (ESWL). Actas Urol Esp. 2009; 33: 296-303.
- Uemura K, Takahashi S, Shintani-Ishida K, Nakjima M, Saka K, Yoshida K: A death due to perirenal hematoma complicating extracorporeal shockwave lithotripsy. J Forensic Sci 2008; 53: 469-471.
- Samuel S, Cooper MA, Bull JL, Fowlkes JB, Miller DL: An ex vivo study of the correlation between acoustic emission and microvascular damage. Ultrasound Med Biol. 2009; 35: 1574-1586.
- Mullner T, Mrkonjic L, Kwasny O, Vecsei V: The use of negative pressure to promote the healing of tissue defects: a clinical trial using the vacuum sealing technique. Br J Plast Surg 1997; 50: 194-199.
- Robson MC, Phillips LG, Thomason A, Robson LE, Pierce GF: Platelet-derived growth factor BB for the treatment of chronic pressure ulcers. Lancet 1992;339:23-25.
- Brigido SA, Boc SF, Lopez RC:. Effective management of major lower extremity wounds using an acellular regenerative tissue matrix: a pilot study. Orthopedics 2004; 27: 145-149.
- Bouachour G, Cronier P, Gouello JP, Toulemonde JL, Talha A, Alquier P: Hyperbaric oxygen therapy in the management of crush injuries: a randomized double-blind placebo-controlled clinical trial. J Trauma 1996; 41: 333-339.
- Wang C, Schwaitzberg S, Berliner E, Zarin DA, Lau J:. Hyperbaric oxygen for treating wounds: a systematic review of the literature. Arch Surg 2003; 138: 272-279; discussion 80.
- Stojadinovic A, Elster EA, Anam K, et al.: Angiogenic response to extracorporeal shock wave treatment in murine skin isografts. Angiogenesis 2008; 11: 369-380.
- Davis TA, Stojadinovic A, Anam K, et al.: Extracorporeal shock wave therapy suppresses the early proinflammatory immune response to a severe cutaneous burn injury. Int Wound J 2009; 6: 11-21.
- Kuo YR, Wang CT, Wang FS, Yang KD, Chiang YC, Wang CJ: Extracorporeal shock wave treatment modulates skin fibroblast recruitment and leukocyte infiltration for enhancing extended skin-flap survival. Wound Repair Regen 2009;17: 80-87.
- Kuo YR, Wang CT, Wang FS, Chiang YC, Wang CJ: Extracorporeal shock-wave therapy enhanced wound healing via increasing topical blood perfusion and tissue regeneration in a rat model of STZ-induced diabetes. Wound Repair Regen 2009; 17: 522-530.
- Rodrigues Netto N, Jr., Ikonomidis JA, Longo JA, Rodrigues Netto M: Small-bowel perforation after shockwave lithotripsy. J Endourol 2003; 17: 719-720.
- Matlaga BR, McAteer JA, Connors BA, et al.: Potential for cavitation-mediated tissue damage in shockwave lithotripsy. J Endourol 2008; 22: 121-126.
- Miller DL: Overview of experimental studies of biological effects of medical ultrasound caused by gas body activation and inertial cavitation. Prog Biophys Mol Biol 2007; 93: 314-330.
- Hausdorf J, Lemmens MA, Heck KD, et al.: Selective loss of unmyelinated nerve fibers after extracorporeal shockwave application to the musculoskeletal system. Neuroscience 2008; 155: 138-144.
- Malay DS, Pressman MM, Assili A, et al.: Extracorporeal shockwave therapy versus placebo for the treatment of chronic proximal plantar fasciitis: results of a randomized, placebo-controlled, double-blinded, multicenter intervention trial. J Foot Ankle Surg 2006; 45: 196-210.
Datum: 13.12.2012
Quelle: Wehrmedizinische Monatsschrift 2012/11-12