BIOLOGISCHE STRAHLENDOSIMETRIE MITTELS DIZENTRISCHER CHROMOSOMENANALYSE (DCA) NACH INDIVIDUALEREIGNIS UND MASSENANFALL
Aus dem Institut für Radiobiologie der Bundeswehr in Verbindung mit der Universität Ulm, München (Leiter: Oberstarzt Prof. Dr. V. Meineke
von Christina Beinke und Viktor Meineke
Aufgrund des erweiterten Aufgabenspektrums, aktueller Bedrohungslagen und möglicher militärischer Einsätze in der Folge akzidenteller Ereignisse wie dem Reaktorunglück in Fukushima können Angehörige der Bundeswehr dem Risiko einer potenziellen Strahlenexposition ausgesetzt sein.
Das Spektrum reicht dabei von einer externen Exposition bedingt durch eine Umgebungsstrahlung oder Kontamination mit radioaktivem Material bis hin zur internen Exposition nach einer Inkorporation von Radionukliden. Diesen Expositionen gemeinsam ist die medizinische Konsequenz von strahlenbedingten Früh- (Akute Strahlenkrankheit) beziehungsweise Spätschäden (genetische Schäden / Krebsentstehung). Der Nachweis einer Strahlenexposition und die Abschätzung der individuell absorbierten Dosis als Voraussetzung für die Planung therapeutischer Maßnahmen erfolgt ergänzend zur klinischen und gegebenenfalls physikalischen Dosimetrie mittels spezialdiagnostischer Biodosimetrie- Verfahren.
Abhängig vom Expositionsszenario, zum Beispiel einem akuten Massenanfall möglicher Strahlenunfallopfer, einem akuten Individualereignis oder einer Jahrzehnte zurückliegenden chronischen Exposition, wird ein geeignetes Verfahren ausgewählt. Mit der Analyse dizentrischer Chromosomen und reziproker Translokationen sowie der Zytokinese-Block (CB)-Mikrokern-Analyse stehen dem InstRadBioBw drei international anerkannte Biodosimetrie-Verfahren zur Verfügung, wobei die Dizentrische Chromosomenanalyse (DCA) als die am besten validierte und zuverlässigste Methode zur Abklärung unklarer Strahlenexpositionen gilt. Strategien zur Weiterentwicklung der DCA zu einer leistungs- und netzwerkfähigen Hochdurchsatz-Diagnostik und die Durchführung der DCA am InstRadBioBw werden dargelegt.
Application of the dicentric chromosome analysis (DCA) for biological radiation dosimetry after an individual event and a mass casualty scenario
Summary
Servicemen and -woman are at risk of a potential radiation-exposure due to the enlarged spectrum of deployment of the Bundeswehr for actual risk assessment as well as for military missions after incidents like the Fukushima reactor accident. The spectrum of radiation-exposure covers the external exposure from the environment or the contamination with dispersed radionuclides and internal exposure after incorporation of radio nuclides. All these different types of exposure will lead at least to the clinical consequences of short-term (acute radiation syndrome) or long-term (mutagenesis / cancerogenesis) effects. The verification and quantification of radiation exposure as prerequisite for therapy planning will be performed additionally to clinical and if available physical dosimetry by cytogenetic biological (bio) dosimetry techniques.
In respect of the actual exposure scenario, e. g. a mass casualty event involving a great number of potentially overexposed persons, an individual event or a chronicle exposure which has occurred several decades before, an appropriate biodosimetry method will be chosen. Among three international accepted biodosimetry tools (dicentric chromosome, reciprocal translocation and cytokinesis-block-micronucleus analysis) established at the InstRadBioBw the dicentric chromosome assay (DCA) is considered as the most validated and reliable “gold standard” for biological dosimetry after an acute radiation exposure. The exerted strategies to develop the DCA to a powerful and network-capable high-throughput diagnostic tool will be discussed and the performance of the DCA in the InstRadBioBw will be presented.
Einleitung
Nach einer akuten Strahlenexposition gegenüber Röntgen- oder Gammastrahlung sind häufig therapeutische Maßnahmen einzuleiten oder zumindest Aussagen bezüglich assoziierter Gesundheitsrisiken zu treffen. Dabei ist der Massenanfall potenzieller Strahlenverunfallter eine besondere Herausforderung, da mit Hunderten oder noch mehr Betroffenen, sogenannten „worried well“ (keine oder geringe Strahlenexposition) bis hin zu Patienten mit schweren Gesundheitsstörungen, zu rechnen ist. Um Personen ohne oder mit geringer Exposition von den Patienten zu unterscheiden, die therapeutischer Maßnahmen bedürfen, ist eine schnelle Hochdurchsatz-Screening-Methode im Rahmen der Sichtung erforderlich. Nur so können die zur Verfügung stehenden medizinischen Ressourcen optimal eingesetzt und genutzt werden.
Als Methode der Wahl für die individuelle biologische Dosimetrie nach einem akuten Ereignis gilt nach wie vor die bereits in den sechziger Jahren beschriebene dizentrische Chromosomenanalyse (DCA) [1, 2]. Unter biologischer Dosimetrie versteht man den Nachweis einer Exposition gegenüber ionisierender Strahlung und die Quantifizierung der absorbierten Dosis anhand biologischer Indikatoren. Das dizentrische Chromosom ist vor allem aufgrund seiner Spezifität für ionisierende Strahlung bei niedriger Spontanhäufigkeit, seiner hohen Sensitivität und der sehr hohen Korrelation zwischen einer In-vivo- und In-vitro-Induktion der zuverlässigste biologischer Indikator für eine Exposition gegenüber ionisierender Strahlung.
Das Hauptaugenmerk der Forschung und Aktivitäten in der zytogenetischen Biodosimetrie liegt gegenwärtig auf der Weiterentwicklung der DCA zur Hochdurchsatz-Methode, um die Kapazität der Biodosimetrie nach einem akuten Ereignis zu erhöhen. Um dies zu erreichen, werden verschiedene Strategien wie die Einführung des zytogenetischen Triage-Modus, Standardisierung, Netzwerkbildung und Automatisierung verfolgt. Während der Triage-Modus und die Automatisierung der Arbeitsabläufe eine sehr schnelle Bereitstellung dosimetrischer Informationen nach Strahlenexposition gewährleisten [3, 4], ermöglichen die Standardisierung der Methode und der Aufbau nationaler und internationaler Biodosimetrie-Netzwerke letztendlich die Aufteilung der Arbeitsbelastung bei großem Probenaufkommen auf mehrere Dosimetrielaboratorien [5, 6].
2. Methode
2.1 Dizentrische Chromosomenanalyse (DCA)
2.2.1 Hintergrund
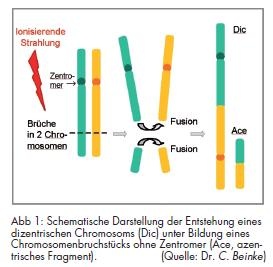
Die Methode basiert auf der Fähigkeit ionisierender Strahlung, DNA-Doppelstrangbrüche zu induzieren, wenn sie auf einen Zellkern trifft, zum Beispiel den Interphase-Zellkern eines zirkulierenden Blutlymphozyten. Als Folge einer anschließenden Fusion zweier zentromerhaltiger Chromosomenbruchstücke („falsche“ Reparatur) entsteht ein dizentrisches Chromosom, in der Regel unter Bildung eines Chromosomenbruchstückes ohne Zentromer (azentrisches Fragment, Abb 1). Diese Aberrationen können nach Stimulierung der Zellteilung und Arretierung in der Metaphase durch Anfärben mikroskopisch sichtbar gemacht werden. Dizentrische Chromosomen zählen zu den instabilen, letalen Aberrationen, das heißt, die Zelle verliert nach spätestens zwei bis drei Teilungen irreversibel ihre Teilungsfähigkeit. Daher sind dizentrische Chromosomen für die Analyse lange zurückliegender Expositionen weniger gut geeignet als stabile, über die Zeit persistierende, symmetrische- Translokationen.
2.2.2 Durchführung
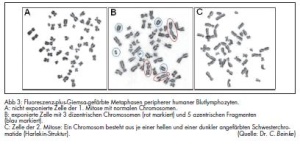
Die DCA (Abb 2) wird mit einfach zu gewinnendem Probenmaterial, möglichst innerhalb von vier Wochen nach Strahlenexposition entnommenem peripherem venösem Blut, durchgeführt. Die mit Phythämagglutinin zur Teilung stimulierten Lymphozyten benötigen eine 48- stündige Kultivierung, inklusive der Blockierung der Zellen in der Metaphase durch Zugabe des Spindelgiftes Colcemid. Anschließend werden die Zellen geerntet und die Metaphasen nach hypotonischer Behandlung mit einem Methanol/Eisessig-Gemisch fixiert. Auf Glasobjektträger aufgebracht, werden die Präparate der Fluoreszenz-plus-Giemsa-Färbung unterzogen, wodurch aufgrund der Kultivierung in Gegenwart von Bromdesoxyuridin Metaphasen der ersten und zweiten Mitose unterschieden werden können (Abb 3). Anschließend wird die mikroskopisch beobachtete Häufigkeit dizentrischer Chromosomen in Metaphasen der ersten Mitose mit Bezug auf eine laborintern erstellte Standard-Kalibrierkurve in eine Dosis umgerechnet.
2.2.3 Dosisrekonstruktion
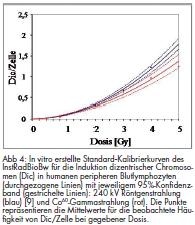
Um die Dosis zuverlässig abschätzen zu können, muss ein Dosimetrielabor über eigene, in vitro mit humanen Lymphozyten generierte, Standard-Kalibrierkurven verfügen. Nur so können die durch methodische Variationen bedingten Ungenauigkeiten ausgeschlossen werden. Dazu wird für mindestens acht Dosen von 0,1 Gy bis 4,0 Gy die Dizentrik-Häufigkeit pro Zelle bestimmt und die Dosis-Wirkungsbeziehung aufgestellt. Die Anzahl der auszuwertenden Metaphasen liegt in Abhängigkeit von der Höhe der applizierten Dosis zwischen mehreren 100 und mehreren 1 000 Metaphasen pro Dosis. Zusätzlich sind laborintern erstellte Kontrolldaten auf der Basis der spontanen Dizentrik-Häufigkeit in nicht strahlenexponierten Personen notwendig. Für die Berechnung der Koeffizienten der Standardkurve sowie zur Abschätzung der Dosis nach fraglicher Strahlenexposition existieren mittlerweile speziell für die zytogenetische Dosimetrie entwickelte und frei erhältliche Computerprogramme („CABAS“, „DoseEstimate“) [7, 8]. InstRadBioBw besitzt zur Dosisrekonstruktion laborintern erstellte Standard-Kalibrierkurven für 240 kV Röntgen- und Co60-Gammastrahlung (Abb 4). Daneben sind eigene Kontrolldaten zur Spontanhäufigkeit verfügbar, welche 0,7 dizentrische Chromsomen pro Zelle beträgt und in ca. 16 000 Metaphasen aus unbestrahltem Blut bestimmt wurde.
3. Anwendungsbereich
3.1 Dosisabschätzung
Die DCA kann zur Dosisrekonstruktion grundsätzlich nach akuter oder chronischer homogener oder inhomogener Ganzkörper- oder Teilkörperexposition eingesetzt werden. Nach akuter homogener Ganzkörperexposition beträgt die untere Nachweisgrenze der DCA ca. 0,1 Gy für locker ionisierende Strahlung (Gamma-, Röntgenstrahlung). Für eine zuverlässige Dosisabschätzung nach fraglicher Strahlenexposition müssen in diesem niedrigen Dosisbereich bis zu 1 000 Metaphasen ausgewertet werden. Dagegen ist die Methode nach chronischer Strahlenexposition weniger sensitiv, da die Dizentrik-Häufigkeit in Abhängigkeit vom Turnover der Lymphozyten im peripheren Blut einer strahlenexponierten Person im Verlauf der Zeit sinkt. Daher muss mit geeigneten Rechenmodellen unter Berücksichtigung der Lymphozyten-Halbwertszeit von 1,5 bis 3 Jahren [10, 11] die initiale Aberrationshäufigkeit und anschließend die absorbierte Dosis geschätzt werden.
Nach inhomogener oder Teilkörperexposition haben sowohl Dosis als auch betroffenes Körpervolumen einen Einfluss auf die Aberrationshäufigkeit. Nach der Exposition vermischen sich die im betroffenen Körperareal geschädigten Zellen im Blutkreislauf mit ungeschädigten Zellen. Zur Dosisberechnung und Abschätzung der Größe des betroffenen Körpervolumens müssen statistische Rechenmodelle zur Betrachtung der Verteilung der dizentrischen Chromosomen auf die Zellen hinzugezogen werden (Methode nach Dolphin, QdR-Methode) [12, 13].
3.2 Zytogenetischer Triage-Modus
Für eine zuverlässige individuelle Dosisabschätzung müssen in Abhängigkeit von der Höhe der absorbierten Dosis bis zu 1 000 Metaphasen ausgewertet werden. Sind nur wenige Blutproben potenziell exponierter Personen zu analysieren, kann dies in wenigen Wochen geschehen. Zur Erhöhung des Probendurchsatzes und Beschleunigung der Analyse im Fall eines sehr großen Probenaufkommens wurde die Durchführung der Analyse im Triage- Modus vorgeschlagen (Tab 1) [3]. Die konventionelle Methode, basierend auf der Auswertung von bis zu 1 000 Zellen, ist zwar sehr zeitaufwendig, liefert aber sehr zuverlässige Dosisabschätzungen. Der Triage-Modus dagegen ergibt nach der deutlich weniger zeitaufwendigen Auswertung von nur 20- 50 Zellen oder 30 dizentrischen Chromosomen sehr schnelle und grobe Abschätzungen (± 0,5 Gy), die aber für eine Triage als ausreichend gelten. In mehreren Ringversuchen konnte nun die DCA für die zytogenetische Triage auch als Netzwerk-taugliche Methode validiert werden [14, 15, 16). Weitere Studien zielen darauf ab, den Triage- Modus noch weiter zu verkürzen, indem zum Beispiel die Anzahl der auszuwertenden Metaphasen weiter verringert wird (Quickscan) [17].
Die DCA kann also in Abhängigkeit vom jeweiligen Expositionsszenario in zwei verschiedenen Modi durchgeführt werden: konventioneller und Triage- Modus. Der konventionelle Modus liefert sehr zuverlässige Dosisabschätzungen, ist in der Durchführung aber sehr zeitintensiv (2 – 6 Wochen), da bis zu 1 000 Metaphasezellen ausgewertet werden müssen. Der Triage-Modus liefert dagegen nach nur 4 Tagen (Auswertung von 20 – 50 Metaphasen) eine grobe Abschätzung der Dosis (+/- 0,5 Gy), was für die Sichtung der Betroffenen aber als ausreichend gilt.
3.3 Standardisierung und Netzwerkbildung
Zur Harmonisierung zytogenetischer Biodosimetriemethoden hat die IAEA ein Handbuch herausgegeben, welches neben einer umfassenden Darstellung der einzelnen Verfahren, technische Details und Protokolle zur praktischen Durchführung der Methoden enthält. Für die DCA geben zusätzlich zwei ISO-Normen Richtlinien zur Durchführung im konventionellen und im Triage-Modus im Hinblick auf die laborinterne Qualitätssicherung vor [18, 19]. Durch internationale Projekte, zum Beispiel das EU-finanzierte Projekt „Multibiodose“ [20], werden Biodosimetrieverfahren, unter anderem die DCA, zwischen verschiedenen Laboren nicht nur harmonisiert sondern auch an unterschiedliche Massenunfallszenarien angepasst. Zur weiteren Harmonisierung und Validierung vor allem der DCA tragen die von einem effektiven Qualitätsmanagement geforderten Ringversuche bei [14, 16, 22].
Eine solche Standardisierung ist Voraussetzung für die Bildung von Dosimetrie- Netzwerken zur Aufteilung der Arbeitsbelastung bei sehr großem Probenaufkommen. Da die Kapazität eines einzelnen Labors, abhängig von Geräteausstattung und Anzahl erfahrener Mitarbeiter, im Falle eines großen Probenaufkommens schnell überschritten sein kann, werden Biodosimetrie- Netzwerke auf nationaler und internationaler Ebene gebildet, um bei Bedarf durch Arbeitsteilung effizient reagieren zu können. Auf internationaler Ebene etablierte zum Beispiel die WHO das weltweite Netzwerk „BioDoseNet“ zur Unterstützung des Strahlenunfallmanagements, wenn die Kapazität der nationalen Labore im Falle eines großen Strahlenunfalls unzureichend ist [5].
Im InstRadBioBw werden alle Abläufe gemäß seinem zertifizierten Qualitätsmanagementsystem nach ISO 9001:2008 durchgeführt. So wird die systematische Leitung und Lenkung des Institutes, ausgerichtet auf eine ständige Leistungsverbesserung, gewährleistet. Dies geschieht mit besonderem Augenmerk auf die Kundenorientierung (Kunde: Dienstherr, bundeswehrinterne und -externe nationale und internationale Kooperationspartner) und die Einbeziehung unserer Mitarbeiter in das Qualitätsmanagement.
Für den Betrieb eines medizinisch-diagnostischen Servicelabors ist zusätzlich die Einführung und Aufrechterhaltung eines Qualitätsmanagementsystems essenziell, welches die Anforderungen geeigneter branchenspezifischer Normen erfüllt. Um erfolgreich in nationalen und internationalen diagnostischen Netzwerken mitzuwirken, muss die Verlässlichkeit der medizinischen Befunde gewährleistet sein. Der Fachbereich „Zytogenetik“ strebt daher zum Nachweis seiner Kompetenz auf dem Gebiet der Spezialdiagnostik zusätzlich die Akkreditierung gemäß der weltweit gültigen Norm ISO 17025:2008 („Allgemeine Anforderungen an die Kompetenz von Prüfund Kalibrierlaboratorien“) an [21]. Unter Berücksichtigung des methodenspezifischen ISO Normen [18, 19] wird so die Vergleichbarkeit und Reproduzierbarkeit der Messergebnisse der DCA im InstRadBioBw belegt.
3.4 Automatisierung
Die Automatisierung einzelner Arbeitsschritte hat neben der enormen Zeitersparnis auch eine deutlich verbesserte Reproduzierbarkeit der Ergebnisse zur Folge. Vor allem zur Durchführung der Metaphasenpräparation und bildanalytischen Auswertung der Metaphasen inklusive Mikroskopie und Chromosomenanalyse wurden technische Innovationen eingeführt.
Die Fixierung von Metaphasen kann durch den Einsatz eines Metaphasen- Erntemaschine-Systems vollautomatisiert durchgeführt werden (Hannabi Harvester PII, Transgenomic Ltd., Glasgow, UK) (Abb 5). Alle Funktionen wie Zentrifugation, Aspiration, Zufügen der hypotonischen oder Fixiermittellösungen und Resuspendierung der Zellen laufen gemäß vorprogrammiertem Protokoll ab. Diese Zeit kann nun für die Färbung oder Auswertung bereits fertiggestellter Präparate genutzt werden. Der automatisierte Ablauf der Metaphase- Fixierung sorgt vor allem für eine gleichbleibende gute Qualität der Metaphasen und in der Folge für eine größere Reproduzierbarkeit der Ergebnisse und somit auch für eine zuverlässigere Dosimetrie.
Der Einsatz des automatisierten Mikroskopsystems (Abb 6, Metafersystem, Metasystems, Altlussheim, Deutschland) beschleunigt das Auffinden, Aufnehmen und Speichern von Giemsa-gefärbten Metaphasen mindestens um das 20fache. Dieser Vorgang läuft über Nacht ab, sodass die Auswertung direkt am nächsten Morgen beginnen kann. Die manuelle Auswertung, das heißt die mikroskopische Beurteilung jeder einzelnen Metaphase, erfordert eine Einarbeitungszeit von mehreren Monaten und einen fortwährenden laborinternen Abgleich der Ergebnisse verschiedener „Auswerter“, um reproduzierbare Ergebnisse zu erhalten.
Für die manuelle Auswertung von 1 000 Metaphasen müssen in Abhängigkeit von der Qualität der Präparate, der Aberrationshäufigkeit und der Erfahrung des Mitarbeiters mindestens zwei bis vier Tage angesetzt werden zusätzlich zu einer abschließenden Kontrolle aller Aberrationen durch einen erfahrenen Zytogenetiker. Das Software-Modul „DCScore“ (Abb 7, MetaSystems, Altlussheim, Deutschland) ermöglicht dagegen die vollautomatische Analyse der Dizentrik-Häufigkeit in 1 000 Metaphasen in weniger als fünf Minuten. Eine anschließende visuelle Kontrolle der als dizentrisch erfassten Chromosomen durch einen Zytogenetiker nimmt ebenfalls nur wenigen Minuten in Anspruch.
Im Anschluss müssen die Dosisberechnungen gegebenenfalls für jeden einzelnen Patienten ausgeführt und strukturiert dokumentiert und archiviert werden. Die oben genannten anwenderfreundlichen Computerprogramme „CABAS“ und „DoseEstimate“ gewährleisten eine zeitnahe, zuverlässige und übersichtliche Bereitstellung der Daten insbesondere für eine schnelle Triage einer Vielzahl potenziell überexponierter Personen.
Ein „sample-in/result-out“ System, wie es für die Mikrokern- und DNA-Bruchstellen- (FOCI-) Analyse bereits in Erprobung ist [23], existiert gegenwärtig noch nicht. Verschiedene Ansätze zur Automatisierung aller übrigen Arbeitsschritte und auch deren Verknüpfung befinden sich aber in der Entwicklungsphase und sind teilweise bereits realisiert worden [4]. Durch den Einsatz des Metaphaseerntesystems Hanabi PII und des automatisierten Mikroskopsystems sind die Abläufe der DCA im InstRadBioBw bereits weitgehend automatisiert worden. Der nächste Schritt ist die Erstellung von robusten Standard-Kalibrierkurven unter Anwendung des DCScore Software- Moduls, um auch den Zeitaufwand für die mikroskopische Auswertung der Metaphasen maximal zu beschleunigen und dadurch eine schnellstmögliche Bereitstellung dosimetrischer Informationen für den behandelnden Arzt zu gewährleisten.
4. Schlussfolgerungen
Die DCA ist insbesondere in den vergangenen zehn Jahren als spezialdiagnostisches Dosimetrieverfahren in der Strahlenmedizin rasant weiterentwickelt worden. Durchgeführt im konventionellen und manuellen Modus gilt sie als die am besten validierte Methode zur individuellen Biodosimetrie nach akuter Strahlenexposition. Das derzeit wichtigste Ziel ist es, dieselbe Zuverlässigkeit und Genauigkeit des Verfahrens auch bei Automatisierung und Bewältigung einer großen Zahl von Blutproben potenziell überexponierter Personen sowohl innerhalb eines einzelnen Labors als auch im Rahmen einer effizienten internationalen Netzwerk-Diagnostik zu erreichen.
Durch die Teilnahme am Aufbau von Biodosimetrie-Netzwerken auf nationaler und internationaler Ebene, an internationalen Projekten und der Akkreditierung gemäß ISO 17025 mit Durchführung weiterer Ringversuche wird die zytogenetische Biodosimetrie, insbesondere die DCA, im InstRadBioBw fortschreitend weiterentwickelt und im Hinblick auf Qualitätsmanagement und -sicherung optimiert. Das bedeutet außerdem, bestehende Kalibrierkurven (manuell/automatisiert) fortwährend zu aktualisieren und diagnostische Fähigkeiten im Hinblick auf weitere relevante Strahlenqualitäten auszuweiten, um dieses für die sanitätsdienstliche Einsatzunterstützung essenzielle Verfahren auf aktuellstem Stand anbieten zu können.
Literatur
- Bender MA, Gooch PC: Persistent chromosome aberrations in irradiated human subjects. Rad Res 1962; 16: 44-53
- IAEA: Cytogenetic Analysis for Radiation Dose Assessment. A Manual (Technical Report 405), Vienna: International Atomic Energy Agency; 2001
- Lloyd DC, Edwards AA, Moquet JE, Guerrero-Carbajal YC: The role of cytogenetics in early triage of radiation casualties. Applied Radiation and Isotopes 2000; 52: 1107-1112
- Martin PR, Berdychevski RE, Subramanian U, Blakely WF, Prasanna PG: Sample Tracking in an Automated Cytogenetic Biodosimetry Laboratory for Radiation Mass Casualties. Radiat Meas 2007; 42(6-7):1119-1124
- Blakely, W.F., Carr Z, Chub M et al.: WHO 1st Consultation on the Development of a Global Biodosimetry Laboratories Network for Radiation Emergencies (BioDoseNet). Rad Res 2009; 171(1): 127-139.
- Wilkinson, D., Segura, T., Prud’homme-Lalonde, L., et al.: Canadian biodosimetry capacity for response to radiation emergencies. Radiat Meas 2007; 42(6-7): 1128-1132.
- Deperas J, Szluinska M, Deperas-Kaminska M, Edwards A, Lloyd D, Lindholm C, et al.: CABAS: a freely available PC program for fitting calibration curves in chromosome aberration dosimetry. Radiat Prot Dosim 2007; 124:115-23.
- Ainsbury EA, Lloyd D. Software for dose estimation for cytogenetic biodosimetry. Health Phys 2010; 98(2): 290-295
- Beinke C, Braselmann H, Meineke V: Establishment of An X-Ray Standard Calibration Curve By Conventional Dicentric Analysis As Prerequisite for Accurate Radiation Dose Assessment. Health Physics 2010; 98(2): 261-268.
- Lloyd DC, Purrt RJ, Reeder EJ: The incidence of unstable chromosome aberrations in peripheral blood lymphocytes from unirradiated and occupationally exposed people. Mutation Research 1980; 72:523-532
- Ramalho AT, Nascimento AC: The fate of chromosomal aberrations in 137 Cs-exposed individuals in the Goiania radiation accident. Health Phys 1991; 60(1):67-70
- Dolphin G: Biological dosimetry with particular reference to chromosome aberrations analysis. A review of methods: In: Handling of radiation accidents. Vienna: Proc Int Symp; 1969
- Sasaki MS, Miyata H: Biological dosimetry in atomic bomb survivors. Nature 1968; 220:1189-93
- Di Giorgio M, Barquinero JF, Vallerga MB, Radl A, Taja MR, Seoane A et al.: Biological Dosimetry Intercomparison Exercise: An Evaluation of Triage and Routine Mode Results by Robust Methods. Rad Res 2011; 175: 638-649
- Romm H, Wilkins RC, Coleman CN, Lillis-Hearne PK, Pellmar TC, Livingston GK et al.: Biological Dosimetry by the Triage Dicentric Chromosome Assay: Potential Implications for Treatment of Acute Radiation Syndrome in Radiological Mass Casualties. Radiation Research 2011; 175(3):397-404
- Beinke C, Oestreicher U, Riecke A, Kulka U, Meineke V, Romm H: Inter-laboratory comparison to validate the dicentric assay as a cytogenetic triage tool for medical management of radiation accidents. Radiat Meas 2011; Epub; http://dx.doi.org/10.1016/j.radmeas.2011.05.038
- Flegal FN, Devantier Y, McNamee JP, Wilkins RC. Quickscan dicentric chromosome analysis for radiation biodosimetry. Health Phys 2010; 98(2): 276-281
- International Organization for Standardization (ISO): Radiation Protection – Performance criteria for service laboratories performing biological dosimetry by cytogenetics. ISO 19238, ISO, Genf; 2004
- International Organization for Standardization (ISO): Radiation Protection – Performance criteria for service laboratories performing cytogenetic triage for assessment of mass casualties in radiological or nuclear emergencies – General principles. ISO 21243, ISO, Genf; 2008
- Multi-disciplinary biodosimetric tools to manage high scale radiological casualties (MULTIBIODOSE) - Capability project funded within the 7th EU Framework Programme under Theme 10 – SECURITY: http://www.multibiodose.eu/index.htm
- International Organization for Standardization (ISO): Allgemeine Anforderungen an Prüf- und Kalibrierlaboratorien. ISO 17025, ISO, Genf; 2008
- Wilkins CR, Romm H, Kao T et al.: Interlaboratory comparison of the dicentric chromosome assay for radiation biodosimetry in mass casualty events. Rad Res 2008; 169(5): 551-560 [23] Garty C, Chen Y, Salerno A. et al.: The RABIT: A rapid automated biodosimetry tool for radiological triage. Health Physics 2010; 98(2): 209-217
Datum: 28.11.2011
Quelle: Wehrmedizinische Monatsschrift 2011/8-9