HYPERTROPHE OBSTRUKTIVE KARDIOMYOPATHIE (HOCM) – FALLDARSTELLUNG
Hypertrophic obstrucive cardiomyopathy - Case report
Aus der Abteilung für Innere Medizin (Leitender Arzt: Oberstarzt Dr. U. Schumann) am Bundeswehrkrankenhaus Westerstede (Chefarzt: Flottenarzt Dr. K. Reuter)
Anja Siepelmeyer und Udo Schumann
WMM; 57. Jahrgang (Ausgabe 5-6/2013, S: 129-132)
Zusammenfassung
Der plötzliche Herztod gehört zu den häufigsten Todesursachen in Deutschland. Ursächlich sind meist ventrikuläre Herzrhythmusstörungen im Rahmen von strukturellen Herzerkrankungen.
Die hypertrophe obstruktive Kardiomyopathie (syn.: Myokardiopathie) gewinnt in diesem Rahmen eine besondere Bedeutung, da es sich um die häufigste genetische Erkrankung des Myokards handelt mit erhöhtem Risiko für maligne Herzrhythmusstörungen. Insbesondere bei jungen Leistungssportlern gilt sie als häufige Ursache des plötzlichen Herztodes. So gibt es zahlreiche Beispiele von plötzlichen Todesfällen von vermeintlich gesunden Sportlern.
Dies ist von besonderer wehrmedizinischer Relevanz aufgrund der körperlichen Belastung von Soldaten im In- und Ausland. Dieser Artikel soll Truppenärzte sensibilisieren, Patienten mit entsprechendem Risikopotenzial frühzeitig zu erkennen und im Zweifel großzügig Facharztabteilungen vorzustellen.
Schlagworte: Plötzlicher Herztod, hypertrophe obstruktive Kardiomyopathie.
Summary
Sudden cardiac death is the most common cause of death in Germany and other industrial nations. Often it is caused by ventricular irregular heart beats in patients with an structural heart disease. The hypertrophic obstructive cardiomyopathy (CM) is a leading cause of sudden unexpected cardiac death in young athletes. It is a genetic disease of the myocardium and the prevalence is about 0.2 % to 0.5 % of the general population. Patients are frequently asymptomatic until sudden cardiac death and for this reason it is important to identify high risk patients early. Military physicians should be aware of the patients with an appropriate risk potential.
Keywords: Sudden cardiac death, hypertrophic obstructive cardiomyopathy.
Einleitung
Der plötzliche Herztod (PHT) gehört mit einer Häufigkeit von über 100 000 Todesfällen/Jahr in Deutschland zu den häufigsten Todesursachen [1, 2]. Er wird definiert als natürlicher Tod durch eine kardiale Ursache innerhalb von einer Stunde nach Auftreten erster Symptome [2, 3]. Ursächlich sind häufig ventrikuläre Arrhythmien [2, 3, 4]. Mit zunehmendem Patientenalter entstehen diese meist im Rahmen einer koronaren Herzerkrankung [3, 4]. Bei jungen Patienten kommt es jedoch vielfach zum plötzlichen Herztod durch anderweitige strukturelle Herzerkrankungen [5]. Der hypertrophen obstruktiven Kardiomyopathie (HOCM) kommt dabei eine besondere Bedeutung zu.
Hypertrophe obstruktive Kardiomyopathie
Die hypertrophe obstruktive Kardiomyopathie (HOCM) ist die häufigste genetische Erkrankung des Myokards [6, 7]. Betroffen ist circa einer von 500 – 1 000 Einwohnern [7]. Es besteht ein autosomal-dominanter Erbgang mit variabler Penetranz, sodass in circa 50 % der Fälle eine familiäre Häufung auftritt [6, 7]. Aktuell sind über 1 400 Mutationen an über acht Genen bekannt [8]. Häufig betroffene Proteine sind die schwere Kette des Beta-Myosins, das Myosinbindungsprotein C und das Troponin T, die insgesamt für etwa 70 % der HOCM-Fälle verantwortlich sind [6, 7]. Eine Korrelation zwischen Genmutation und klinischer Ausprägung der HOCM ist bisher nicht nachgewiesen [7]. Eine Genmutationsanalyse sollte allerdings nur zum Familienscreening von Angehörigen ersten Grades erfolgen [7].
Histologisch zeigt sich dies typischerweise in einem „fiber disarray“ mit verdickten Kardiomyozyten, die in Wirbeln und verzweigt angeordnet sind [6, 7]. Durch die Fehlorganisation der Myozyten kommt es zu einer asymmetrischen Hypertrophie vor allem des linken Ventrikels mit Beteiligung des Septums und Obstruktion des linksventrikulären Ausflusstraktes [6, 7]. Abhängig von der Morphologie entwickelt sich somit eine dynamische Obstruktion mit Ausbildung eines intrakavitären systolischen Druckgradienten, welcher unter Belastung weiter ansteigt [6, 7].
Klinisch bleiben die Patienten oft beschwerdefrei. Erst unter Belastung treten bei einem Teil der Patienten Dyspnoe und pektanginöse Beschwerden, Schwindel, Palpitationen und Synkopen auf [6, 7]. Von besonderer Bedeutung ist der plötzliche Herztod durch maligne Herzrhythmusstörungen bei bis dahin asymptomatischen Patienten, zumeist nach starker körperlicher Belastung [3 – 7].
Die körperliche Untersuchung ergibt gewöhnlich einen Normalbefund [6, 7]. Gelegentlich besteht jedoch bei Betroffenen ein Systolikum mit punctum maximum über Erb, das sich unter Belastung verstärkt aufgrund der dynamischen Obstruktion des Ausflusstraktes mit assoziierter Mitralinsuffizienz [7]. Das EKG ist meist nicht wegweisend und zeigt mitunter Linkshypertrophiezeichen, zum Teil bestehen auch Pseudoinfarktzeichen mit tiefen Q-Zacken und T-Negativierungen [6, 7]. Die Durchführung eines Langzeit-EKG zum Nachweis von Herzrhythmusstörungen, insbesondere ventrikulärer Tachykardien, ist zwingend erforderlich [6, 7].
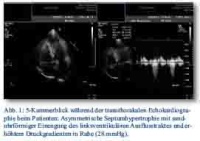
Echokardiographisch zeigt sich typischerweise eine asymmetrische Septumhypertrophie ( > 13 mm Dicke) oder eine Hypertrophie des gesamten linksventrikulären Myokards mit sanduhrförmiger Einengung des linksventrikulären Ausflusstraktes [7]. Zudem wölbt sich in der Systole das vordere Mitralsegel gegen das Septum. Dies wird auch als „systolic anterior motion“ (SAM)-Phänomen) bezeichnet [6, 7]. Gleichzeitig kommt es zum vorzeitigen Schluss der Aortenklappe [7]. Das Ausmaß der Obstruktion ist in der Dopplerechokardiographie über ein säbelscheidenartiges Flussprofil sichtbar und mittels erhöhter systolischer Flussgeschwindigkeit im linksventrikulären Ausflusstrakt mit erhöhtem Druckgradienten messbar [7]. Eine Provokation ist obligat und bewirkt eine weitere Zunahme der Druckgradienten [7]. Somit kann eine hämodynamische Klassifikation nach ACC/ESC in drei Schweregrade vorgenommen werden:
– Grad 1: Druckgradient > 30 mmHg in Ruhe,
– Grad 2: Druckgradient < 30 mmHg in Ruhe oder > 30 mmHg unter Provokation,
– Grad 3: Druckgradient < 30 mmHg in Ruhe und unter Provokation.
Weiterführende bildgebende Verfahren wie Kardio-CT oder Kardio-MRT sind ebenfalls möglich zur Bestimmung der asymmetrischen Hypertrophie sowie erhöhter Druckgradienten [7].
Eine invasive Diagnostik mittels Herzkatheteruntersuchung ist vor einer geplanten operativen Therapie einer HOCM und zum Ausschluss einer begleitenden koronaren Herzerkrankung (KHK) oder bei unsicherer Diagnose der HOCM indiziert [6, 7].
Therapeutisch steht zunächst das Meiden von starker körperlicher Belastung im Vordergrund [3, 4, 6, 7]. Daher sind auch positiv inotrope Substanzen (Digitalis, Sympathomimetika), starke Nachlastsenker und Nitrate kontraindiziert [6, 7]. Vielmehr besteht die Indikation zur Betablockertherapie, alternativ auch die Gabe von Verapamil bei Betablockerunverträglichkeit [3, 4, 6, 7]. Eine gegebenenfalls koexistente arterielle Hypertonie sollte medikamentös straff eingestellt werden zur Reduktion des myokardialen Wachstumsstimulus [7]. Es werden diesbezüglich neben Betablockern und Diuretika auch zentrale Alphablocker empfohlen [7].
Abhängig vom Risikoprofil wie positive Familienanamnese, rezidivierende Synkopen, linksventrikuläre Hypertrophie > 30 mm, ventrikuläre Tachykardien und hypotones Blutdruckverhalten unter Belastung (siehe Tab. 1) ist eine Implantation eines implantierbaren Cardioverter Defibrillators (ICD) zur Primärprophylaxe des plötzlichen Herztodes durch maligne Herzrhythmusstörungen anzustreben [3, 4, 6, 7, 9].
Bei erheblicher Obstruktion des linksventrikulären Ausflusstraktes kann eine interventionelle Therapie mittels chirurgischer Myoektomie oder auch durch die transkoronare Ablation der Septumhypertrophie (TASH) erfolgen [6, 7]. Indiziert ist dies bei symptomatischen Patienten mit NYHA III – IV trotz medikamentöser Therapie beziehungsweise bei einem Druckgradienten von > 50 mmHg in Ruhe oder nach Provokation [7].
Frühere therapeutische Ansätze mittels Herzschrittmachertherapie blieben erfolglos [7]. Bei der TASH wird durch Alkoholinjektion in einen koronaren Septumast mit Versorgungsgebiet eines Hypertrophieareals eine lokalisierte Myokardnekrose verursacht [6, 7]. Dadurch kann im chronischen Verlauf eine Myokardausdünnung erzielt werden [7]. Sowohl die chirurgische Myoektomie als auch die TASH sind nach bisherigen Erfahrungen gleichwertige therapeutische Verfahren [7].
Als Ultima ratio gilt eine Herztransplantation [7].
Prognostisch beträgt die jährliche Letalität circa 2 % bei allen HOCM-Patienten [10]. Bei symptomatischen Patienten besteht eine deutlich schlechtere Prognose, insbesondere bei zusätzlichem Vorliegen einer Herzinsuffizienz oder koexistentem Vorhofflimmern mit eventuellem Auftreten von thromboembolischen Ereignissen [11, 12], sodass in spezialisierten Zentren Letalitätsraten von 3 – 6 % in Risikokollektiven beschrieben werden.
Fallbeschreibung
Ein 44 Jahre alter Patient stellte sich 02/2013 in unserer Ambulanz vor zur Abklärung rezidivierender Herzrhythmusstörungen. Anamnestisch berichtete er über paroxysmales Vorhofflimmern in den vorherigen Jahren (bisher ohne Antikoagulation). In diesem Rahmen wären 2004 auch einmalig eine elektrische Kardioversion sowie eine Kardio-MRT erfolgt. Seither wäre keine kardiologische Diagnostik mehr durchgeführt worden. Die weitere Eigenanamnese war bis auf eine Ileusoperation unauffällig. Auf Nachfragen berichtete der Patient über einen plötzlichen Herztod des Vaters mit 32 Jahren aus ungeklärter Ursache.
Innerhalb der letzten sieben Monate habe der Patient nun erneut das Gefühl an Herzrhythmusstörungen zu leiden. Zeitgleich wäre es auch zu Beklemmungsgefühlen und Herzstichen gekommen. Des Weiteren berichtete er über einen Leistungsverlust und Schweißausbrüche unter Belastung sowie Dyspnoe (NYHA III). Inzwischen wäre die Symptomatik ein- bis zweimal täglich aufgetreten und er wäre überhaupt nicht mehr belastbar. So wäre Treppensteigen schon nicht mehr möglich gewesen. Er merkte auch jedes Mal, wenn „das Herz dann wieder in den richtigen Rhythmus“ zurückspringe.
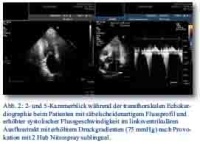
In der Aufnahmesituation war der Patient in Ruhe beschwerdefrei. Im Ruhe-EKG bestand ein Normalbefund. In der körperlichen Untersuchung imponierte jedoch ein 3/6-Systolikum mit punctum maximum über Erb bei echokardiographisch unauffälliger Klappenmorphologie. Der linke Ventrikel war normal dimensioniert, jedoch deutlich hypertrophiert (IVSd/PWd 13,2/12 mm) bei guter linksventrikulärer Funktion von circa 65 %. Dabei fand sich eine prominente Hypertrophie am basalen Septum, die sich in den oben genannten Standardmessungen nicht widerspiegelte (Abb. 1). Im linksventrikulären Ausflusstrakt war eine deutliche Flussbeschleunigung (Vmx über Aortenklappe 2,6 m/s, max. PG 28 mmHg, MPG 14 mmHg) messbar (Abb. 1). Nach Stimulation mit 2 Hub Nitrolingual (Wirkstoff: Glyceroltrinitrat) kam es zu einem massiven Anstieg des Druckgradienten auf > 75 mmHg mit SAM-Phänomen (Abb. 2). Somit ergab sich das echokardiographische Bild einer hypertroph-obstruktiven Kardiomyopathie (HOCM) ACC/ESC Grad 2 nach der hämodynamischen Klassifikation.
Nach intensiver Recherche ließ sich ein MRT-Befund des Patienten von 01/2005 finden. Dort lag bereits die Diagnose HOCM mit den entsprechenden Phänomenen vor. Kontrollen oder diagnostische und therapeutische Schritte waren damals aber nicht erfolgt. Wir ergänzten somit die Diagnostik zunächst durch ein Langzeit-EKG. Dort fielen monomorphe, nicht-anhaltende ventrikuläre Tachykardien auf, sodass wir sofort mit einer Betablockade begannen. Da der Patient in Anbetracht der Symptomatik und des plötzlichen Herztodes des Vaters als Hochrisikopatient einzustufen war, wurde sofort zur Prävention des plötzlichen Herztodes ein ICD implantiert. Zudem sahen wir die Indikation zur perkutanen Septumablation als gegeben an. Nach erneuter Indikationsprüfung und Ausschluss einer koronaren Herzerkrankung mittels Linksherzkatheteruntersuchung
erfolgte am 12.04.2013 komplikationslos die transkoronare
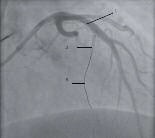
Ablation der Septumhypertrophie (TASH). Es wurden circa 1,5 – 2 ml 70 %-ige Alkohollösung in den 1. Septumast injiziert, der gegen den Ramus interventricularis anterior (RIVA) mit einem Ballon geblockt wurde, um eine iatrogene Nekrose zu erzielen (Abb. 3). Nach Beendigung der Rehabilitationsphase stellte sich der Patient am 16.05.2013 erneut in unserer Ambulanz zur Verlaufskontrolle vor. Inzwischen hatte sich der Befund bereits echokardiographisch deutlich verbessert und der Druckgradient im linksventrikulären Ausflusstrakt betrug nun 14 mmHg in Ruhe und 30 mmHg nach Provokation mit Nitrolingual. Eine engmaschige Verlaufskontrolle in unserer Ambulanz wird jedoch weiterhin notwendig sein, um das Langzeitergebnis der TASH zu überwachen und gegebenenfalls weitere therapeutische Maßnahmen durchzuführen. Eine dauerhafte Thrombembolieprophylaxe mit Xarelto wurde bereits eingeleitet.
Abb. 3: Herzkatheterunterdarstellung der transkoronaren Ablation der Septumhypertrophie (TASH) beim Patienten, 1 RIVA, 2 Ballon im 1. Septumast. 3. Draht im 1 Septumast
Diskussion
Die HOCM gilt als häufige Ursache des plötzlichen Herztodes, insbesondere bei jungen Leistungssportlern [2, 3, 4, 6, 7]. Durch die körperliche Belastung kommt es zu einer zunehmenden Obstruktion des linksventrikulären Ausflusstraktes, infolge dessen können maligne Herzrhythmusstörungen mit Todesfolge resultieren [6, 7]. So gibt es zahlreiche Beispiele von plötzlichen Todesfällen von vermeintlich gesunden Sportlern. Dies ist von besonderer wehrmedizinischer Relevanz aufgrund der körperlichen Belastung von Soldaten im In- und Ausland.
Im geschilderten Fall bestanden die Hauptrisikofaktoren (Tab. 1) in der positiven Familienanamnese (Vater mit mutmaßlichem plötzlichen Herztod) und der nachweisbaren nicht anhaltenden ventrikulären Tachykardie im Langzeit-EKG. Bereits bei Vorliegen eines Risikofaktors 1. Ranges wird die Implantation eines Defibrillators zur Primärprophylaxe des plötzlichen Herztodes von den Fachgesellschaften empfohlen [7, 9].
Mit der Anzahl der Risikofaktoren steigt auch das individuelle Risiko des Patienten. Eine Risikobewertung war bei diesem Patient jedoch bisher nicht erfolgt. Therapeutisch empfahlen wir dem Patienten einen Verzicht auf starke körperliche Belastung sowie ein Meiden von Kraftsport. Leichte sportliche Aktivitäten sind jedoch möglich. Auf eine ausreichende Flüssigkeitszufuhr sollte geachtet werden. Des Weiteren sind Vor- und Nachlast senkende Medikamente streng kontraindiziert.
Eine Verbesserung der Hämodynamik im Rahmen des iatrogen getriggerten Remoddelings am basalen Septum konnten wir bereits fünf Wochen nach der TASH echokardiographisch nachweisen. Die TASH wird in zahlreichen Studien der chirurgischen Myoektomie als gleichwertig angesehen und ist weniger invasiv, weswegen wir uns in Abstimmung mit dem Patienten dafür entschieden [7]. Risiken sind neben den üblichen Komplikationen eines Myokardinfarktes, insbesondere der Rückfluss des Alkohols in den RIVA, was einen großen Vorderwandinfarkt nach sich ziehen würde und unbedingt zu vermeiden ist.
Das beim Patienten aufgetretene Vorhofflimmern in der Vergangenheit ist möglicherweise als erster Hinweis auf diese strukturelle Herzerkrankung zu bewerten, was auch das MRT zeigte. Der Ileus in der Vorgeschichte des Patienten war möglicherweise auch thromboembolisch verursacht. Dies konnte jedoch anhand der Vorbefunde in der G-Akte nicht hinreichend geklärt werden. Insgesamt beträgt das Apoplex/Embolierisiko circa 0,8 %/Jahr und ist in 88 % der Fälle assoziiert mit Vorhofflimmern [12]. HOCM-Patienten haben zudem ein vierfach höheres Embolierisiko als Patienten mit hypertropher nicht obstruktiver Kardiomyopathie [13].
Dieses Beispiel zeigt, das die gravierende Diagnose bei einem „klassischen HOCM Patienten“ durchaus hätte früher erkannt werden können, wobei in diesem Fall glücklicherweise keine lebensbedrohlichen Komplikationen aufgetreten sind.
Schlussfolgerungen
Die HOCM ist ein wehrmedizinisch relevantes Krankheitsbild, das in der sanitätsdienstlichen Versorgung und sportmedizinischen Betreuung der Soldatinnen und Soldaten beachtet werden muss. Dieser Artikel soll Truppenärzte sensibilisieren, Patienten mit erhöhtem Risikopotenzial frühzeitig zu erkennen und im Zweifel großzügig in den Facharztabteilungen vorzustellen.
Bildquelle:
Abbildungen 1 und 2: Dr. Udo Schumann, Abteilung für Innere Medizin, Bundeswehrkrankenhaus Westerstede.
Abbildung 3: Herzkatheterdarstellung der TASH am Klinikum Oldenburg durchgeführt durch Dr. Udo Schumann, Abteilung für Innere Medizin, Bundeswehrkrankenhaus Westerstede.
Literatur
- Krüger-Brand, Heike E.: Sportmedizin: Register zum plötzlichen Herztod, Dtsch Ärztebl 2012; 109(18): 932.
- Kindermann W, Urhausen A: Plötzlicher Herztod beim Sport. Bundesinstitut für Sportwissenschaft, Köln 2000, 1 – 55.
- Douglas P, Zipes A, Camm J, et al.: Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death, Europace 2006; 8: 746 – 837.
- Tebbenjohanns J, Willems S, Antz M, Pfeiffer D, Seidl K-H, Lewalter T: ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death – executive summary , Der Kardiologe, Band 2, Nr. 5, Kardiologe 2008; 2: 363 – 388.
- Corrado D, Basso C, Rizzoli G, Schiavon M, Thiene G. Does sports activity enhance the risk of sudden death in adolescents and young adults? J Am Coll Cardiol. 2003; 42 (11): 1959 - 63.
- Renz-Polster H, Krautzig S, Basislehrbuch Innere Medizin, 4.Auflage, München, 2008; 132 – 135.
- Prinz C, Farr M, Hering D, Horstkotte D, Faber L: The diagnosis and treatment of hypertrophic cardiomyopathy. Dtsch Ärztebl Int 2011; 108 (13): 209 – 215.
- Maron BJ, Maron MS, Semsarian C.: Genetics of hypertrophic cardiomyopathy after 20 years: clinical perspectives. J Am Coll Cardiol. 2012; 60(8): 705 – 715.
- Jung W, Andresen D. Block M et al.: DSG Leitlinie zur Implantation von Defibrillatoren. Clin Res Cardiol 2006; 95 (12): 696 – 708.
- Roberts R, U Sigwart: Current concepts of the pathogenesis and treatment of hypertrophic cardiomyopathy. Circulation 2005; 112: 293 – 296.
- Takagi E, Yamakado T, Nakano T. et al.: Prognosis of completely asymptomatic adult patients with hypertrophic cardiomyopathy. J Am Coll Cardiol 1999; 33(1): 206 – 211.
- Maron BJ, Olivotto I, Bellone P et al: Clinical profile of stroke in 900 patients with hypertrophic cardiomyopathy. J Am Coll Cardiol 2002; 39(2): 301 – 307.
- Elliot PM, Gimeno JR, Tome MT. et al.: Left ventricular outflow tract obstruction and sudden death risk in patients with hypertrophic cardiomyopathy. Eur Heart J 2006; 27 (16): 1933 – 1941.
Datum: 25.06.2013
Quelle: Wehrmedizinische Monatsschrift 2013/5-6