Praktische Umsetzung von Antibiotic Stewardship (ABS) – ABS-Führerschein
Nach einem Vortrag bei der ARKOS-Tagung Hamburg, (Workshop: Mini ABS-Führerschein Bw)
Bedeutung von ABS
Die zunehmenden und sich weltweit ausbreitenden Antibiotikaresistenzen insbesondere bei den gramnegativen Erregern werden aktuell von den großen Gesundheitsorganisationen wie der World Health Organization (WHO) [1], den amerikanischen Centers for Disease Control and Prevention (CDC) [2] oder auch des European Center for Disease Prevention and Control (ECDC) [3] als eine der größten Herausforderungen für unsere Gesundheitssysteme angesehen. Daher hat das Thema nicht nur Eingang in die medizinische Fachwelt gefunden, sondern wird auch in der Laienpresse und der Politik zunehmend thematisiert. Um die Bedrohung zu verdeutlichen, wird die Anzahl der Toten durch Infektionen mit multiresistenten Erregern (MRE) mit den Todesfällen durch andere Ursachen verglichen: Das ECDC geht davon aus, dass europaweit jährlich 33 000 Menschen an derartigen Infektionen versterben – so viele wie an Influenza, Tuberkulose und HIV/ AIDS zusammen [4]. Der vielfach zitierte ONeill-Report geht aktuell von etwa 700 000 Toten weltweit aus, eine Zahl die bis 2050 noch auf etwa 10 000 000 Tote ansteigen könnte, so dass im Jahr 2050 mehr Menschen an einer Infektion mit MRE versterben könnten als an Krebs [5].
Der Sanitätsdienst der Bundeswehr ist auf dem Gebiet ABS schon seit 2014 engagiert: Beginnend am BwKrhs Berlin wurden ABS-Kommissionen in den Bw(Z)Krhs etabliert. Es folgte dann im Jahr 2017 die Gründung des Arbeitskreises Antiinfektiva, Resistenzen und Therapie (AK ART Bw) durch den Stellvertreter des Inspekteurs des Sanitätsdienstes und Kommandeur Gesundheitseinrichtungen.
Dieses Gremium setzt sich unter Leitung von Kdo SanDst VI 1 aus Vertretern der Konsiliargruppen und den Leitern der ABS-Kommissionen zusammen und initiiert bzw. setzt um ein basierend auf den einschlägigen Leitlinien „konzern-weites“ ABS-Programm. Erarbeitet wurden bereits verschiedene Handlungsempfehlungen wie ein Leitfaden zur perioperativen Antibiotikaprophylaxe (PAP), ein Leitfaden zur präemptiven Antibiotikatherapie der gefechtsassoziierten Verletzungen oder auch aktuell ein Leitfaden zur antibiotischen Therapie in der truppenärztlichen/ truppenzahnärztlichen Versorgung.
Diese und weitere Dokumente sind im WikiService Bw auf den Seiten des Hygienemanagements der Bundeswehr abzurufen. Hier finden sich auch die Kontaktdaten der Ansprechpartner für den AK ART.
Praktische Umsetzung im Alltag der medizinischen Versorgung
Antibiotic Stewardship kann nach aktuellen Leitlinien [6] eine Vielzahl von übergeordneten organisatorischen und strukturellen BMaßnahmen sowie zahlreiche Einzelmaßnahmen umfassen. Oft sind diese Empfehlungen für den Arbeitsalltag aber wenig hilfreich. Hier setzen die Empfehlungen des ABS-Führerscheins an, die einen praxisorientierten und prägnanten 10-Punkte Plan vorschlagen:
1. Garbage in, garbage out (GIGO) – achten Sie auf die richtige Präanalytik.
Die Hypothese aus der Informatik, dass ein qualitativ schlechtes Ergebnis erzielt wird, wenn ein Rechenprozess mit qualitativ schlechten Daten „gefüttert“ wird, gilt im übertragenen Sinn auch für die mikrobiologische Diagnostik. Relevant ist hier vor allem, kurze Transportzeiten des mikrobiologischen Untersuchungsmaterials sicherzustellen sowie möglichst detaillierte Angaben über Verdachtsdiagnose und aktuelle antiinfektive Therapien mitzuteilen. Dies liegt zu allererst in der Verantwortung des behandelnden Arztes.
2. Ein Sixpack ist für alle gut – entnehmen Sie immer 3 Blutkulturpaare von unterschiedlichen Entnahmeorten.
Untersuchungen belegen eine im Vergleich zur Entnahme von 2 Blutkulturpaaren um 8 % gesteigerte diagnostische Sensitivität [7]. Wichtig in diesem Zusammenhang ist die kontaminationsfreie Entnahme unter aseptischen Bedingungen, sobald der Verdacht auf eine systemische Infektion besteht.
3. Staphylococcus aureus in der Blutkultur ist keine Kontamination!
Eine Staphylococcus aureus-Bakteriämie ist eine komplikationsträchtige Erkrankung, die häufig unterschätzt und nicht aggressiv und lange genug behandelt wird. Auch deshalb geht sie mit einer hohen Letalität von bis zu 30 % einher. Wichtig sind die konsequente Fokussuche inkl. TEE und bildgebender Diagnostik sowie die Fokussanierung. Die intravenöse Antibiotikatherapie erfolgt üblicherweise mit Flucloxacillin oder Cefazolin, bei MRSA mit Vancmoycin oder Daptomycin.
4. Focus, Focus, Focus – eine gezielte antiinfektive Therapie ist immer besser als eine kalkulierte!
Daher sollte im Rahmen der Reevaluation 48 bis 72 Stunden nach begonnener Antibiotikabehandlung und bei Vorliegen der Ergebnisse/ Antibiogramme aus der Mikrobiologie eine Anpassung der antiinfektiven Therapie erfolgen. Oft kann dabei von einem initial breiten Wirkspektrum auf ein schmales und fokussiertes Spektrum umgestellt werden, was den Selektionsdruck und damit auch den Kollateralschaden reduzieren kann.
5. „I“ ist das neue „S“ im Antibiogramm: Erreger empfindlich bei erhöhter Dosierung des Medikaments!
Mit Beginn des Jahres 2019 trat eine neue Definition des „I“ im Antibiogramm in Kraft: Bei einer Resistenztestung nach den Kriterien des European Committee on Antimicrobial Susceptibility Testing (EUCAST) bedeutet „I“ nicht mehr „intermediär“, also „irgendwie nicht sicher wirksam“, sondern weist darauf hin, dass die getestete Substanz definitiv für die Therapie in Frage kommt, allerdings in einer erhöhten Dosierung („I“ steht für „increased exposure“). Hier ist das betreuende Labor in der Verantwortung, geeignete Dosierungsempfehlungen auf den Befunden anzugeben, damit es nicht zu Missverständnissen und einem vermehrten Gebrauch von Breitspektrumantibiotika kommt.
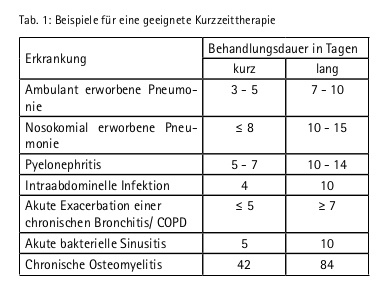
6. Shorter is better – die Antibiotika-Packung muss nicht leer werden!
Die 7-Tage Woche, wie wir sie heute kennen, wurde im Jahr 321 nach Christus durch Kaiser Konstantin eingeführt. Noch heute, im Zeitalter der evidenz-basierten Medizin, wird die Standardantibiotikatherapie für mindestens 7 Tage verabreicht, bei schweren Infektion auch oft für 14 Tage. Aktuelle Studienergebnisse belegen, dass bei einer Vielzahl von infektiösen Erkrankungen eine Kurzzeittherapie einer herkömmlichen „längeren“ Therapie nicht unterlegen ist [8].
7. Einmal ist besser als dreimal – verabreichen Sie eine PAP als Single Shot!
Eine perioperative Antibiotikaprophylaxe sollte 30 - 60 Minuten vor Schnitt in einer adäquaten Dosierung als Einmalgabe intravenös verabreicht werden. Nur bei einer langen OP-Dauer, die über die doppelte Halbwertzeit der gewählten Substanz hinausgeht (in der Regel nach 3 Stunden), oder bei hohem Blutverlust (> 1,5 l), sollte eine Wiederholungsdosis verabreicht werden. Auch an eine Gewichtsadaptation sollte gedacht werden: Bei der großen therapeutischen Breite der in der Regel eingesetzten Cephalosporine der 1. oder 2. Generation sollte ab einem Körpergewicht > 120 kg die doppelte Dosis verabreicht werden.
Hierzu hat der AK ART einen Leitfaden herausgegeben, der auf den o.g. Seiten des WikiService Bw abrufbar ist.
Bei einer manifesten Infektion oder einem nicht vollständig sanierten Fokus wird dagegen eine antiinfektive Therapie und keine Prophylaxe durchgeführt.
8. Es muss nicht immer ein Antibiotikum sein – erwägen Sie eine symptomatische Therapie!
Gerade Atemwegsinfekte stellen in der truppenärztlichen Praxis aber auch in den Notaufnahmen häufige Konsultationsgründe dar. Da sie sind in der Mehrzahl der Fälle (> 80 %) viral verursacht sind, sollte hier primär eine symptomatische Therapie verordnet und der Patient entsprechend aufgeklärt werden. Aber auch der unkomplizierte Harnwegsinfekt der jungen Frau kann in Absprache mit der Patientin rein symptomatisch behandelt werden [9]. Info-Flyer für Patienten finden sich zum Download auf den o.g. Seiten im WikiService Bw.
9. Der vergessene Rest bei der Kurzinfusion– verabreichen Sie die korrekte Dosis!
Ein Standard-Infusionssystem hat ein Volumen von ca. 12 ml, mit Verlängerungen und 3-Weg-Hahn vergrößert sich das Volumen weiter. Löst man ein Antibiotikum in 50 ml und spült das Restvolumen des Infusionssystems nicht nach, so werden 20 bis 25 % der geplanten Dosis des Antibiotikums nicht verabreicht. Aus der Hämato-Onkologie weiß man, dass es im Rahmen von Chemotherapien so zu Unterdosierungen mit unzureichender Wirkung kommen kann. Auch bei der intravenösen antiinfektiven Therapie sollte das Restvolumen daher berücksichtigt werden und mit geeigneten Infusionslösungen nachgespült werden, um den Behandlungserfolg nicht durch unbeabsichtigte Unterdosierung zu gefährden oder einer Resistenzentwicklung Vorschub zu leisten [10].
10. Es muss nicht immer i. v. sein – erwägen sie eine Oralisierung!
Auch um den Patienten vor den Infektions- und sonstigen Komplikationen eines Gefäßkatheters zu schützen, sollte nach Stabilisierung des Patienten im Rahmen einer wiederholten Evaluation erwogen werden, eine initial intravenös begonnene Therapie auf eine orale Therapie umzustellen.
Literatur beim Verfasser
Verfasser:
OFA Dr. Svenja Liebler, Kdo SanDst VI 1,
OFA Dr. Trixi Braasch und
FLA Dr. Martin Müller, BwKrhs Berlin
Kontakt-Email: [email protected]
Datum: 22.06.2020
Quelle: Wehrmedizin und Wehrpharmazie 1/2020