BIOMARKER ZUR ABSCHÄTZUNG VON STRAHLENSCHÄDEN
Biomarkers for Assessment of Radiation Damage
Aus dem Institut für Radiobiologie der Bundeswehr in Verbindung mit der Universität Ulm, München (Leiter: Oberstarzt Prof. Dr. med. V. Meineke)
Mark E. Hotz, Konrad Steinestel und Viktor Meineke
WMM, 58. Jahrgang (Ausgabe 5/2014, S. 166-169)
Zusammenfassung
Hintergrund: Die frühzeitige Kenntnis von Intensität und Ausmaß einer Strahlenexposition erlaubt eine vielfach wirksamere Behandlung. Im Rahmen eines Forschungsprojektes wird deshalb am Institut für Radiobiologie der Bundeswehr (InstRadBioBw) nach Biomarkern gesucht, deren Veränderungen sich reproduzierbar innerhalb der ersten 48 h nach einem lokalen oder systemischen Strahlenschaden im peripheren Blut nachweisen lassen.
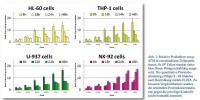
Methoden: An unterschiedlichen humanen permanenten Zelllinien (z. B. HL-60, THP-1, MonoMac-1, U-937) wurden strahleninduzierte Proteinveränderungen (z. B. bei Zytokinen, Wachstumsfaktoren, Zellzyklusproteinen sowie Proteinen zur Genregulation, Apoptose und DNA-Reparatur) untersucht. Der Einfluss von Röntgenstrahlung wurde zeitabhängig nach Bestrahlung (Röntgen 240kV, 1 Gy/min) durch Messung der Produktion verschiedener Zytokine und anderer Proteinmarker, wie z. B. ATM und ICAM-1, mittels sandwich-Enzyme-Linked Immunosorbent Assay (ELISA) und Western Blot Analyse gemessen.
Ergebnisse: Signifikante Effekte konnten unter anderem bei der strahleninduzierten Produktion der Proteine ICAM-1 und ATM beobachtet werden. Bei den untersuchten Zellpopulationen nahmen die Proteinmengen mindestens um das 2-fache zu.
Schlussfolgerungen: Die Identifikation und Charakterisierung von potenziellen Bioregulatoren kann die Vorhersage der Entstehung eines akuten Strahlensyndroms bereits zu einem frühen Zeitpunkt nach einem Strahlenereignis ermöglichen. Dies hilft entscheidend bei der Einleitung entsprechender Therapiemaßnahmen und kann ferner dazu beitragen, die vorhandenen Therapieoptionen für strahlenexponiertes Personal nachhaltig zu verbessern.
Schlagworte: Biomarker, strahleninduzierte Proteine, molekularer Strahlennachweis
Summary
Background: Early knowledge about intensity and dose of irradiation makes medical care much more effective. Therefore a research project is in progress at the Bundeswehr Institute of Radiobiology (InstRadBioBw) to determine which biomarkers can be rapidly and reproducibly detected in the peripheral blood within the first 48 hours after radiation event in order to predict the extent of local or systemic radiation damage.
Methods: Human permanent cell lines (e.g. HL-60, THP-1, MonoMac-1, U-937) were used as a model system for investigations on radiation-induced protein-shifts (e.g. cytokines, growth factors, cell-cycle and gene regulatory proteins, apoptosis and DNA repair enzyme proteins). To examine the effect of X-ray on these cells, the production of different cytokines and further protein markers (e.g. ATM and ICAM-1) were measured time-dependent after irradiation (240kV X-ray, 1 Gy/min) by sandwich-Enzyme-Linked Immunosorbent Assay (ELISA) or Western Blot analysis.
Results: Significant effects on the production of ICAM-1 adhesion protein and ATM could be observed. Screened cell populations showed a more than 2-fold increase of protein production levels.
Conclusions: Identification and characterization of potential bioregulators may assist to predict the development of a radiation syndrome at an early stage. This can support the initialization of a specific therapy and can lead to the enhancement of therapeutic options for irradiated personnel.
Keywords: biomarkers, radiation-induced proteins, molecular irradiation-proof
Einführung
Die meisten Strahlenschäden nach Exposition gegenüber ionisierender Strahlung oder nach Terroranschlägen, bei denen ein konventioneller Sprengsatz radioaktives Material (radiological dispersal device; RDD oder „schmutzige Bombe“) in der Umgebung freisetzt, sind heterogen und stellen für das behandelnde Personal eine besondere Herausforderung dar. Einerseits können bei diesen Szenarien sehr viele Personen auf einmal betroffen sein, andererseits können die Schweregrade der Verletzungen vielschichtig sein und von einer beträchtlichen Zahl „worried wells“ bis hin zu Patienten mit einem akuten Strahlensyndrom sowie konventionellen Verletzungen reichen. Medizinisches Personal, welches triagiert, muss in der Begutachtung und Behandlung von Patienten mit diesen Kombinationsschäden vor dem Hintergrund des akuten Strahlensyndroms hinreichend ausgebildet sein. Generell herrscht zu Unrecht immer noch die Meinung vor, dass (Strahlen-) Schäden lediglich symptomatisch behandelt werden. Dies liegt unter anderem daran, dass kausal orientierte Therapieansätze und hier vor allem evidenzbasierte Therapien bisher kaum zur Verfügung stehen [1, 2].
Abb. 1: Mitarbeiter der AG Proteomics des InstRadBioBw bei der Proteinaufbereitung und anschließenden quantitativen Proteinbestimmung.Klinische Symptome können als entscheidende Parameter der akuten Strahlenreaktion dafür genutzt werden, Auftreten, Intensität und Verlauf der Strahlenkrankheit abzuschätzen.
Ein entsprechendes System, welches 24 „indicators of effect“ für die Bewertung der Schwere eines Strahlenschadens nutzt, ist das METREPOL („Medical Treatment Protocols for radiation accident victims“- Konzept [3]. Seit 2007 wurde an der Universität Ulm weiterhin ein Curriculum entwickelt und in ein Trainingsprogramm umgesetzt, welches Inhalte wie Radiobiologie, Diagnose und Management von Strahlenunfallpatienten, das akute Strahlensyndrom, die medizinische Versorgung sowie die Verwendung der biologischen Dosimetrie vermittelt [4].
Am InstRadBioBw sind eine Reihe von strahlen- und molekularbiologischen Verfahren zur Abschätzung von Strahlenschäden auf den verschiedenen Ebenen der biologischen Organisation von der Einzelzelle über den Gewebeverband bis hin zum Gesamtorganismus etabliert (Tabelle 1). Diese Verfahren werden ständig optimiert und weiterentwickelt, um eine möglichst frühzeitige und genaue Abschätzung zu ermöglichen. Obwohl die dizentrische Chromosomenanalyse den Goldstandard der biologischen Dosimetrie darstellt, ist diese eine zeitaufwendige und laborintensive Methode mit besonderen Einschränkungen [5].
Einen Schwerpunkt der aktuellen Arbeit des Institutes stellt die Überprüfung der Verwendbarkeit biologischer Indikatoren für zertifizierte Verfahren einer in vivo durchführbaren Spezialdiagnostik dar. Auf dem Weg dorthin wird gegenwärtig ein Forschungsprojekt bearbeitet, welches den Einsatz von verschiedenen Proteinmarkern des peripheren Blutes dahingehend überprüft, ob diese eine frühe Antwort auf eine Strahlenexposition vermitteln. Wäre dies machbar, könnte auf dieser Basis ein nicht-invasiver, feldtauglicher Schnelltest entwickelt werden.
Frühere Studien haben gezeigt, dass eine Ganzkörperexposition die Hämatopoese in Abhängigkeit der Strahlendosis, Dosisrate und Strahlenqualität nachhaltig beeinträchtigt. Das entstehende sog. Hämatopoetische Strahlensyndrom hat einen wesentlichen Anteil am strahleninduzierten Multiorganversagen [6]. Ebenso ist im Zusammenhang mit dem hämatopoetischen Syndrom eine Reihe von klinischen Parametern gut charakterisiert, wie z. B. Lymphozyten, Granulozyten und Thrombozyten. Deren klinische Charakteristik ebenso wie die klinischen Symptome sind für den Behandlungsverlauf essenziell [3]. Somit sind Serumproteine, die die Proliferation dieser Zellpopulationen beeinflussen, ebenso wie Proteine, die auf Entzündungsreaktionen in Folge eines Strahlenereignisses hinweisen, aber auch induzierte DNA-Reparaturenzyme als Reaktion auf einen Strahlenschaden an der DNA potenzielle Biomarker mit Signalfunktion für ionisierende Strahlung. Dass die Zytokinproduktion durch den Einfluss ionisierender Strahlung signifikant erhöht wird, ist bereits bekannt [7]. Weitere Arbeiten deuten darauf hin, dass ionisierende Strahlung einen modulierenden Effekt auf eine Reihe von Proteinen hat, die potenziell für die Früherkennung und zur Entwicklung eines Schnelltestes geeignet sein können [8].
Methoden
Die Untersuchungen wurden in vitro an Zellkulturen folgender Zelllinien durchgeführt: HL-60 (myeloische Leukämiezelllinie mit promyelozytärer Differenzierung), THP-1, MM-1 (myeloische Leukämiezelllinien mit monozytärer Differenzierung), U-937 (histiozytische Lymphomzelllinie mit makrophagenartiger Differenzierung), NK-92 (Natürliche Killer Lymphomzelllinie) und YT (T/NK Leukämiezelllinie). Der Effekt potenzieller Proteinkandidaten wurde an frisch isolierten peripheren mononukleären Blutlymphozyten überprüft. Dazu wurden die jeweiligen Zellpopulationen mit Röntgenstrahlung (240kV, 1 Gy/min) dosis- und zeitvariabel bestrahlt. Der Nachweis der Proteine erfolgte mittels der Immunoassay-Verfahren ELISA bzw. Western-Blot-Analyse aus den Zellkulturüberständen, Zelllysaten oder aus dem Blutplasma mittels spezifischer Antikörper. Das ELISA-Verfahren wurde nach der sandwich-Methode durchgeführt. Dabei bindet der spezifische Antikörper an das entsprechende Antigen (Markerprotein). Dieser Antikörper ist zugleich mit einem niedermolekularen Enzym kovalent verbunden. Eine Antigen-Antikörper-Bindung kann indirekt dadurch sichtbar gemacht werden, dass die gekoppelten Enzyme aus einem farblosen Chromogen ein farbiges Reaktionsprodukt liefern, welches photometrisch bestimmt werden kann. Bei der Western-Blot-Analyse werden die Gesamtproteine in einem Detergens-haltigen Puffer gelelektrophoretisch in Abhängigkeit ihrer molaren Masse aufgetrennt, auf eine Nitrozellulose-Membran übertragen und dort einer Nachweisreaktion unterzogen.
Erste Ergebnisse
Bisher wurden insgesamt 21 Proteinmarker auf modulierende Effekte nach Röntgenbestrahlung untersucht. Dabei konnten Unterschiede in der zeitlichen Abhängigkeit oder in Abhängigkeit der Dosis genauso wenig ignoriert werden wie Unterschiede zwischen den untersuchten Zellpopulationen. Bei neun Proteinmarkern ließen sich in mehreren Versuchen (n=3) reproduzierbare Ergebnisse erzielen, mit denen signifikante Effekte
(p < 0,05) zeit- (8 - 48 Stunden nach Bestrahlung) bzw. dosisabhängig (20 cGy - 10 Gy) bei mindestens einer Zellpopulation nachgewiesen werden konnten. Aufgrund der Fülle der Daten werden in diesem Artikel exemplarisch Ergebnisse für das Protein ATM und ICAM-1 dargestellt.
Ataxia Telangiectasia Mutated (ATM) Kinase
Verschiedene zelluläre Signaltransduktionswege werden durch ionisierende Strahlung aktiviert. Unter allen Signalproteinen ist die Kinase Ataxia Telangiectasia Mutated (ATM) der wichtigste Sensor für DNA-Schäden. Die schwerste Form der DNA-Schäden ist der Doppelstrangbruch (DSB; double-strand break) des DNA-Moleküls. Die ersten molekularen Ereignisse, die auf einen Doppelstrangbruch hindeuten, sind die Phosphorylierung des Histons H2AX. Diese Phosphorylierung kommt zustande, weil die strahleninduzierten Veränderungen des Chromatins die Phosphorylierung des Proteins ATM zur Folge haben. Phosphoryliertes ATM (phospho-ATM; p-ATM) wiederum vermittelt downstream die Phosphorylierung von H2AX, wobei die Phosphatgruppe des ATM auf das H2AX-Protein übertragen wird. In der Literatur wird ATM folglich auch als hypersensitiv gegenüber ionisierender Strahlung beschrieben [9]. Die schnelle Hochregulierung der ATM- Kinaseaktivität bzw. die Vermittlung dieser molekularen Phosphorylierungsreaktionen sind typisch für strahleninduzierte DNA-Schäden und Voraussetzung für Downstream-Veränderungen bei der Zellzykluskontrolle oder anderen molekularen Prozessen der Signaltransduktion. Erste Ergebnisse zeigen, dass es Unterschiede bei der Produktion von ATM in den verschiedenen Zelllinien gibt. So produzierten HL-60, THP-1 und U-937 Zellen bei Dosen oberhalb von 0,6 Gy mehr als die 10 - fache Menge p-ATM bereits nach acht Stunden, während die späteren Messungen (>8 Stunden) zwar erhöhte p-ATM-Konzentrationen nachwiesen, jedoch nicht über die 10 - fache Menge hinaus. Bei U-937 Zellen konnte zudem gezeigt werden, dass bei diesen späteren Messungen (>8 Stunden) der Zeitpunkt der Messung irrelevant ist und ein schwacher Dosiseffekt vorhanden ist. Anders als bei den Zelllinien HL-60, THP-1 und U-937, welche myeloischen Ursprungs sind, zeigten „lymphatisch gereifte“ NK-92 Zellen einen späten Effekt bei der p-ATM-Produktion (≥24 Stunden). Dieser Effekt wurde zudem durch höhere Dosen verstärkt. Im Vergleich dazu konnte ein dosisabhängiger Effekt bei HL-60 Zellen 48 Stunden nach Bestrahlung nicht mehr festgestellt werden. Insgesamt konnten bei diesen gezeigten Zelllinien hohe Proteinkonzentrationen, teilweise 15-fach über dem Hintergrund, bei einer Dosis von 1 Gy gemessen werden und damit starke Strahleneffekte verdeutlicht werden.
Intercellular Adhesion Molecule 1 (ICAM-1)
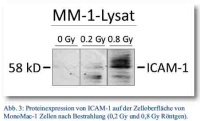
Das Intercellular Adhesion Molecule 1 (ICAM-1) oder auch als CD54 bezeichnet, wird grundsätzlich nur schwach auf Leukozyten, epithelialen Endothelzellen und anderen Zelltypen exprimiert. Diese Expression kann jedoch durch immunogene Substanzen stimuliert werden, wie IFN-g, TNF-a, IL-1b und Lipopolysaccharid. Die lösliche Form des ICAM-1 kann dabei infolge einer zerstörten Zelloberfläche auch im Serum vorkommen. Mit Hilfe der Western Blot-Analyse konnte gezeigt werden, dass bei bestrahlten MonoMac-1 Zellen 24 Stunden nach Bestrahlung dosisabhängig ICAM-1 auf der Oberfläche dieser monozytären Leukämiezellen exprimiert wird.
Während bei einer Dosis von 0,2 Gy eine nur sehr schwache Proteinbande bei 58 kD detektiert werden konnte, führten 0,8 Gy Röntgenbestrahlung zu einem signifikanten Signal und damit zu einer deutlichen Strahlenantwort.
Diskussion
Ziel dieser Arbeit war es, zunächst in vitro zu überprüfen bzw. die Frage zu stellen, ob die oben beschriebenen Proteinmethoden biodosimetrisch zur Anwendung kommen und dem triagierenden Arzt einen Hinweis auf sich entwickelnde Strahlenschäden geben können. Diese Frage konnte positiv beantwortet werden. In einem nächsten Schritt werden diese Ergebnisse nun auf die in vivo Situation übertragen.
Bei den Untersuchungen zum p-ATM konnte gezeigt werden, dass dieses Signalprotein schnell durch Bestrahlung induziert wird und sich signifikante Mengen nachweisen lassen, auch wenn diese populationsbedingt schwanken. Aufgrund der auch beim ICAM-1 beobachteten Effekte erscheinen diese Protein-basierten Nachweismethoden für Anwendungen im Rahmen der Biodosimetrie als sehr geeignet, zumal deren Nachweis weder kosten- noch zeitintensiv ist. Mit Hilfe einer feldtauglichen Variante erhielte der triagierende Arzt ein zusätzliches Werkzeug, um schnell zwischen „worried wells“ und „potenziell bestrahlten“ Patienten unterscheiden zu können. Bei letzteren könnte eine notwendige Therapie dann umgehend eingeleitet werden.
Aufgrund der Tatsache, dass die meisten der untersuchten Proteine im Körper nicht ausschließlich nach Strahlenereignissen exprimiert werden, erscheint es notwendig, dass ausgewählte Proteine zu einem in sich geschlossenen Bündel, einem sog. Cluster, vereint werden. Hierfür sind weiterführende Untersuchungen essenziell. Zudem steht außer Frage, dass eine Übertragbarkeit dieses in vitro Modells auf ein in vivo Modell gründlich geprüft werden muss.
Schlussfolgerungen
Der vorliegende Artikel verdeutlicht, dass effiziente molekularbiologische Protein-Nachweismethoden vorhanden sind, in vitro mindestens eine semi-quantitative Aussage über ein potenzielles Strahlenereignis zu treffen. Ein Cluster von neun Markern, die sowohl zeitliche wie auch Dosiseffekte abbilden können, erscheint realistisch. Neben der Suche nach weiteren potenziellen Proteinkandidaten stellt die Wahl des geeigneten in vivo Systems die nächste Herausforderung dar. Denkbar erscheint die Überprüfung der vorliegenden Ergebnisse mittels bestrahlten chimären NOD-SCID-Mäusen sowie Seren von Patienten nach Radiojodtherapie.
Literatur
- Dainiak N, Gent RN, Carr Z, Schneider R, Bader J, Buglova E, Chao N, Coleman CN, Ganser A, Gorin C, Hauer-Jensen M, Huff LA, Lillis-Hearne P, Maekawa K, Nemhauser J, Powles R, Schünemann H, Shapiro A, Stenke L, Valverde N, Weinstock D, White D, Albanese J, Meineke V: Literature review and global consensus on management of acute radiation syndrome affecting nonhematopoietic organ systems. Disaster Med Public Health Prep 2011. 5(3): 183-201.
- Dainiak N, Gent RN, Carr Z, Schneider R, Bader J, Buglova E, Chao N, Coleman CN, Ganser A, Gorin C, Hauer-Jensen M, Huff LA, Lillis-Hearne P, Maekawa K, Nemhauser J, Powles R, Schünemann H, Shapiro A, Stenke L, Valverde N, Weinstock D, White D, Albanese J, Meineke V: First global consensus for evidence-based management of the hematopoietic syndrome resulting from exposure to ionizing radiation. Disaster Med Public Health Prep 2011. 5(3): 202-212.
- Fliedner TM, Friesecke I, Beyrer K (eds): Medical Management of Radiation Accidents – Manual on the Acute Radiation Syndrome (METREPOL European Commission concerted action). London: British Institute of Radiobiology 2001.
- Hotz ME, Fliedner TM, Meineke V: Radiation accident preparedness: a European approach to train physicians to manage mass radiation casualties. Health Phys 2010. 98(6): 894-897.
- Beinke C, Braselmann H, Meineke V: Establishment of an x-ray standard calibration curve by conventional dicentric analysis as prerequisite for accurate radiation dose assessment. Health Phys 2010. 98(2): 261-268.
- Fliedner TM, Dörr H, Meineke V: Multi-organ involvement as a pathogenetic principle of the radiation syndromes: a study involving 110 case histories documented in SEARCH and classified as the bases of haematopoietic indicators of effect. Br J Radiol [Suppl] 2005. 27: 1-8.
- Daniak N: Hematologic consequences of exposure to ionizing radiation. Exp Hematol 2002. 30: 513-258.
- Marchetti F, Coleman MA, Jones IM, Wyrobek AJ: Candidate protein biodosimeters of human exposure to ionizing radiation. International Journal of Radiation Biology 2006. 82(9): 605-639.
- Paules RS, Innes CL, Sieber SO, Shackelford RE, Heinloth AN, Deming PB, Cistulli CA, Bennett L, Bushel PR, Afshari CA, Kaufmann WK: ATM is characterized by hypersensitivity. Nature Genetics (2001). 27(78): doi:10.1038/87240.
Bildquelle: Dr. Hotz, Institut für Radiobiologie der Bundeswehr
Datum: 08.07.2014
Quelle: Wehrmedizinische Monatsschrift 2014/5