Einsatz von Nahrungsmitteln und Nahrungssupplementen bei alkylanzien-induzierten Hautschäden
Use of nutrients and supplements for alkylating agent-induced skin damage
Robert Giesche*, Tanja Popp*, Annette Schmidt*, Horst Thiermann*, Dirk Steinritz*
Zusammenfassung
Einleitung: Schwefellost (S-Lost) ist eine hochtoxische, alkylierende Verbindung, die erstmals im Ersten Weltkrieg eingesetzt wurde. Nach Kontakt mit S-Lost treten nach einer klinischen Latenzzeit von bis zu 24 Stunden charakteristische Symptome an Haut, Augen, Lunge und inneren Organen auf. Kutane Anzeichen sind Erytheme, Inflammation, Blasenbildung und Ulzerationen der betroffenen Hautareale. Auch Halblost (CEES) und Chlorambucil besitzen eine vergleichbare hautschädigende Wirkung. Bis heute existiert kein Antidot zur Therapie von S-Lost-induzierten Schäden. In dieser Arbeit wurden mögliche protektive Eigenschaften von Nahrungsmitteln und Supplementen auf alkylanzien--induzierte Zellschäden in vitro untersucht.
Material/Methoden: Humane Keratinozyten (HaCaT) dienten als Surrogatmodell für die menschliche Haut. Nach einer Vorinkubation der HaCaT mit den zu untersuchenden Testsubstanzen Natrium-Ascorbylphosphat, Bromelain, Ginkgo, Vitamin D3, α-Linolensäure und Docosahexaensäure für 2 oder 24 Stunden erfolgte eine Exposition mit den Alkylanzien S-Lost, CEES und Chlorambucil.
Ergebnisse: Bei Ginkgo, Vitamin D3 und Docosahexaensäure konnte eine Erhöhung der Zellviabilität im Vergleich zu einer mit Chlorambucil oder S-Lost-vergifteten, unbehandelten Kontrolle festgestellt werden. Weiterhin wurde der Einfluss der Testsubstanzen auf S-Lost--induzierte Veränderungen in wichtigen zellulären Signalwegen untersucht. Es zeigte sich, dass Ginkgo, Vitamin D3 und Docosahexaensäure eine anti-apoptotische Wirkung auf S-Lost-exponierte Zellen aufwiesen.
Diskussion und Ausblick: Die Ergebnisse der in vitro Versuche zeigten protektive Eigenschaften von -Ginkgo und Vitamin D3 bei S-Lost-induzierten Zellschäden. Diese könnten potenziell auch in vivo vorhanden sein, was Chancen auf die Entwicklung nebenwirkungsarmer Protektiva eröffnet. Mit der, im Rahmen dieser Arbeit etablierten, Screening-Methode kann zukünftig eine effektive Untersuchung, der möglichen protektiven Wirkung von Nahrungsmitteln und Supplementen auf eine Alkylanzien-induzierte Zelltoxizität, erfolgen.
Schlüsselworte: S-Lost, Alkylanzien, Apoptose, Ginkgo, Vitamin D3
Summary
Introduction: The chemical warfare agent sulfur mustard (SM) is a highly toxic alkylating agent, which was first used in World War I. After exposure, symptoms related to skin, eye and lung damage develop after a characteristic symptom-free period of several hours. Erythema, inflammation, blistering and ulceration are observed in the affected skin areas. The same effect can be observed for other alkylating compounds like the nitrogen mustard chlorambucil and the monofunctio-nal SM analogue CEES. Currently, there is no antidote available.
In this study, potentially protective effects of nutrients and supplements on alkylating agent-induced cytotoxi-city was investigated in vitro.
Material/Methods: Human keratinocytes (HaCaT), a surrogate model for human skin, were pretreated 2 or 24 hours with the substances of interest: sodium ascorbic phosphate, bromelain, ginkgo, cholecalciferol (vitamin D3), α-linolenic acid und docosahexaenoic acid. Afterwards, cells were exposed to the different alkylating agents.
Results: Ginkgo extract, vitamin D3 and docosahex-aenoic acid treatment increased cell viability compared to chlorambucil- or SM-exposed sham-treated controls. To elucidate the molecular toxicology of alkylating agents in more detail, various cellular signaling pathways were investigated. Ginkgo, vitamin D3 and docosahexaenoic acid exhibited antiapoptotic effects on exposed cells.
Discusssion and perspective: Our results revealed that these substances may have a benefit in SM-induced cell damage. This may also hold true in vivo, thus paving the road for the development of protective drugs with few side effects. The screening-method, which has been established within this study, will allow effective testing of nutrients and supplements regarding their protective effects on alkalyting agents induced cytotoxicity.
Keywords: Sulfur mustard, alkylating agent, apoptosis, ginkgo, vitamin D3
Einleitung
Die Gefahr eines Einsatzes von S-Lost, vor allem durch terroristische Organisationen im Rahmen asymmetrischer Bedrohungsszenarien, hat signifikant zugenommen. Dies wird durch die forensisch nachgewiesene Verwendung von S-Lost 2013 in Syrien und 2015 im Irak unterstrichen [18, 20]. Derzeit steht bei einer Exposition mit dem Hautkampfstoff oder mit ähnlich wirkenden alkylierenden Substanzen keine spezifische Behandlung zur Verfügung. Es fehlt ein wirksames Antidot. Adjuvantiv einsetzbare Substanzen sind bisher ebenfalls nicht verfügbar.
Klinik und Folgen der Lostvergiftung
Der erste Kontakt mit dem Kampfstoff verläuft klinisch inapparent [26]. Erst nach einer Latenzzeit von mehreren Stunden sind Anzeichen einer Exposition mit S-Lost zu erkennen. Dabei sind die am stärksten betroffenen Organe das Auge, die Haut und der Respirationstrakt [3]. Typische kutane Anzeichen sind Erytheme, Inflammation, Blasenbildung und Ulzerationen der betroffenen Hautareale [3]. Pigmentierungsstörungen (sowohl Hyper- als auch Hypopigmentierung) treten ebenfalls regelmäßig auf. Eine Langzeithospitalisierung betroffener Patientinnen und Patienten über Wochen und Monate aufgrund der Hautschäden ist oftmals erforderlich. Eine S-Lost--Exposition kann zu verschiedenen Langzeitfolgen führen. Selbst 15 bis 20 Jahre nach einer einmaligen Exposition kann eine Erblindung (sog. „Mustard Gas Keratopathy“) auftreten [4]. Nach inhalativer Aufnahme kann sich als Sonderform einer chronisch obstruktiven pulmonalen Erkrankung die sogenannte „Mustard Lung“ ausbilden [3]. S-Lost besitzt zudem eine kanzerogene Wirkung. So wurde ein erhöhtes Risiko für Lungenkrebs bei Fabrikarbeitern festgestellt, welche über einen längeren Zeitraum subakut toxischen Dosen von S-Lost ausgesetzt waren [3, 21].
Molekulare Toxikologie von S-Lost
Die molekulare Toxikologie von S-Lost ist komplex. Der Kampfstoff ist eine hochreaktive chemische Verbindung, die im menschlichen Körper eine Vielzahl von Reaktionen eingehen kann. Nach der Bildung eines heterocyclischen Sulfoniumions reagiert es mit Kohlenhydraten, Proteinen, Phospholipiden sowie Nukleinsäuren [4, 14]. Bedingt durch die zwei Chlorethylketten handelt es sich um ein bifunktionales Molekül. Entstehende Quervernetzungen erhöhen die schädigende Wirkung.
Die Alkylierung der DNS ist u. a. ein Auslöser von Apoptose und Nekrose sowie des Zellzyklusarrests einer exponierten Zelle [13]. Zusätzlich kommt es zur Bildung von reaktiven Sauerstoffspezies (ROS) und somit zu -oxidativem Stress. Zudem wird ein Anstieg der intrazellulären Calcium-Konzentration sowie eine Ent-zündungs-reaktion induziert. Letztere ist durch einen Anstieg von pro-inflammatorischen Interleukinen (z. B. IL-1α, -1ß, -6, -8), Leukotrien B4 und Tumornekrosefaktor α (TNFα) gekennzeichnet [22].
Nahrungsmittel und Supplemente als Protektoren?
Für eine Reihe von Nahrungsmitteln und Supplementen wurden ROS-protektive und anti-inflammatorische Eigenschaften beschrieben. Es sollte deshalb in dieser Arbeit untersucht werden, ob diese in vitro die zytotoxische Wirkung von S-Lost reduzieren können. Dabei -wurden die zu untersuchenden Zellen mit den Nahrungsmitteln oder Supplementen vorbehandelt und an-schlie-ßend mit S-Lost exponiert. Die zu untersuchenden Substanzen wurden anhand ihrer ROS-protektiven Effekte oder antientzündlichen Wirkung identifiziert. Folgende Stoffe wurden für die Studie ausgewählt:
- Natrium-Ascorbylphosphat (NAP), ein phosphatiertes Derivat des Vitamin C, wurde auf Grund seines in der Literatur beschriebenen antioxidativen Effektes gewählt. Vitamin C und seine Derivate reagieren unter Bildung von Dehydroascorbinsäure direkt mit freiem ROS und fungieren somit als ROS-Scavenger [9]. Die phosphatierte Form des Vitamins zeigt, beispielsweise als Magnesium-Ascorbylphosphat, deutlich protektive Effekte vor UV-Strahlung in Keratinozyten in vitro
[12, 17]. - Bei Bromelain handelt es sich um Cystein-Proteasen, Peroxidasen und Phosphatasen der Pflanzenfamilie der Bromeliaceae [27, 1]. Die Enzyme sind in der Lage, zellschädliche freie Radikale und insbesondere ROS zu reduzieren [27]. Zusätzlich wird eine anti-inflammatorische Wirkung von Bromelain beschrieben [2].
- Ein Ginkgo-Extrakt (im Folgenden Ginkgo) wurde als weitere Substanz getestet, da für alle Inhaltsstoffe des Extrakts, bis auf Ginkgolsäure, antioxidative und anti-inflammatorische Wirkungen beschrieben werden [25].
- Vitamin D3 wird eine anti-inflammatorische Wirkung zugeschrieben, da es den intrazellulären Vitamin-D-Rezeptor (VDR) bindet, in den Zellkern transloziert und dort die Genexpression beeinflusst. So wird unter anderem die Bildung der Cyclooxigenase-2 gesenkt, was eine Entzündungsreaktion reduzieren kann [15].
- Als letzte Substanzen wurden die zwei essentiellen Omega-3-Fettsäuren α-Linolensäure (ALA) und Docosa-hexaensäure (DHA) verwendet, da sie oxidativen Stress reduzieren können [10]. Zusätzlich konnte für ALA ein positiver Effekt auf die Proliferationsrate von Stammzellen beschrieben werden [24]. DHA zeigte in einer klinischen Studie anti-inflammatorische Effekte [7]. Es wurde vermutet, dass die beschriebenen -Wirkungen den S-Lost-Pathomechanismus positiv - beeinflussen und somit Zellschäden reduzieren könnten.
Studienziel
Ziel der Arbeit war die Untersuchung möglicher protektiver Effekte der beschriebenen Nahrungsmittel und Supplemente auf S-Lost-induzierte Zellschäden. Dabei standen die S-Lost-induzierte ROS-Erhöhung sowie die entstehende Entzündungsreaktion im Vordergrund. Zusätzlich wurde die Apoptose als Endpunkt beider Pathomechanismen durch entsprechende Proteinanalytik untersucht. Um die möglichen protektiven Effekte zu bewerten und zu beschreiben, wurden die Untersuchungen um zwei weitere Alkylanzien (das monofunktionelle S-Lost Analogon Halblost (CEES) und das Stickstofflostzytostatikum Chlorambucil) ergänzt.
Aufgrund des Fehlens eines geeigneten Antidots gegen S-Lost oder andere Alkylanzien wäre eine Reduktion der Hautschäden oder anderer klinischer Parameter durch den Einsatz von Nahrungsmitteln oder Supplementen von erheblichem Nutzen. Sie könnten, einen klinischen Benefit vorausgesetzt, im Sinne einer gut verträglichen Präventivmaßnahme prophylaktisch supplementiert werden. Zwar war es von Anfang an wenig wahrscheinlich, dass die untersuchten Substanzen schon bestehende Therapieoptionen ersetzen können; sie könnten jedoch therapieunterstützend wirken und die Hospitalisierung oder Behandlungsdauer der betroffenen Patientinnen und Patienten möglicherweise verkürzen. Darüber hinaus könnten die Substanzen einen protektiven Einfluss auf noch nicht geschädigte Zellen haben, um so eine Ausbreitung der S-Lost-Wirkung im Gewebe zu verringern. Im Vordergrund der Untersuchungen stand die Identifizierung möglicher S-Lost protektiver Substanzen, welche das Potenzial besitzen, als sinnvolles Adjuvans zu bestehenden Therapien verwendet werden zu können.
Material und Methoden
Für die Etablierung eines adäquaten Modellsystems diente eine humane Keratinozytenzelllinie (HaCaT). Diese wurde unter Standardbedingungen bei 37 °C und 5 % CO2 in Dulbecco’s Modified Eagle Medium (DMEM) mit 5 %igem fetalem Kälberserum (FKS) kultiviert. Ernte und erneute Aussaat der Zellen erfolgten alle 3 bis 4 Tage.Zu Beginn der Arbeit wurde die Zellzahl für das gewählte Testsystem optimiert. Anschließend konnte mit dem Testsystem die Verträglichkeit (Toxizitätsbestimmungen, Ermittlung der LC50) der zu untersuchenden Nahrungsmittel, Supplemente und Alkylanzien bestimmt werden. Die Ermittlung des Endpunkts der Zellzahloptimierung sowie die Verträglichkeitsuntersuchungen erfolgten über die Messung der Zellviabilität mittels eines modifizierten Tetrazoliumtests (XTT-Assay; Cell Proliferation Kit II XTT von Roche® Apllied Life Science). Die Grundlage eines Tetrazoliumtests basiert auf der enzymatischen Reduktion eines Tetrazols in ein Formazan, welches anschließend photometrisch bestimmt werden kann. Dieses setzt einen funktionellen mitochondrialen Metabolismus der Zellen voraus. Die Zellviabilität ist ein Surrogatmarker für die Vitalität einer Zelle und beschreibt den Anteil von lebensfähigen Zellen innerhalb einer Population. Dabei wird das Tetrazol von zelleigenen Enzymen reduziert und der entstandene Komplex photometrisch gemessen. Je mehr Zellen lebensfähig sind, desto höher ist die gemessene Absorption.
Zur Bestimmung der Zytotoxizität der Alkylanzien wurden Dosis-Wirkungs-Kurven erstellt. Dazu wurden unter Standardbedingungen kultivierte (siehe oben) HaCaTs mit absteigenden Konzentrationen der zu untersuchenden Gifte für 24 h inkubiert. Anschließend wurde ein XTT--Assay durchgeführt, um die Zellviabilität der inkubierten HaCaTs zu bestimmen. Anhand der somit erhaltenen Dosis-Wirkungs-Kurven konnte die LC50-Konzentration für S-Lost (25,3 µM), CEES (4090 µM) und Chlorambucil (786,8 µM) ermittelt werden. Die LC50-Konzentrationen waren der Ausgangspunkt für die Festlegung der im Testsystem verwendeten Alkylanzien-Dosis. Basierend auf den Ergebnissen wurden drei Alkylanzien-Konzentrationen ausgewählt. Dabei waren die sinnvoll gerundeten LC50-Konzentrationen bei CEES (4000 µM) und Chlorambucil (800 µM) die höchste verwendete Dosis dieser Alkylanzien. Zusätzlich wurden die LC25- und LC10-Konzentrationen untersucht (Chlorambucil 675 und 725 µM; CEES 2800 und 3300 µM), um mögliche Effekte bei niedrigeren Expositionsdosen ermitteln zu können. Bei S-Lost wurde die Entscheidung zu einer anderen Einteilung getroffen, da in den weiterführenden Versuchen bei den initial eingesetzten Konzentrationen nur geringe Effekte im Vergleich zur Kontrolle festgestellt werden konnten. Es war daher nötig, die Konzentration – von der LC50-Konzentration ausgehend – zu verdoppeln. Für die weiteren Versuche wurden somit Konzentrationen von 25, 50 und 100 µM S-Lost verwendet.
Zusätzlich wurde die Verträglichkeit (Toxizität) der eingesetzten Nahrungsmittel und Supplemente getestet. Aus Dosis-Wirkungs-Kurven wurden über die jeweiligen LC50-Werte die Konzentrationen ermittelt, welche keinen schädlichen Einfluss auf die verwendeten HaCaT aufwiesen.
Als höchste jeweils nichttoxische Konzentration ergaben sich folgende Konzentrationen für
- NAP 10 mM,
- Vitamin D3 20 µm,
- ALA und DHA jeweils 50 µM,
- Bromelain[1] 15 µg/ml und für
- Ginkgo 1 600 µg/ml.
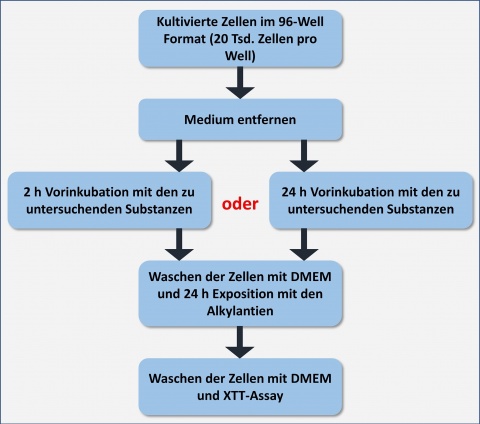
Das weitere Vorgehen zur Ermittlung des Einflusses von Nahrungsmitteln und Supplementen bei alkylanzien-induzierten Hautschäden wird in Abbildung 1 dargestellt. Um mögliche akute protektive Effekte von Effekten mit zeitlicher Latenz differenzieren zu können, wurden zwei unterschiedliche Vorinkubationszeiten gewählt. Bei einer zweistündigen Vorinkubation hatten die Testsubstanzen einen generell geringen Einfluss auf Stoffwechselvorgänge wie zum Beispiel die Bioproteinsynthese, aber ein hohes antioxidatives Potenzial, da sie von der Zelle noch nicht vollständig metabolisiert wurden. Bei einer 24-stündigen Vorinkubation haben die Testsubstanzen keine antioxidative Kapazität mehr, hatten aber durch ihre Metaboliten einen erwartet höheren Einfluss auf Stoffwechselvorgänge wie zum Beispiel die Bioproteinsynthese. Für jedes Nahrungsmittel bzw. Supplement wurden jeweils in verschiedenen Versuchen die Wirkungen nach einer 2 h und 24 h Vorinkubation überprüft.
Zur Überprüfung der in der Literatur [9, 27, 25, 10] beschriebenen antioxidativen Kapazitäten der Testsub-stanzen, diente ein in vitro Testsystem (CAA-Assay; -OxiSelectTM Cellular Antioxidant Assay Kit von Cell Biolabs). Dabei handelt es sich um ein biologisches Testsystem, bei dem vitale Zellen (HaCaTs) unter physiologischen Reaktionsbedingungen verwendet werden. Der Vorteil dieser Herangehensweise gegenüber chemischen Tests ist, dass biologische Parameter, wie z. B. die Aufnahme der Substanzen durch eine Zellmembran und der zelluläre Metabolismus, berücksichtigt werden.
S-Lost induziert Apoptose und beeinflusst andere Stoffwechselkaskaden [13]. Um diese teilweise unbekannten Mechanismen genauer zu untersuchen, wurden Prote-ine verschiedenster Stoffwechselvorgänge oder Signalkaskaden qualitativ bestimmt. Dazu wurden immunologische Screening-Tests (PathScan-Array; PathScan® Stress and Apoptosis Signaling Antibody Array Kit und PathScan® Intracellular Signaling Array Kit von Cell Signaling) durchgeführt. Bei diesen Sandwich-Immuno-assay befindet sich ein primärer Antikörper auf einer Nitrocellulose-Membran. Die Zielproteine binden diesen und werden anschließend von einem sekundären Antikörper erfasst. In einem weiteren Reaktionsschritt wird dieser mit einem Fluoreszenzmarker versetzt, welcher photometrisch detektiert werden kann. Der Einfluss der drei Supplemente (Ginkgo, DHA und Vitamin D3), welche einen nachweislichen Einfluss auf die S-Lost-, CEES- und Chlorambucil--induzierte Zellschäden hatten, wurde untersucht.
Ergebnisse
Verträglichkeitsuntersuchungen
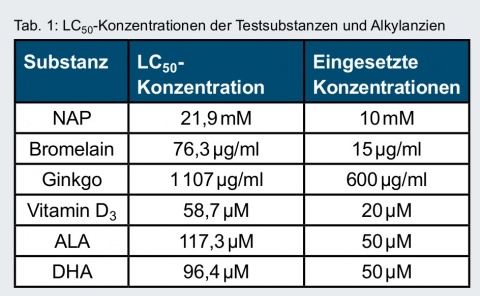
Zunächst werden die Ergebnisse der Verträglichkeitsuntersuchungen in Bezug auf die Toxizität der eingesetzten Testsubstanzen und Alkylanzien dargestellt. Die dabei ermittelten LC50-Konzentrationen sind in Tabelle 1 abgebildet. Die „eingesetzte Konzentration“ entspricht einer Konzentration, bei der keine Einschränkungen der Zellviabilität zu beobachten war.
Einfluss auf die Zellviabilität
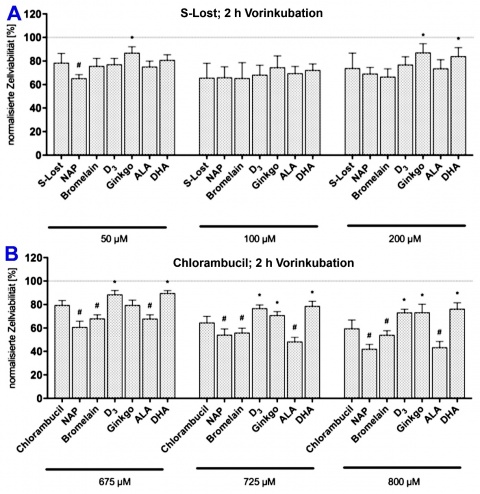
Der Einfluss der Nahrungsmittel und Supplemente auf Alkylanzien-induzierte Hautschäden wurde durch den in Abbildung 1 dargestellten Versuchsaufbau untersucht. Die Ergebnisse der Testsubstanzen, welche einen signifikanten Einfluss auf die Zellviabilität besitzen, sind in Abbildung 2 dargestellt.
Bei einer 2-stündigen Vorinkubation der Zellen mit Ginkgo und DHA mit anschließender Exposition gegenüber 50 μM und 200 µM S-Lost waren, im Vergleich zu einer unbehandelten Kontrolle, signifikante Verbesserungen der Zellviabilität zu beobachten (Abbildung 2A). Vitamin D3, Ginkgo und DHA zeigten nach einer 24-stündigen Vorinkubation und anschließender 24-stündiger Exposition gegenüber Chlorambucil eine signifikante Zellviabilitätssteigerung (Abbildung 2B). Auf die Zytotoxizität des S-Lost Analogons CEES hatte keine der untersuchten Substanzen eine positive Wirkung (Daten nicht dargestellt).
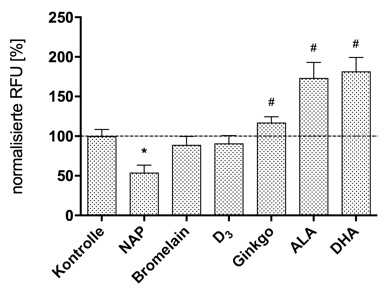
Zusätzlich wurde die oxidative Kapazität der Testsub-stanzen untersucht. Dabei sollten etwaige antioxidative Eigenschaften der Nahrungsmittel und Supplemente identifiziert werden. Wie in Abbildung 3 erkennbar, zeigte nur NAP eine Senkung der normalisierten relativen Fluoreszenz (RFU). Das bedeutet, dass einzig NAP ein antioxidatives Potenzial besitzt. Entgegen der allgemeinen Darstellung in der Literatur [25, 10] zeigten Ginkgo, ALA und DHA sogar eine Steigerung der Bildung freier Radikale, welche einen möglichen Zellschaden ver-ursachen könnten. Dieser Effekt ist mit einer Erhöhung der normalisierten RFU gekennzeichnet (siehe Abbildung 3).
Apoptose und intrazelluläre -Signalkaskaden
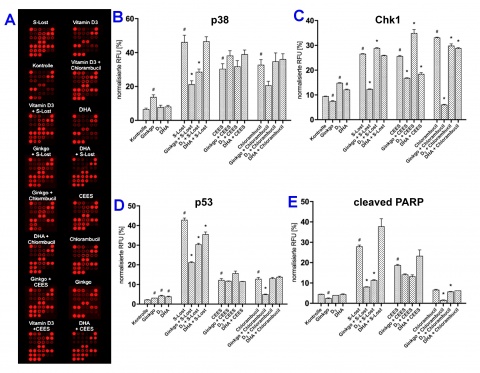
Zur Untersuchung des Einflusses der Testsubstanzen auf alkylanzien-induzierte Veränderungen in den wichtigsten zellulären Signalwegen wurden spezifische Proteine der Apoptose und intrazellulären Signalkaskaden untersucht. Dabei wurden HaCaT mit Vitamin D3, Ginkgo und DHA über 24 Stunden und anschließend gegenüber den drei Alkylanzien exponiert. Vier signifikante Ergebnisse werden in Abbildung 4 dargestellt. Exemplarisch wird in Abbildung 4A die Fluoreszenzaufnahme eines Proteinarrays dargestellt. Hier lassen sich die Effekte der Testsubstanzen und Alkylanzien ablesen.
Die untersuchten Proteine im Signalweg der Apoptose können in verschiedene Gruppen untergliedert werden: Zum einen sind die MAP-Kinasen zu nennen, zu welchen Erk1/2, SAPK/JNK und p38 gehören [8, 23]. Diese werden u. a. durch extrazelluläre Signale sowie von zellulärem Stress aktiviert [16]. Die zweite Gruppe bilden die Checkpoint-Kinasen Chk1 und Chk2. Sie werden aktiviert, wenn bei der Zellteilung DNS-Schäden auftreten [28]. S-Lost hat eine nachgewiesene DNS-alkylierende und somit schädigende Wirkung und induziert zudem oxidativen Stress [14, 13]. Es wird daher eine Beeinflussung dieser zwei Signalwege erwartet. MAP-Kinasen und die Checkpoint-Kinasen können zudem das Tumorsupressorgen p53 aktivieren, welches maßgeblich am programmierten Zelltod (Apo-ptose) beteiligt ist [11]. In dem durch p53 ausgelösten Signalweg werden Caspase-3 und -7 aktiviert, wodurch der Prozess der Apoptose induziert wird [6]. Aus den beschriebenen Signalwegen wurden einzelne aktivierte Proteine identifiziert (p38, Chk1 und p53), welche in Abbildung 4B-4D dargestellt sind. Es zeigt sich, dass die eingesetzten Testsubstanzen (Ginkgo, Vitamin D3 und DHA) die durch alkylanzien-induzierte Proteinaktivierung reduzieren können.
Diskussion und Ausblick
Bewertung der Ergebnisse
Die durchgeführte Arbeit zeigt, dass ein möglicher protektiver Einfluss auf alkylanzien-induzierte Hautschäden durch die untersuchten Nahrungsmittel und Supplemente angenommen werden kann. NAP, Bromelain, Vitamin D3, Ginkgo, ALA und DHA besitzen nach einer CEES--Exposition keinen Einfluss auf die Zellviabilität. Auch NAP, Bromelain und ALA führen bei einer S-Lost- oder Chlorambucil-induzierten Zellviabilitätssenkung zu keiner positiven Wirkung. Ginkgo und DHA lassen nach einer 2-stündigen S-Lost-Exposition einen leicht protektiven Effekt erkennen. Auch Vitamin D3 erzielte nach einer 24-stündigen Vorinkubation und anschließender Vergiftung mit Chlorambucil eine zellviabilitätssteigernde Wirkung. NAP ist die einzige Testsubstanz, welche einen signifikanten antioxidativen Effekt aufweist. Die in der Literatur [25] beschriebene ROS-protektive Wirkung von Ginkgo konnte in der durchgeführten Bestimmung der oxidativen Kapazität (CAA-Assay) nicht reproduziert werden. Daher müssen andere zelluläre Mechanismen, die über eine reine ROS-protektive Wirkung hinausgehen, in Betracht gezogen werden.
Ausblick
Die Ergebnisse der Arbeit zeigen, dass eine Supplementierung mit Ginkgo und Vitamin-D3 eine positive Wirkung haben könnte, was in weiteren Studien verifiziert werden sollte. So könnten zusätzliche Versuche mit komplexeren in vitro Modellen und in vivo Versuchen realisiert werden. Ein etabliertes Cokulturmodell mit HaCaT und THP-1 Zellen als Surrogat für die immunologische Hautkomponente ist für ein weiteres Vorgehen denkbar [5]. Zudem sollte in weiteren Versuchen die Bioverfügbarkeit der Substanzen und die somit resultierende Konzentration im menschlichen Körper, sowie die Metabolisierung der Substanzen berücksichtigt werden. Die Untersuchung und Identifikation weiterer zellulärer Mechanismen, welche die Ursachen der beschriebenen protektiven Wirkung erklären, ist bereits Gegenstand aktueller Arbeiten. Im Rahmen dieser Arbeit konnte eine Screening--Methode zur Identifizierung von protektiven Stoffen gegenüber Alkylanzien erfolgreich etabliert werden. Die Untersuchungen von weiteren Nahrungsmitteln, Supplementen oder anderen potenziell protektiven Stoffen ist somit -zukünftig stark vereinfacht. Dies ermöglicht eine schnelle und effiziente Durchführung von weiteren in vitro -Studien.
Kernaussagen
- Die Freisetzung pro-inflammatorischer Zytokine sowie die Aktivierung von Erk1/2 und p38 -Signalkaskaden nach durch Alkylanzien induzierten Zell-schäden wird durch Ginkgo, DHA und Vitamin D3 reduziert.
- Ginkgo, D3 und DHA zeigten eine signifikante Reduktion der Apoptose.
- Für die Untersuchung der Wirkung von Nahrungsmitteln und Supplementen auf durch Alkylanzien indu--zierte Zellschäden konnte eine effektive Screening---Methode etabliert werden.
Literatur
- Aktories K, Forth W, Allgaier C: Allgemeine und spezielle Pharmakologie und Toxikologie. Für Studenten der Medizin, Veterinärmedizin, Pharmazie, Chemie und Biologie sowie für Ärzte, Tierärzte und Apotheker; mit 305 Tabellen. München: Elsevier, Urban & Fischer 2010.
- Amini A, Masoumi-Moghaddam S, Ehteda A, Morris DL: Bromelain and N-acetylcysteine inhibLiteratuit proliferation and survival of gas-trointestinal cancer cells in vitro: Significance of combination therapy. J Exp Clin Cancer Res. 2014; 33: 92.
- Balali-Mood M, Abdollahi M: Basic and clinical toxicology of mustard compounds. Springer International Publishing 2015; 135-272.
- Balali-Mood M, Hefazi M: The pharmacology, toxicology and medical treatment of sulphur mustard poisoning. Fundam Clin Pharmacol. 2005; 19(3): 297-315.
- Balszuweit F, Menacher G, Bloemeke B, et al.: Development of a co-culture of keratinocytes and immune cells for in vitro investigation of cutaneous sulfur mustard toxicity. Chem Biol Interact. 2014; 223: 117-124.
- Ben Messaoud N, Yue J, Valent D, Katzarova I, Lopez JM: Osmo-stress-induced apoptosis in Xenopus oocytes: Role of stress protein kinases, calpains and Smac/DIABLO. PLoS One. 2015; 10(4): e0124482.
- Bernabe-Garcia M, Lopez-Alarcon M, Villegas-Silva R, et al.: Beneficial Effects of Enteral Docosahexaenoic Acid on the Markers of Inflammation and Clinical Outcomes of Neonates Undergoing Cardiovascular Surgery: An Intervention Study. Ann Nutr Metab. 2016; 69(1): 15-23.
- Cook SJ, Stuart K, Gilley R, Sale MJ: Control of cell death and mitochondrial fission by ERK1/2 MAP Kinase signalling. FEBS J 2017; 284(24): 4177-4195.
- Covarrubias-Pinto A, Acuna AI, Beltran FA, Torres-Diaz L, Castro MA: Old Things New View: Ascorbic Acid Protects the Brain in Neurodegenerative Disorders. Int J Mol Sci. 2015; 16(12): 28194-28217.
- Galan-Arriero I, Serrano-Munoz D, Gomez-Soriano J, et al.: The role of Omega-3 and Omega-9 fatty acids for the treatment of neuropathic pain after neurotrauma. Biochim Biophys Acta Biomembr. 2017; 1859(9 Pt B): 1629-1635.
- Hampp S, Kiessling T, Buechle K, et al.: DNA damage tolerance path-way involving DNA polymerase and the tumor suppressor p53 regulates DNA replication fork progression. Proc Natl Acad Sci U S A. 2016; 113(30): E4311-E4319.
- Hwang TL, Tsai CJ, Chen JL, et al.: Magnesium ascorbyl phosphate and coenzyme Q10 protect keratinocytes against UVA irradiation by suppressing glutathione depletion. Mol Med Rep. 2012; 6(2): 375-378.
- Kehe K, Balszuweit F, Steinritz D, Thiermann H: Molecular toxicology of sulfur mustard- induced cutaneous inflammation and blistering. Toxicology 2009; 263(1): 12-19.
- Kehe K, Szinicz L: Medical aspects of sulphur mustard poisoning. Toxicology 2005; 214(3): 198-209.
- Krishnan AV, Feldman D: Molecular pathways mediating the anti-inflammatory effects of calcitriol: Implications for prostate cancer chemoprevention and treatment. Endocr Relat Cancer. 2010; 17(1): R19-R38.Liu Y, Zhang X, Wang J, Yang J, Tan WF: JNK is required for maintaining the tumor- initiating cell-like properties of acquired chemoresistant human cancer cells. Acta Pharmacol Sin. 2015; 36(9): 1099-1106.
- Morisaki K, Ozaki S: Synthesis of novel vitamin C phosphodiesters: Stability and antioxidant activity. Carbohydr Res. 1996; 286: 123-138.
- Organisation für das Verbot chemischer Waffen OPCW: Pressemitteilung vom 26.02.2014. (last accessed on 01 February 2018).
- Papirmeister B, Gross CL, Meier HL, Petrali JP, Johnson JB: Molecular basis for mustard-induced vesication. Fundam Appl Toxicol. 1985; 5(6 Pt 2): 134-149.
- Reuters Exclusive: Samples confirm Islamic State used mustard gas in Iraq-diplomat. (last accessed on 25 May 2017).
- Rowell M, Kehe K, Balszuweit F, Thiermann H: The chronic effects of sulfur mustard exposure. Toxicology 2009; 263 (1): 9-11.
- Sabourin CLK, Danne MM, Buxton KL, Casillas RP, Schlager JJ: Cytokine, chemokine, and matrix metalloproteinase response after sulfur mustard injury to weanling pig skin. J Biochem Mol Toxicol. 2002; 16 (6): 263-272.
- Shah SA, Ishinaga H, Takeuchi K: Clarithromycin inhibits TNF-α-induced MUC5AC mucin gene expression via the MKP-1-p38MAPK-dependent pathway. Int Immunopharmacol. 2017; 49: 60-66.
- Steinritz D, Bölck B, Schwarz J, et al.: Effect of N-acetyl cysteine and alpha-linolenic acid on sulfur mustard caused impairment of in vitro endothelial tube formation. Toxicol Sci. 2010; 118 (2): 521-529.
- Wang C, Wang B: Ginkgo Biloba Extract Attenuates Oxidative Stress and Apoptosis in Mouse Cochlear Neural Stem Cells. Phytother Res. 2016; 30 (5): 774-780.
- Worek F, Thiermann H, Jenner J: Chemical warfare toxicology. Vol-ume 2: Management of poisoning Includes bibliographical references and index. Cambridge (UK): Royal Society Of Chemistry 2016; 120-156.
- Zavadova E, Desser L, Mohr T: Stimulation of reactive oxygen species production and cytotoxicity in human neutrophils in vitro and after oral administration of a polyenzyme preparation. Cancer Biother. 1995; 10 (2): 147-152.
- Zhang Y, Hunter T: Roles of Chk1 in cell biology and cancer therapy. Int J Cancer. 2014; 134 (5): 1013-1023.
Zitierweise
Giesche R, Popp T, Schmidt A, Thiermann H, Steinritz D: Einsatz von Nahrungsmitteln und Nahrungssupple-menten bei alkylanzien-induzierten Hautschäden. WMM 2019; 63(7): 218-225.
Citation
Giesche R, Popp T, Schmidt A, Thiermann H, Steinritz D: Use of nutrients and supplements for alkylating agent-induced skin damage. WMM 2019; 63(7):
218-225.
Für die Verfasser
Stabsapotheker Robert Giesche
Zentrales Institut des Sanitätsdienstes der Bundeswehr Kiel
Kopperpahler Allee 120; 24119 Kronshagen
E-Mail: [email protected]
[ 1 ] Bromelain und Ginkgo sind Stoffgemische; somit kann keine molare Konzentration angegeben werden.
*Institut für Pharmakologie und Toxikologie der Bundeswehr, München
Datum: 10.09.2019