PSMA PET/CT und PET/MRT in der Diagnostik des Prostatakarzinoms
Aus der Unterabteilung VI des Kommando Sanitätsdienst der Bundeswehr¹, Koblenz (Unterabteilungsleiter: Oberstarzt Dr. Thomas Harbaum), dem Institut für Präventivmedizin der Bundeswehr², Andernach (Leiter: Oberstarzt Prof. Dr. Dr. Dieter Leyk) und der Klinik für Nuklearmedizin³, der Klinik für Radiologie und Neuroradiologie⁴ und der Klinik für Urologie⁵ des Bundeswehrzentralkrankenhauses3, Koblenz (Kommandeur und Ärztlicher Direktor: Generalarzt Dr. Norbert Weller)
Diagnostic of the Prostate Carcinoma with PSMA PET/CT and PET/MRI
Manuela A. Hoffmann¹,²,³, Helmut J. Wieler³, Kerstin Smolka⁴, Hans-Ulrich Schmelz⁵, Stephan Waldeck⁴
Zusammenfassung
Das Prostatakarzinom (PCa) ist das häufigste Karzinom des Mannes in Europa. Die Klinik für Urologie des Bundeswehrzentralkrankenhauses (BwZKrhs) Koblenz hat das zertifizierte Prostatakarzinomzentrum Koblenz-Mittelrhein gegründet, um die Diagnostik und die Therapie von Patienten mit PCa zu optimieren. Die Einführung des Prostata-Spezifischen Membran-Antigens (PSMA) in die Diagnostik ist ein weltweiter Durchbruch in der klinischen Routine Nuklearmedizinischer Abteilungen.
Die Position der Bildgebung mit 68Gallium(Ga)-PSMA und PET in der Diagnostik des primären und rezidivierenden PCa wird dargestellt. Die wichtigsten verfügbaren Daten von vorliegenden zumeist retrospektiven Studien werden diskutiert.
Die Bildgebung mit 68Ga-PSMA besitzt beim primären Staging bei Patienten mit mittlerem bis hohem Risikograd des Prostatakarzinoms eine erhebliche Relevanz. Die Kombination der PET/CT und/oder PET/MRT mit der pelvinen multiparametrischen (mp) Magnetresonanztomographie hat eine erhebliche Bedeutung beim Management der Patienten erreicht. Die 68Ga-PSMA PET/CT ist der 18F- bzw. 11C-Cholin PET/CT sowohl beim Primär- als auch beim Sekundär-staging überlegen. Bei Patienten mit einem biochemischen Rezidiv ist die PET/CT-Positivität direkt assoziiert mit der Höhe des Anstiegs des Prostata-Spezifischen Antigens (PSA).
Schlüsselwörter: 68Gallium-PSMA, PET/CT, PET/MRT, PET-geführte personalisierte Therapie, Prostatakarzinom
Summary
Prostate cancer (PCa) is the leading cancer in men in Europe. The department of Urology of the Bundeswehr Central Hospital Koblenz has founded the certified PCa-Center Koblenz--Mittelrhein to optimize diagnostics and treatment of patients with PCa. The introduction of prostate-specific membrane-antigen (PSMA) into diagnostic is a worldwide breakthrough in the clinical routine of nuclear medicine departments.
The value of 68Ga-PSMA PET imaging as a diagnostic procedure for primary and recurrent PCa is assessed. The most eminent data from mostly retrospective studies currently available are discussed. The current knowledge on 68Ga-PSMA PET implicates that primary staging with PET/CT and/or PET/MRI is meaningful in patients with intermediate to high-risk PCa and that the combination with pelvic multiparametric (mp) MRI reaches the highest impact on patient management. 68Ga-PSMA PET/CT is superior to 18F/11C--Choline PET/CT in primary as well as in secondary staging. In patients with biochemical relapse, PET/CT positivity is directly associated with prostate-specific antigen (PSA) increase.
Keywords: 68Gallium-PSMA, PET/CT, PET/MRI, PET--guided personalized therapy, prostate cancer
Einleitung
Das Prostatakarzinom (PCa) ist die häufigste Tumorerkrankung des Mannes in Deutschland. Die Neuerkrankungshäufigkeit für 2016 wurde mit 66 900 Fällen angegeben. Unter allen Krebserkrankungen lag die Mortalität im Jahr 2012 mit 12 957 Patienten an 3. Stelle [7, 22]. Eine exakte Diagnostik bei Verdacht auf ein PCa ist essentiell für einen schnellen und kurativen Therapieansatz. Die bildgebende Diagnostik bei Patienten mit einem vermuteten Rezidiv des PCa nach initialer Therapie mit kurativem Ansatz stellt eine Herausforderung dar.
Bildgebende Diagnostik des Prostatakarzinoms
Primärdiagnostik

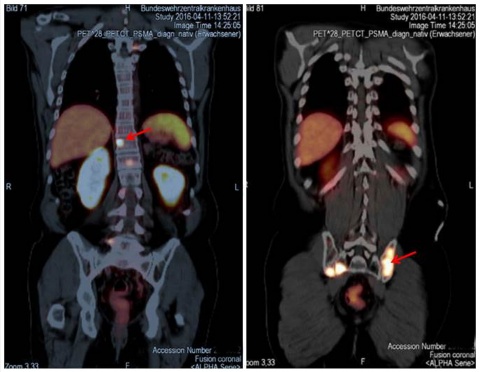
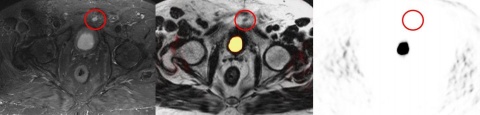
In der Literatur finden sich zunehmende Hinweise darauf, dass mit Hilfe der sog. PSMA PET eine weitere Steigerung der Diagnosesicherheit möglich ist. Das PSMA ist ein integrales Membran-Protein, welches in Prostatakarzinomzellen bis zu 1000-fach stärker exprimiert wird als in gesunden Prostatazellen. Die Expression ist insbesondere in höhergradigen Karzinomen bei einer metastatischen Erkrankung und in hormonrefraktären PCa gesteigert (Abbildung 1). Folgerichtig wurde das PSMA zu einem Target hochgradigen Interesses für die spezifische Bildgebung und Therapie beim PCa. Den Arbeitsgruppen aus Heidelberg [4, 10] und München [10] gebührt der Verdienst für die Einführung einer mittlerweile weltweit anerkannten diagnostischen Methode.
Die Expression von PSMA in der Prostata steigt mit zunehmender Tumoraggressivität, während es in blandem Prostatagewebe kaum nachweisbar ist [8, 34, 37]. Deshalb wird zunehmend an der Entwicklung von Hybridmethoden gearbeitet, die die PSMA PET und die mpMRT in einem Untersuchungsdurchgang durchführen können, um die hohe Sensitivität der MRT mit der metabolischen Aussage der PET zu verbinden [23, 26, 36]. Dies ist besonders im Hinblick auf eine Unterschätzung des Tumorgrades sowie für die Optimierung der TNM-Klassifikation prätherapeutisch von erheblicher Bedeutung. Meist wird das PSMA an den Tracer 68Ga gekoppelt, seit neuem auch an 18F [35].
Rezidivdiagnostik
Etwa 40 % der Patienten, bei denen ein primär kurativer lokaltherapeutischer Ansatz gewählt wird, erleiden ein Rezidiv der Erkrankung [30]. Die überwiegende Anzahl dieser Patienten entwickelt ein sogenanntes biochemisches Rezidiv, d. h. einen Anstieg des PSA ohne klinische Evidenz für das Vorhandensein von Metastasen [9]. Dieses „biochemische Tumorrezidiv“ tritt bei ca. 20 - 30 % der Patienten nach radikaler Prostatektomie und bei bis zu 60 % nach Strahlentherapie auf [12, 24]. Im Falle eines solchen Rezidivs gerät die konventionelle Schnittbildgebung mittels Spiral-CT oder MRT häufig an ihre Grenzen, insbesondere im Hinblick auf Fragen zur Beurteilung pathologischer Lymphknoten. Daher wurde intensiv nach Wegen gesucht, die bildgebenden Verfahren zu verbessern. Der Fokus der Forschung lag dabei in den vergangenen Jahren v. a. auf dem PSMA.
Die aktuellen deutschen S3-Leitlinien zur Diagnostik des PCa haben dieser Entwicklung Rechnung getragen, und die PSMA PET/CT gilt jetzt als integraler Bestandteil der Diagnostik [27, 28].
Stellenwert des PSMA PET/CT
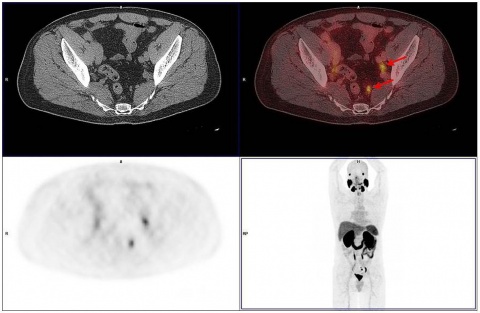
Die Magnet-Resonanz-Tomographie, speziell die multiparametrische Hochfeld-MRT (3T), ist aktuell die marktverfügbar sensitivste morphologische bildgebende Methode. Es liegt nahe, die hohe Sensitivität der MRT mit einem hochspezifischen Tracer zu kombinieren. Daher ist der direkte Vergleich von PSMA PET/CT und PET/MRT (multiparametrisch) von erheblichem Interesse für künftige Untersuchungen [6]. Es ist bereits jetzt unbestritten, dass in Zukunft die Hybridverfahren PET/CT – PET/MRT bessere Ergebnisse bringen als die einzelnen morphologischen Methoden [33].
Eigene Vergleichsuntersuchungen PSMA PET/CT – PET/MRT
Nach Einführung des PET/MRT am BwZKrhs Koblenz wurden die Untersuchungsergebnisse der ersten Patienten, die mit beiden Methoden untersucht wurden, miteinander verglichen.
Untersuchungsmethoden
Die PET/CT-Aufnahmen wurden mit Hilfe des Biograph64 TruePoint (True V HD) PET/CT Scanners (Siemens, Erlangen) erstellt. Dabei erfolgten 60 Minuten nach Injektion von 68Ga-PSMA-11 (im Mittel 176 MBq, zwischen 157 - 268 MBq, je nach Körpergewicht) Ganzkörperaufnahmen. PSMA-11 erhielten wir als Eigenhersteller von der Klinik für Nuklearmedizin der Universitätsmedizin Mainz bzw. von Advanced Accelerator Applications (AAA) Bonn. Die PET/MRT-Aufnahmen mit simultaner Akquisition von MRT--Sequenzen (nativ) erfolgten etwa 2 Stunden nach Injektion der Aktivität mit Hilfe des Biograph mMR 3-Tesla-Hybrid-System (Siemens, Erlangen), unmittelbar im Anschluss an die PET/CT-Untersuchung. Im Rahmen der Durchführung der PET/MRT wurden folgende Sequenzen eingesetzt: T2 Turbo Spin Echo (TSE) transversal, coronal und sagittal; T1 TSE coronal; T2 sagittal; diffusionsgewichtete Sequenzen (B50/500/1000); Short-Tau Inversion Recovery (STIR) transversal.
Ergebnisse
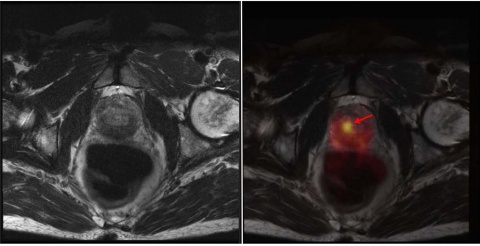
Bei dieser (zunächst noch kleinen) Gruppe von Patienten fanden sich in 31 Fällen (31/34) Übereinstimmungen der Befunde. Keine einzige zusätzliche pathologische Veränderung (Läsion/Lymphknoten/Lokalrezidivsituation) wurde erst durch die zweite Untersuchung erkannt.
In drei Fällen (3/34) konnte eine Diskrepanz aufgezeigt werden; bei zwei Fällen war das PET/CT, in einem Fall das PET/MRT überlegen.
Bei einem Patienten waren drei im PET/CT hochstoffwechsel-aktive Prostatakarzinomherde im PET/MRT nicht abgrenzbar; der intraprostatische PET/MRT-Befund war nicht beurteilbar.
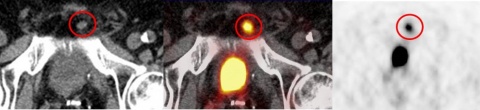
Folgerungen und Ausblick
Die Durchführung der ergänzenden PET/MRT-Untersuchung ist für die beteiligten ärztlichen Kolleginnen und Kollegen eine wichtige Erfahrung im Sinne von Qualitätssicherung und Befunderhärtung, sodass wir eine prospektive Studie zum Vergleich dieser beiden Methoden planen, zumal hierzu bisher nur wenige Daten vorliegen. Hierbei sollten neuere Algorithmen zur Streustrahlenkorrektur bei der PET/MRT Anwendung finden, um die Problematik des Halo-Artefaktes auszuschalten.
Kernaussagen
- Mit Hilfe der mpMRT/Ultraschall fusioniert geführten Biopsien kann eine signifikant höhere Detektionsrate von klinisch relevanten Prostatamalignomen erreicht werden, als es konventionelle diagnostische Prozeduren ermöglichen.
- Die Einführung des Prostata-spezifischen Membran-Antigens (PSMA) ist ein weltweiter Durchbruch in der klinischen Anwendung in Nuklearmedizinischen Abteilungen (in Diagnostik und Therapie).
- Die PSMA PET/CT gilt als integraler Bestandteil bei der Rezidivdiagnostik des PCa.
- Die PSMA PET und die mpMRT ergänzen sich bezüglich Sensitivität und Spezifität.
Literatur
- Afshar-Oromieh A, Avtzi E, Giesel FL et al.: The diagnostic value of PET/CT imaging with the (68)Ga-labelled PSMA ligand HBED-CC in the diagnosis of recurrent prostate cancer. Eur J Nucl Med Mol Imaging 2015; 42 (2): 197 - 209.
- Afshar-Oromieh A, Zechmann CM, Malcher A et al.: Comparison of PET imaging with a (68)Ga-labelled PSMA ligand and (18)F-choline-based PET/CT for the diagnosis of recurrent prostate cancer. Eur J Nucl Med Mol Imaging 2014; 41 (1): 11 - 20.
- Afshar-Oromieh A, Haberkorn U, Schlemmer HP et al.: Comparison of PET/CT and PET/MRI hybrid systems using a 68Ga-labelled PSMA ligand for the diagnosis of recurrent prostate cancer: Initial experience. Eur J Nucl Med Mol Imaging 2014; 41 (5): 887 - 897.
- Afshar-Oromieh A, Malcher A, Eder M et al.: PET imaging with a 68Gagallium-labelled PSMA ligand for the diagnosis of prostate cancer: Biodistribution in humans and first evaluation of tumour lesions. Eur J Nucl Med Mol Imaging 2013; 40 (4): 486 - 495.
- Ahmed HU, El-Shater Bosaily A, Brown LC et al.: Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer (PROMIS): A paired validating confirmatory study. The Lancet 2017; 389 (10071): 815 - 822.
- Avanesov M, Karul M, Derlin T: (68)Ga-PSMA als neuer Tracer für die Evaluation des Prostatakarzinoms: Vergleich zwischen PET-CT und PET-MRT beim biochemischen Rezidiv. Radiologe 2015; 55 (2): 89 - 91.
- Böhmer D, Wirth M, Miller K et al.: Radiotherapy and hormone treatment in prostate cancer. Dtsch Arztebl Int 2016; 113 (14): 235 - 241.
- Ceci F, Uprimny C, Nilica B et al.: (68)Ga-PSMA PET/CT for restaging recurrent prostate cancer: Which factors are associated with PET/CT detection rate? Eur J Nucl Med Mol Imaging 2015; 42 (8): 1284 - 1294.
- Cornford P, Bellmunt J, Bolla M et al.: EAU-ESTRO-SIOG Guidelines on prostate cancer. Part II: Treatment of relapsing, metastatic, and castration-resistant prostate cancer. Eur Urol 2017; 71 (4): 630 - 642.
- Eder M, Schäfer M, Bauder-Wüst U et al.: 68Ga-complex lipophilicity and the targeting property of a urea-based PSMA inhibitor for PET imaging. Bioconjug Chem 2012; 23 (4): 688 - 697.
- Eiber M, Maurer T, Souvatzoglou M et al.: Evaluation of Hybrid 68Ga-PSMA Ligand PET/CT in 248 patients with biochemical recurrence after radical prostatectomy. J Nucl Med 2015; 56 (5): 668 - 674.
- Freedland SJ, Presti JC, Amling CL et al.: Time trends in biochemical recurrence after radical prostatectomy: Results of the SEARCH database. Urology 2003; 61 (4): 736 - 741.
- Giesel FL, Fiedler H, Stefanova M et al.: PSMA PET/CT with Glu-urea-Lys-(Ahx)-68Ga(HBED-CC) versus 3D CT volumetric lymph node assessment in recurrent prostate cancer. Eur J Nucl Med Mol Imaging 2015; 42 (12): 1794 - 1800.
- Grisanti S, Antonelli A, Buglione M et al.: Analysis of circulating tumor cells in prostate cancer patients at PSA recurrence and review of the literature. Anticancer Res 2016; 36 (6): 2975 - 2981.
- Heidegger I, Skradski V, Steiner E et al.: High risk of under-grading and -staging in prostate cancer patients eligible for active surveillance. PLoS ONE 2015; 10 (2): e0115537.
- Heidenreich A, Bastian PJ, Bellmunt J et al.: EAU guidelines on prostate cancer. Part II: Treatment of advanced, relapsing, and castration-resistant prostate cancer. Eur Urol 2014; 65 (2): 467 - 479.
- Hoffmann MA, Wieler HJ, Maus S et al.: Diagnostic performance of 68Ga-PSMA PET/CT to detect significant prostate cancer and comparison with 18F-Choline PET/CT. J Nucl Med 2017; 58 Supplement 1: 540.
- Hoffmann MA, Wieler HJ, Jakobs FM et al.: Diagnostischer Stellenwert der multiparametrischen MRT mit gezielter Fusionsbiopsie der Prostata bei Patienten mit PSA-Anstieg und negativer Stanzbiopsie zur Detektion klinisch signifikanter Prostatakarzinome. Korrelation mit dem Gleason Score. Nuklearmedizin 2017; 56 (4): 147 - 155.
- Hoffmann MA, Taymoorian K, Ruf C et al.: Diagnostic performance of multiparametric magnetic resonance imaging and fusion targeted biopsy to detect significant prostate cancer. Anticancer Res 2017; 37 (12): 6871 - 6877.
- Hoffmann MA, Miederer M, Wieler HJ et al.: Diagnostic performance of 68Gallium-PSMA-11 PET/CT to detect significant prostate cancer and comparison with18FEC PET/CT. Oncotarget 2017; 8 (67): 111073 - 111083.
- Hoffmann MA, Wieler HJ, Smolka K: „Head-to-head comparison of 68Ga-PSMA PET/CT and 68Ga-PSMA PET/MRI for restaging of biochemical recurrent prostate cancer. J Transl Sci; (im Druck).
- Kaatsch P, Spix C, Katalinic A et al.: Beiträge zur Gesundheitsberichterstattung des Bundes – Krebs in Deutschland 2011/2012. Berlin: Robert Koch-Institut 2015.
- Kesch C, Visensia M, Radtke JP: Intraindividueller Vergleich von 18F-PSMA-PET/CT, mpMRT und radikalem Prostatektomiepräparat bei Männern mit primär diagnostiziertem Prostatakarzinom. Nuklearmedizin 2017; 56 (4): V54.
- Khuntia D, Reddy CA, Mahadevan A et al.: Recurrence-free survival rates after external-beam radiotherapy for patients with clinical T1-T3 prostate carcinoma in the prostate-specific antigen era: What should we expect? Cancer 2004; 100 (6): 1283 - 1292.
- Krohn T, Verburg FA, Pufe T et al.: (68)GaPSMA-HBED uptake mimicking lymph node metastasis in coeliac ganglia: An important pitfall in clinical practice. Eur J Nucl Med Mol Imaging 2015; 42 (2): 210 - 214.
- Langer DL, van der Kwast TH, Evans AJ et al.: Intermixed normal tissue within prostate cancer: Effect on MR imaging measurements of apparent diffusion coefficient and T2--sparse versus dense cancers. Radiology 2008; 249 (3): 900 - 908.
- Leitlinienprogramm Onkologie. Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF: Interdisziplinäre Leitlinie der Qualität S3 zur Früherkenung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, Langversion 4.0.
http://leitlinienprogramm-onkologie.de/uploads/tx_sbdownloader/LL_Prostata_Langversion_4.0.pdf (last accessed on 03 May 2018). - Lenzen-Schulte M: Leitlinienprogramm Onkologie: Eine „living guideline“ zum Prostatakarzinom. Dtsch Arztebl Int 2017; 114 (3): A80.
- Mottet N, Bellmunt J, Bolla M et al.: EAU-ESTRO-SIOG Guidelines on prostate cancer. part 1: Screening, diagnosis, and local treatment with curative intent. Eur Urol 2017; 71 (4): 618 - 629.
- Mullins JK, Feng Z, Trock BJ et al.: The impact of anatomical radical retropubic prostatectomy on cancer control: The 30-year anniversary. J Urol 2012; 188 (6): 2219 - 2224.
- Oliveira IS, Pontes-Junior J, Abe DK et al.: Undergrading and understaging in patients with clinically insignificant prostate cancer who underwent radical prostatectomy. Int Braz J Urol 2010; 36 (3): 292 - 299.
- Pepe P, Garufi A, Priolo GD et al.: Multiparametric MRI/TRUS fusion prostate biopsy: Advantages of a transperineal approach. Anticancer Res 2017; 37 (6): 3291 - 3294.
- Picchio M, Mapelli P, Panebianco V et al.: Imaging biomarkers in prostate cancer: Role of PET/CT and MRI. Eur J Nucl Med Mol Imaging 2015; 42 (4): 644 - 655.
- Sweat SD, Pacelli A, Murphy GP et al.: Prostate-specific membrane antigen expression is greatest in prostate adenocarcinoma and lymph node metastases. Urology 1998; 52 (4): 637 - 640.
- Szabo Z, Mena E, Rowe SP et al.: Initial Evaluation of (18)FDCFPyL for prostate-specific membrane antigen (PSMA)-targeted PET imaging of prostate cancer. Mol Imaging Biol 2015; 17 (4): 565 - 574.
- Woythal N, Kempkensteffen C, Miller K: Ga-68 PSMA PET/CT in the detection of primary prostate cancer: an initial experience. Nuklearmedizin 2017; 56: V48.
- Wright GL, Haley C, Beckett ML et al.: Expression of prostate-specific membrane antigen in normal, benign, and malignant prostate tissues. Urol Oncol 1995; 1 (1): 18 - 28.
- Wu X, Reinikainen P, Kapanen M et al.: Diffusion-weighted MRI provides a Useful biomarker for evaluation of radiotherapy efficacy in patients with prostate cancer. Anticancer Res 2017; 37 (9): 5027 - 5032.
Bildquelle (alle Abbildungen): Bundeswehrzentralkrankenhaus Koblenz
Zitierweise:
Hoffmann MA, Wieler HJ, Smolka K, Schmelz HU, Waldeck S: PSMA PET/CT und PET/MRT in der Diagnostik des Prostatakarzinoms. Wehrmedizinische Monatsschrift 2018; 62(8): 266 - 270.
Citation:
Hoffmann MA, Wieler HJ, Smolka K, Schmelz HU, Waldeck S: Diagnostic of the Prostate Carcinoma with PSMA PET/CT and PET/MRI. Wehrmedizinische Monatsschrift 2018; 62(8): 266 - 270.
Für die Verfasser
Oberfeldarzt Dr. med. Manuela A. Hoffmann
Kommando Sanitätsdienst der Bundeswehr, Koblenz
Institut für Präventivmedizin der Bundeswehr, Andernach
E-Mail: [email protected]
Datum: 08.08.2018










