Wundzentrum des BwKrhs Berlin erfolgreich rezertifiziert - einzigartig in der Bundeswehr -
Aus der Abteilung Dermatologie, Venerologie und Allergologie (Chefarzt: Oberstarzt Dr. R. Hartmann) des Bundeswehrkrankenhauses Berlin (Kommandeur: Admiralarzt Dr. G. Reuter)
Das Wundzentrum des Bundeswehrkrankenhauses (BwKrhs) Berlin wurde erneut nach den Vorgaben der Initiative chronische Wunde e. V. (ICW) fächerübergreifend zertifiziert – bundesweit gibt es das bisher nur viermal und ist einzigartig in der Bundeswehr!

Deutschlandweit gibt es insgesamt vier derart zertifizierte interdisziplinäre Wundzentren. Neben dem BwKrhs Berlin sind noch die Universitätsklinik der Hansestadt Hamburg Eppendorf, das Universitätsklinikum Essen und die Universitätsklinik Düsseldorf von der ICW dreifach zertifiziert.
Durch vermehrte Auslandseinsätze der Bundeswehr ist auch bei Soldaten vermehrt mit dem Auftreten von großen Weichteil-Defekten und der Entwicklung chronischer Wunden zu rechnen. Daher ist die Versorgung komplexer chronischer Wunden nach Traumata oder durch Infektionskrankheiten einsatzmedizinisch besonders relevant.
Allein in Deutschland leiden drei bis vier Millionen Menschen an einer chronischen Wunde. Von einer „chronischen Wunde“ spricht man, wenn diese trotz adäquater Therapie nach 8 Wochen keine Heilungstendenz zeigt. Da die Genese solcher Wunden sehr unterschiedlich sein kann, gestaltet sich die Therapie oftmals schwierig. Zu den häufigsten Ursachen zählen chronisch venöse Insuffizienz, periphere arterielle Verschluss Krankheit, Stoffwechselerkrankungen wie Diabetes mellitus, oder chronischer Druck (Dekubitus). Andere Ursachen, wie Verletzungen, Autoimmunvaskulopathien, Infektionskrankheiten oder Hauttumore sind selten, sollten aber dennoch nicht übersehen werden. Solch seltenere Ursachen möchten wir Ihnen nachfolgend beispielhaft anhand von drei kleinen Fallberichten veranschaulichen.
Fallbericht 1 – Wundheilungsstörung bei Akne conglobata
Anamnese
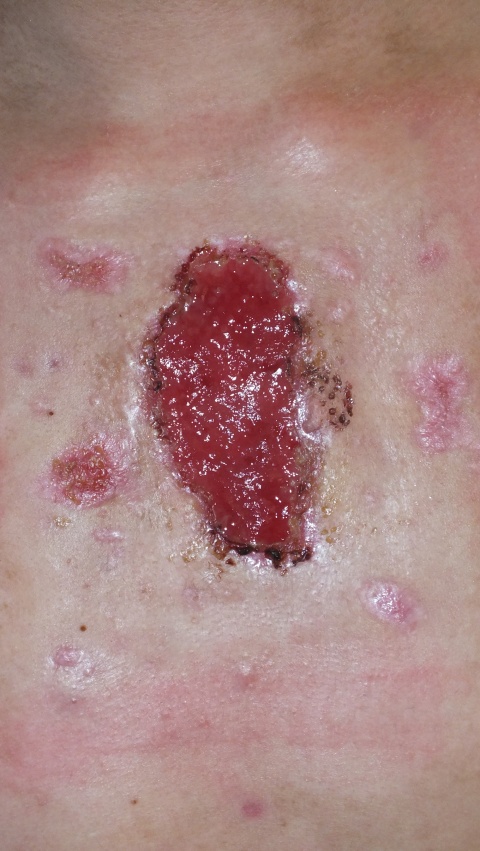
Ein 15-jähriger Patient stellt sich bei uns mit einer seit etwa sieben Monaten bestehender offenen Wunde auf Höhe des Sternums zur Abklärung vor. Außer einer Akne conglobata, die seit sieben Monaten mit Isotretinoin per os behandelt wird, sind keine Erkrankungen bekannt.
Aufnahmebefund
Bei Aufnahme zeigt sich sternal auf Höhe des zweiten bis vierten Intercostalraums eine etwa 8x4 cm messende, scharfbegrenzte Ulzeration mit rotem Granulationsgewebe, ohne Fibrinbelege und deutlichem Foetor. In der Wundumgebung sehen wir multiple, maximal bis zu 2x1 cm messende, reizlose, hellrosa Narben.
Nebenbefundlich bestehen Pusteln auf erythematösem Grund im Gesicht bei bekannter Akne, sowie eine Cheilitis sicca unter System-Therapie mit Isotretinoin.
Die restliche körperliche Untersuchung zeigte sich altersentsprechend unauffällig.
Diagnostik
Das Aufnahmelabor zeigte sich komplett unauffällig.
Mikrobiologisch ließen sich mäßig Staphylococcus aureus und vereinzelt koagulasenegative Staphylokokken nachweisen.
Die bei Aufnahme durchgeführte Probeentnahme zeigte histologisch lediglich Granulationsgewebe, vereinbar mit einer Wundheilungsstörung bei Akne conglobata. Es bestand kein Anhalt für Malignität.
Therapie und Verlauf
Initial behandelten wir antiseptisch und verwendeten silikonhaltige Distanzgitter als Wundauflage. Die Isotretinoin-Therapie wurde pausiert. Im Verlauf führten wir eine Spalthauttransplantation durch. Am sechsten postoperativen Tag zeigte sich das Transpalantat vollständig angewachsen.
Diskussion
In Bezug auf diesen Fall haben wir überlegt, ob die Wundheilungsstörung möglicherweise als Isotretinoin-Nebenwirkung anzusehen ist, da anamnestisch ein Zusammenhang zwischen dem Auftreten der Wunde und dem Beginn der oralen Einnahme von Isotretinoin bestand. Dem Vitamin A, welches über den intranukleären Rezeptor (RXR) in die Genexpression eingreift, wird eine Wichtigkeit für eine intakte Epithelfunktion zugeschrieben. Hieraus könnte die sehr häufige Nebenwirkung (1/10) von Isotretinoin einer erhöhten Verletzlichkeit der Haut hergeleitet werden. Eine konkrete Wundheilungsstörung aufgrund einer regelmäßigen Einnahme konnten wir nach einer Literaturrecherche nicht belegen. Des Weiteren werden als Nebenwirken u. a. Infektionen der Haut mit grampositiven Bakterien genannt (selten 1/10000). Wir betrachteten diese Nebenwirkungen als Gründe für die Unterhaltung der Wunde unseres jungen Patienten und entschieden uns die Isotretinoin-Therapie zu pausieren und empfehlen bei chronischen Wunden unter Isotretinoin-Therapie das Fortführen dieser Therapie zumindest kritisch zu überdenken. Für endgültige Empfehlungen bedürfte es jedoch angepasster und umfassenderer Studien.
Fallbericht 2 – Abheilung eines Pyoderma gangraenosum unter Dapson
Anamnese:
Eine 80-jährige Patientin stellte sich in unserer Wundsprechstunde mit einem seit etwa einem Jahr bestehenden, deutlich größenprogredientem Ulcus an der linken Mamma vor. Es bestünden stechend-schneidende Schmerzen, schon bei leichter Berührung, wie dem Reiben der Kleidung. Parallel bestünde seit mehreren Monaten ein trockener Husten. Diesbezüglich wurde vier Monate zuvor in einem auswärtigen Haus ein CT-Thorax durchgeführt. Es wurde eine Bronchopneumonie diagnostiziert und mit Moxifloxazin über vier Wochen behandelt. Die Kontrolluntersuchung zeigte einen rückläufigen, aber noch nicht vollständig abgeheilten Befund.
Abgesehen von einem medikamentös mit Candesartan und HCT eingestellten arteriellen Hypertonus bestanden keine relevanten Vorerkrankungen.
Aufnahmebefund
Wir sahen bei Aufnahme eine schmerzgeplagte Patientin in leicht reduziertem Allgemeinzustand und normalen Ernährungszustand.Die Perkussion der Lunge zeigte beidseits sonoren Klopfschall, die Lungengrenzen waren gut Atem verschieblich. Auskultatorisch bestand links basal ein verschärftes Atemgeräusch, über restlichen Lungenabschnitten vesikuläres Atemgeräusch.
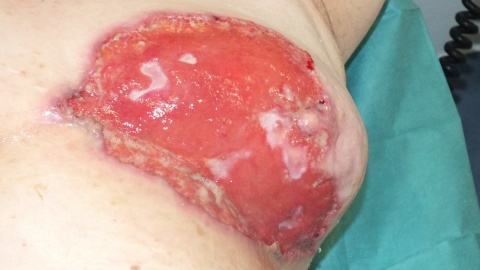
Im Bereich der linken Mamma zeigte sich ein 13x15 cm durchmessendes, unregelmäßig begrenztes Ulcus (Sternum bis Mamille) mit unterminierten livid roten Wundrändern. Der Wundgrund war größtenteils granulierend, kranial fibrinbelegt, am unteren Wundpol stärker belegt und stärker sezernierend. In der Mitte der Läsion zeigten sich unregelmäßig begrenzte epithelisierte stegartige Areale, die Mamille war narbig eingezogen.
Am linken Oberarm zeigte sich ein weiteres etwa 1cm durchmessendes Ulcus. Dieses war rundlich konfiguriert, ebenfalls mit livid rotem unterminierten Randwall, auch hier war der Wundgrund rosig granulierend. Über dem rechten medialen Malleolus zeigte sich ein 1 cm durchmessender zentral ulzerierter hautfarbener Nodus.
Diagnostik
Im Aufnahmelabor war das CRP mit 61,5 mg/l (<5 mg/l) pathologisch erhöht und es bestand eine relative Lymphopenie 10,2 % (19 - 53 %). Die durchgeführte Vaskulitis Diagnostik war komplett unauffällig. Mittels MTB-Quantiferontest wurde eine Tuberkulose ausgeschlossen.
Kulturell wurde im Wundabstrich Proteus mirabilis nachgewiesen.
Die bei Aufnahme durchgeführte Probeexzision zeigte eine Ulzeration mit diffusem neutrophilenreichen Infiltrat, es bestand kein Anhalt für Tuberkulose, Mammakarzinom oder andere Malignität.
Das Röntgen-Thorax zeigte kavernöse Raumforderungen in beiden Lungen, rechtsseitig mit Aspekt der Spiegelbildung, zusätzlich wurde der Verdacht auf Infiltrate im rechten Mittellappen geäußert.
Das CT-Thorax zeigte Infiltrationen mit Kavernenbildung im Segment 1 und 2 links mit Kompression des Segmentbronchus und Atelektase im Segment 3 links, Infiltration mit Kaverne und Spiegelbildung im Mittellappen, den rechten Oberlappen infiltrierend. Lateral davon zeigte sich ein kugelförmiges, pneumonisches Infiltrat. Außerdem sah man vergrößerte Lymphknoten infracarinal. Das Ulcus der linken Mamma war ohne Verbindung nach intrathorakal.
In der Bronchoskopie sah man eine ausgeprägte straßenartige Schleimhauthypertrophie.
In der Broncheoalveolären Lavage konnten keine säurefesten Stäbchen nachgewiesen werden. Sowohl Ziehl-Neelsen Färbung als auch PCR auf Mykobakterium tuberculosis waren negativ.
Kulturell konnten nur physiologische Keime, sowie Streptokokken nachgewiesen werden.
Der histologische Befund zeigte neben einem neutrophilenreichen Infiltrat überwiegend fibrosierte respiratorische Schleimhaut war hier passend zu einer chronischen, abszedierenden Pneumonie. Es bestand kein Anhalt für Malignität. Granulome konnten nicht nachgewiesen werden.
Therapie und Verlauf
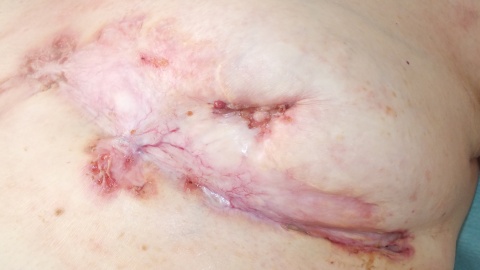
Wir entnahmen mehrere Probebiopsien, welche eine Ulzeration mit neutrophilenreichem Infiltrat, passend zu einem Pyoderma gangraenosum zeigten. Hinweise auf Tuberkulose, Mammakarzinom oder andere Malignität zeigten sich nicht. Granulome konnten nicht nachgewiesen werden. Die Differentialdiagnose einer Tuberkulose wurde bei negativem Quantiferontest und des fehlenden Nachweises von säurefesten Stäbchen und der negativen Tbc-PCR der BAL verworfen.
Das Autoantikörperlabor (u. a. ANA, ANCA) zeigte sich komplett unauffällig.
Die abszedierende Pneumonie wurde initial mit Ampicillin/Sulbactam intravenös behandelt. Im Verlauf stellten wir die Antibiose gemäß der Empfehlung unserer internistischen Kollegen auf Tazobactam um und führten diese über insgesamt sechs Wochen durch.
Das Pyoderma gangraenosum behandelten wir mit Prednisolon 1 mg / kg Körpergewicht per os unter Gastroprotektion und Osteoporose Prophylaxe. Topisch wurde mit Klasse-IV-Steroiden, antiseptischen Wundspüllösungen und Polyurethan-Schäumen als Wundauflage gearbeitet. Um systemische Kortikosteroide einzusparen leiteten wir einen individuellen Heilversuch mit Dapson 50 mg zweimal täglich ein. Im weiteren Verlauf konnte bei gutem Ansprechen auf diese Therapie das Prednisolon sukzessive reduziert und schließlich abgesetzt werden.
Nach inzwischen 18-monatiger Therapie sind die Ulzerationen unter cribiformer Narbenbildung nahezu abgeheilt. Es ist geplant, die Therapie mit Dapson noch bis zur vollständigen Abheilung fortzuführen.
Fazit
Oft sind wir im Bereich der Wundtherapie mit Befunden konfrontiert, welche nicht klar einer einzelnen Äthiopathologie zugeordnet werden können, oder wie das Pyoderma gangraenosum „Ausschluss Diagnosen“ sind. Oftmals sind diese Patienten höheren Alters und multipel vorerkrankt. Dies stellt sowohl in der Diagnostik als auch in der Therapie eine Herausforderung dar. Beispielsweise litt unsere Patientin parallel an einer abszedierenden Pneumonie, was eine therapeutische Herausforderung bei langfristiger immunsuppressiver Therapie darstellte und eine enge Zusammenarbeit insbesondere mit unseren internistischen Kollegen notwendig machte.
Fallbericht 3 -Vegetierende Form eines Pyoderma gangraenosum mit beginnendem Erysipel
Anamnese
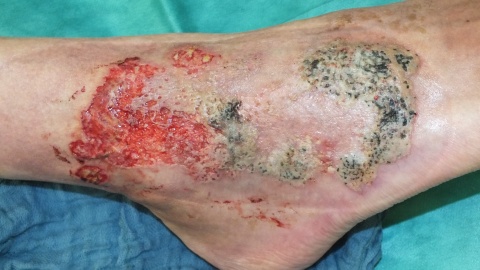
Ein 61-jähriger Patient präsentiert sich in unserer Wundsprechstunde mit einer schmerzhaften Wucherung an einem vorbekannten Ulkus am rechten Außenknöchel mit Schmerzen und neu aufgetretener Rötung.
Vier Monate zuvor sei er stationär wegen einer ulzerierenden Läsion an gleicher Lokalisation bei Verdacht auf ein Pyoderma gangraenosum behandelt worden, die Läsion sei unter steroidaler Therapie im Verlauf fast vollständig abgeheilt. In der Labordiagnostik hatten sich laut Arztbrief zuvor keine spezifischen Hinweise für eine Vaskulitis oder Kollagenosen gezeigt. In der Histologie waren neutrophile Granulozyten sowie eine ausgeprägte hypertrophe Vaskulopathie kleiner Arterien/Arteriolen nachgewiesen worden. Unter der Therapie sei es zu einer deutlichen Befundbesserung gekommen. Seit wenigen Wochen sei die Läsion jedoch deutlich größenprogredient, wuchernd und zunehmend schmerzhaft. Die angepassten Kompressionsstrümpfe seien schmerzbedingt seit einigen Wochen nicht mehr getragen worden.
Vier Jahre zuvor habe der Patient selbstlimitierende Ulzera an beiden Innenknöcheln gehabt. Als Vorerkrankungen bestehen eine COPD Stadium GOLD 4 mit Emphysemlunge und Lungengerüstfibrose und Z. n. mehrfacher Sepsispneumonie, eine arzneimittelinduzierte Osteoporose mit Z. n. mehrfachen Wirbelfrakturen sowie eine rheumatoide Arthritis seit 14 Jahren.
Eine Therapie mit Hydroxychloroquin sei sieben Wochen zuvor aufgrund der Diagnose des Pyoderma gangraenosum auf Etanercept umgesetzt worden. Hierunter sei es zu einer deutlichen Verschlechterung des Befundes gekommen. Zur Zeit der Vorstellung steht aufgrund einer bildgebenden Untersuchung zudem eine fragliche Lungentuberkulose im Raum, welche demnächst abgeklärt werden sollte.
Aufnahmebefund
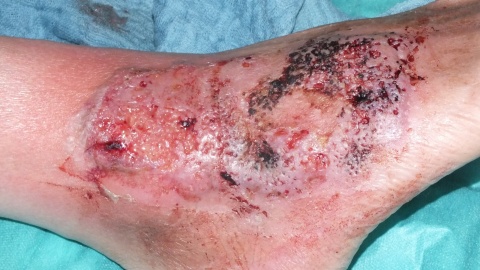
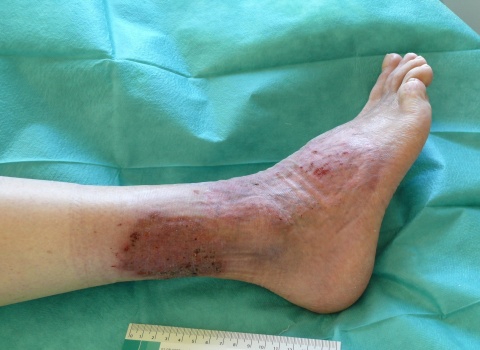
Kachektischer, schmerzgeplagter Patient mit angedeuteter Facies lunata in reduziertem Allgemeinzustand. 13 cm x 6 cm messende, unscharf begrenzte Ulzeration, teils eleviert mit Hypergranulation. Teils livider Wundrand, Mazeration, keine Unterminierung. Überwärmtes Umgebungserythem. Ausgeprägte Corona phlebectatica paraplantaris. Fußpulse seitengleich palpabel, Füße warm.Diagnostik
Bis auf ein erhöhtes CRP 27 mg/l (<5 mg/l) zeigte sich das Routine-Aufnahmelabor unauffällig. Die erweiterte Diagnostik ergab einen deutlich erhöhten Rheumafaktor 345 IU/ml (<15 IU/ml), sowie eine Erhöhung von Anti-CCP > 340 /ml (< 7 U/ ml). Das ANA-Screening war mit einem Titer von 1:320 (<1:100) positiv und zeigte eine granuläre zytoplasmatische Fluoreszenz. ENA-Screening war grenzwertig, SS-A/Ro 2-fach positiv. Ebenso waren das AMA- Screening mit einem Titer von 1:320 (<1:40) und Nachweis von AMA M2, sowie das ANCA-Screening mit einem Titer von 1:100 (<1:10) positive, ohne Nachweis von pANCA oder cANCA. Mittels MTB-Quantiferontest wurde eine Tuberkulose ausgeschlossen.
Die histologische Aufarbeitung der bei Aufnahme entnommenen Probebiopsie zeigte ein neutrophilenreiches Infiltrat, sowie eine Vaskulopathie.
Im Wundabstrich konnte reichlich MRSA nachgewiesen werden, außerdem zeigte sich eine nasale, pharyngeale und rektale MRSA-Besiedlung.
Therapie und Verlauf
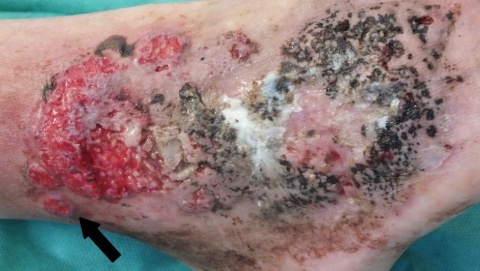
Wir entnahmen erneut Probebiopsien, welche ein neutrophilenreiches Infiltrat passend zu einem Pyoderma gangraenosum zeigten. Hinweise auf eine primäre Vaskulitis oder auf Malignität zeigten sich nicht. Auffallend war die trotz adäquater Lokalanästhesie starke Schmerzhaftigkeit der Probeentnahme. Zudem zeigte sich im Verlauf eine Progredienz des Befundes im Bereich der Biopsie im Sinne eines Pathergie Phänomens.
Die Differentialdiagnose einer Tuberkulose wurde bei negativem Quantiferontest verworfen. Das auffällige Autoantikörperlabor werteten wir in Zusammenhang mit der Histologie und der Klinik am ehesten als mit der rheumatoiden Arthritis assoziiert.
Die Therapie erfolgte probatorisch mit Prednisolon 1 mg /kg Körpergewicht per os unter Gastroprotektion und Osteoporose Prophylaxe. Topisch wurden antiseptische Umschläge und ein Klasse-IV-Steroid unter Okklusion angewendet. Die analgetische Therapie erfolgte mit niedrigpotenten Opioiden sowie Novaminsulfon. Eine kalkulierte antibiotische Therapie wurde mit Ampicillin/Sulbactam intravenös durchgeführt und nach Vorliegen des Resistogramms bei MRSA auf Clindamycin umgestellt. Die Umgebungsrötung sowie die laborchemischen Entzündungszeichen zeigten sich hierunter rückläufig.
Parallel wurde eine MRSA-Sanierung durchgeführt. Nach erfolgter Ernährungsberatung erhielt der kachektische Patient hochkalorische Ernährung. Bei vorbekannter COPD und Bettlägerigkeit führte der Patient zudem selbständig Atemtraining zur Pneumonie Prophylaxe durch.
Im Verlauf konnte bei Befundverbesserung die Prednisolondosis auf 15 mg/Tag reduziert werden; eine Kompressionstherapie, welche anfangs schmerzbedingt nicht toleriert wurde, konnte nach vier Tagen begonnen werden. Als Wundauflage kamen Polyurethan-Schäume und Distanzgitter zum Einsatz.
Nach 21 Tagen entließen wir den Patienten mit deutlich gebessertem Lokalbefund mit der Empfehlung das Prednisolon unter Beibehaltung der topischen Steroidtherapie nach Schema auszuschleichen in die Häuslichkeit.
Wir sahen den Patienten einige Male poststationär bei stabilem Befund, bis er sich nach vier Monaten mit einem Rezidiv erneut stationär vorstellte.
Diskussion
Die vegetierende Form eines Pyoderma gangraenosum ist eine seltene Variante einer ebenso seltenen Erkrankung. Darüber hinaus gibt es keine laborchemischen oder histologischen Zeichen, welche uns eine eindeutige Diagnose erlauben. Wie im oben genannten Fall zu sehen, waren wir uns trotz der vorher bereits einmal gestellten Diagnose sehr unsicher.Auch wenn im Idealfall die Diagnose vor der Therapie steht, ist oft ein pragmatisches Vorgehen vonnöten, um trotz verschiedener Differentialdiagnosen zeitnah mit der notwendigen Therapie zu beginnen. Manchmal erlaubt es sogar erst die Befundentwicklung unter Therapie, sich einer Diagnose sicher zu werden. In diesem speziellen Fall stellten sich einige der Diagnosekriterien[¹] für das Pyoderma gangraenosum erst im Laufe der Therapie heraus.
Tabelle 1: Diagnosekriterien des Pyoderma gangraenosum |
Majorkriterien |
- Klinik: rasch progredient, livider, unterminierter Randsaum, sterile Pustel |
- Ausschluss anderer Ursachen |
Minorkriterien |
- Pathergiephänomen |
- cribiforme Narbenbildung |
- Assoziierte Grunderkrankung (z. B. rheumatoide Arthritis, chronisch entzündliche Darmerkrankung) |
- Histologie: Neutrophiles Infiltrat, lymphozytenreiche Vaskulitis |
- schnelles Therapieansprechen auf Steroide |
Die kursiv geschriebenen Punkte treffen auf den Patienten in der Fallvorstellung zu, die grau markierten Punkte stellten sich erst im Laufe des stationären Aufenthaltes heraus.
Fazit
Oft sind wir im Bereich der Wundtherapie mit Befunden konfrontiert, welche nicht klar einer einzelnen Äthiopathologie zugeordnet werden können. Die meisten der Patienten mit chronischen Wunden sind höheren Alters und oft multipel vorerkrankt; zudem haben sie oft bereits mehrfach Untersuchungen und Therapieversuche hinter sich. Dies stellt sowohl in der Diagnostik als auch in der Therapie eine Herausforderung dar. Zum Beispiel erhielt unser Patient wegen seiner fortgeschrittenen COPD und der rheumatoiden Arthritis bereits Steroide und hatte aufgrund seiner steroidinduzierten Osteoporose schon mehrfach Wirbelkörperfrakturen erlitten.
Oft ist es bei Patienten mit chronischen Wunden notwendig und hilfreich, interdisziplinär vorzugehen. Hierbei werden neben der regelhaften Zusammenarbeit zwischen der Dermatologie, Orthopädie/Unfallchirurgie und Gefäßchirurgie in unserem Wundzentrum auch Innere Medizin, Schmerztherapie, Psychologie, Ernährungsberatung und Sozialdienst hinzugezogen.
Man sieht im oben geschilderten Fall aber auch, dass chronische Wunden sich eben durch ihre Chronizität auszeichnen. Wundpatienten werden häufig oft auch deswegen immer wieder hospitalisiert, weil eine adäquate Versorgung in der Häuslichkeit trotz allen Bemühens nicht immer sicherzustellen ist. Diese Herausforderung ist nur in kleinen Schritten und über eine interdisziplinäre Zusammenarbeit – auch niedergelassenen Ärzten und Pflegediensten – zu meistern.
Anschrift für die Verf.:
Oberstabsarzt Dr. Tina Uhlmann
Fachärztin für Dermatologie, Venerologie und Allergologie
Bundeswehrkrankenhaus Berlin
Scharnhorst Str. 13
10115 Berlin
[email protected]
Fotos: Thilo Pulpanek, Bundeswehrkrankenhaus Berlin
Kommentar: Erstellt in Anlehnung an Su, W. et al. (2004). Pyoderma gangrenosum: clinicopathologic correlation and proposed diagnostic criteria. International Journal of Dermatology, 43(11), 790 - 800.
[1] Su, W. P., Davis, M. D., Weenig, R. H., Powell, F. C., & Perry, H. O. (2004). Pyoderma gangrenosum: clinicopathologic correlation and proposed diagnostic criteria. International Journal of Dermatology, 43(11), 790 - 800.
Datum: 13.06.2018
Quelle: Wehrmedizin und Wehrpharmazie 1/2018