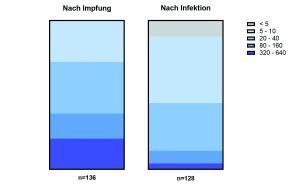
Die körpereigene Immunantwort spielt beim Verlauf einer SARS-CoV-2 Infektion eine entscheidende Rolle. Neben den Antikörpern sind auch sogenannte T-Killerzellen dafür verantwortlich, Viren im Körper aufzuspüren und unschädlich zu machen. WissenschafterInnen des CeMM Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften sowie der Medizinischen Universität Wien zeigten nun in einer Studie, dass SARS-CoV-2 sich durch bestimmte Mutationen für die Immunantwort durch T-Killerzellen unerkennbar machen kann. Die Erkenntnisse der Forschungsgruppen von Andreas Bergthaler, Judith Aberle und Johannes Huppa liefern für die Weiterentwicklung von Impfungen wichtige Hinweise und wurden im Journal Science Immunology veröffentlicht.
Nach einem Jahr Pandemie zeichnet sich für Wissenschaft und Medizin ein immer deutlicheres Bild davon, wie die Immunantwort Menschen vor SARS-CoV-2 schützt. Zwei Akteure spielen dabei eine zentrale Rolle: Antikörper und T-Killerzellen. Während Antikörper direkt an Viren andocken, um diese unschädlich zu machen, erkennen T-Killerzellen virale Eiweiß-Fragmente auf infizierten Zellen und töten diese in der Folge ab, um die Virusproduktion zu stoppen. Immer mehr Studien zeigen, dass sich SARS-CoV-2 durch Mutationen der Antikörper-Immunantwort entziehen kann und damit auch die Wirksamkeit von Impfstoffen beeinträchtigt. Ob solche Mutationen auch T-Killerzellen in ihrer Funktion beeinträchtigen, war bis jetzt nicht geklärt.
Benedikt Agerer im Labor von Andreas Bergthaler (CeMM), Maximilian Koblischke und Venugopal Gudipati in der Arbeitsgruppe von Judith Aberle bzw. Johannes Huppa (beide MedUni Wien) untersuchten nun in enger Zusammenarbeit die Auswirkung von Virusmutationen in sogenannten T-Zell Epitopen, d. h. in Regionen, die von T-Killerzellen erkannt werden. Hierfür sequenzierten sie 750 SARS-CoV-2 Virusgenome von Infizierten und analysierten Mutationen auf ihr Potenzial, T-Zell-Epitope zu verändern.
"Unsere Ergebnisse belegen, dass viele Mutationen in SARS-CoV-2 tatsächlich dazu in der Lage sind. Mithilfe bioinformatischer und biochemischer Untersuchungen sowie Laborexperimenten mit Blutzellen von COVID-19-Patienten konnten wir zeigen, dass mutierte Viren von T-Killerzellen an dieser Stelle nicht mehr erkannt werden können“, so Andreas Bergthaler.
Fokus auf Spike-Protein könnte zu wenig sein
Bei den meisten natürlichen Infektionen stehen mehrere Epitope für die Erkennung durch T-Killerzellen zur Verfügung. Mutiert das Virus an einer Stelle, ist es wahrscheinlich, dass noch andere Epitope die Anwesenheit des Virus verraten. Die meisten der aktuellen Impfstoffe gegen SARS-CoV-2 richten sich ausschließlich gegen das sogenannte Spike-Protein, welches nur eines von 26 Viruseiweißstoffen darstellt. Dadurch reduziert sich auch die Zahl jener Epitope, die grundsätzlich für die Erkennung durch T-Killerzellen zur Verfügung stehen.
„Das Spike-Protein verfügt im Durchschnitt über ein bis sechs dieser T-Zell-Epitope in einem Infizierten. Mutiert das Virus in einer dieser Regionen, steigt das Risiko, dass die infizierten Zellen nicht von den T-Killerzellen erkannt werden“, erklärt Johannes Huppa. Und: Judith Aberle betont: „Vor allem für die Weiterentwicklung der Impfstoffe müssen wir daher genau im Auge behalten, wie das Virus mutiert und welche Mutationen sich global durchsetzen. Aktuell sehen wir wenige Hinweise, dass Mutationen in T-Killerzell-Epitopen sich verstärkt verbreiten.“
Die StudienautorInnen sehen in ihren Daten keinen Grund zur Annahme, dass sich SARS-CoV-2 der Immunantwort des Menschen komplett entziehen kann. Jedoch liefern diese Resultate wichtige Einblicke, wie SARS-CoV-2 mit dem Immunsystem interagiert.
„Darüber hinaus hilft dieses Wissen bei der Entwicklung von effektiveren Impfstoffen mit dem Potenzial, möglichst viele T-Killerzellen über eine Vielzahl von Epitopen zu aktivieren. Ziel sind dabei Impfstoffe, die neutralisierende Antikörper und T-Killerzellen-Antworten für einen möglichst breiten Schutz auslösen“, so die StudienautorInnen.
Die Studie „SARS-CoV-2 mutations in MHC-I restricted epitopes evade CD8+ T cell responses“ erschien in Science Immunology online am 4. März 2021. DOI: 10.1126/sciimmunol.abg6461
AutorInnen: Benedikt Agerer*, Maximilian Koblischke*, Venugopal Gudipati*, Luis Fernando Montaño-Gutierrez, Mark Smyth, Alexandra Popa, Jakob-Wendelin Genger, Lukas Endler, David M. Florian, Vanessa Mühlgrabner, Marianne Graninger, Stephan W. Aberle, Anna-Maria Husa, Lisa Ellen Shaw, Alexander Lercher, Pia Gattinger, Ricard Torralba-Gombau, Doris Trapin, Thomas Penz, Daniele Barreca, Ingrid Fae, Sabine Wenda, Marianna Traungott, Gernot Walder, Winfried F. Pickl, Volker Thiel, Franz Allerberger, Hannes Stockinger, Elisabeth Puchhammer-Stöckl, Wolfgang Weninger, Gottfried Fischer, Wolfgang Hoepler, Erich Pawelka, Alexander Zoufaly, Rudolf Valenta, Christoph Bock, Wolfgang Paster, René Geyeregger, Matthias Farlik, Florian Halbritter, Johannes B. Huppa**, Judith H. Aberle**, Andreas Bergthaler**
*geteilte Erstautorenschaft, **geteilte Studienleitung
Förderung: Die Studie wurde unterstützt durch den Wiener Wissenschafts- und Technologiefonds (WWTF) im Rahmen des WWTF COVID-19 Rapid Response Funding 2020 finanziert, die an Andreas Bergthaler bzw. René Geyeregger vergeben wurden. Benedikt Agerer wurde vom Österreichischen Wissenschaftsfonds (FWF) DK W1212 unterstützt. Mark Smyth und Alexander Lercher sind Inhaber von DOC-Stipendien der Österreichischen Akademie der Wissenschaften Nr. 24813, Nr. 24158 bzw. Nr. 24955). Venugopal Gudipati, Vanessa Mühlgrabner und Johannes B. Huppa erhielten Unterstützung durch den Wiener Wissenschafts- und Technologiefonds (WWTF, LS14-031). Judith H. Abele und Winfried F. Pickl wurden durch den Medizinisch-Wissenschaftlichen Fonds des Bürgermeisters der Stadt Wien unterstützt [Grant COVID003, Grant COVID006]. Christoph Bock und Andreas Bergthaler erhielten durch je einen ERC Starting Grant (Forschungs- und Innovationsprogramm Horizon 2020 der Europäischen Union, Grant Agreement Nummern 679146 bzw. 677006) Finanzierung.
Judith Aberle ist Fachärztin und Professorin für Virologie an der Medizinischen Universität Wien. Sie studierte Medizin an der Universität Wien und absolvierte ihre Facharztausbildung am Zentrum für Virologie, wo sie eine Forschungsgruppe für Virusimmunologie leitet. In ihrer aktuellen Forschung widmet sie sich mit ihrem Team und anderen Forschungsgruppen am Zentrum für Virologie der Charakterisierung von virus-spezifischen T-Zell und Antiköperpopulationen in PatientInnen mit SARS-CoV-2 Infektion und untersucht spezielle SARS-CoV-2 Mutationsmuster in immunsupprimierten PatientInnen sowie deren Bedeutung für den Krankheitsverlauf.
Andreas Bergthaler hat Veterinärmedizin in Wien studiert. Nach seinem Doktorat bei Hans Hengartner und Nobelpreisträger Rolf Zinkernagel an der Universität Zürich und der ETH Zürich folgten postdoktorale Forschungsaufenthalte an der Universität Genf und am Institute for Systems Biology in Seattle. Seit 2011 ist er Forschungsgruppenleiter am CeMM und ERC Start Preisträger.
Johannes Huppa lehrt als Professor Molekulare Immunologie an der Medizinischen Universität Wien. Schwerpunkt seines Forschungsinteresse bildet die hochsensitive Erkennung von Antigenen durch T Lymphozyten. Um diesen Prozess besser zu verstehen, entwickelt und verwendet er gemeinsam mit seinem Team molekulare Mikroskopie-Methoden, wie auch biophysikalische und systembiologische Ansätze.
Das CeMM Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften ist eine internationale, unabhängige und interdisziplinäre Forschungseinrichtung für molekulare Medizin unter wissenschaftlicher Leitung von Giulio Superti-Furga. Das CeMM orientiert sich an den medizinischen Erfordernissen und integriert Grundlagenforschung sowie klinische Expertise um innovative diagnostische und therapeutische Ansätze für eine Präzisionsmedizin zu entwickeln. Die Forschungsschwerpunkte sind Krebs, Entzündungen, Stoffwechsel- und Immunstörungen, sowie seltene Erkrankungen. Das Forschungsgebäude des Institutes befindet sich am Campus der Medizinischen Universität und des Allgemeinen Krankenhauses Wien. www.cemm.at
Die Medizinische Universität Wien (kurz: MedUni Wien) ist eine der traditionsreichsten medizinischen Ausbildungs- und Forschungsstätten Europas. Mit rund 8.000 Studierenden ist sie heute die größte medizinische Ausbildungsstätte im deutschsprachigen Raum. Mit 5.500 MitarbeiterInnen, 30 Universitätskliniken und zwei klinischen Instituten, 12 medizintheoretischen Zentren und zahlreichen hochspezialisierten Laboratorien zählt sie auch zu den bedeutendsten Spitzenforschungsinstitutionen Europas im biomedizinischen Bereich. www.meduniwien.ac.at
CeMM
Forschungszentrum für Molekulare Medizin
der Österreichischen Akademie der Wissenschaften
Lazarettgasse 14, AKH BT 25.3
1090 Wien
Tel.: +43-1/40160-70 092
Mobil: +43-660-8543234
[email protected]
www.cemm.oeaw.ac.at