PERIIMPLANTITIS – DIAGNOSTIK UND THERAPIE
Eine Periimplantitis ist gekennzeichnet durch eine Entzündungsreaktion mit einhergehendem periimplantärem Knochenverlust. Zur Diagnose werden die klinischen Parameter Bluten nach Sondieren (BnS) und Sondiertiefen (ST) in Verbindung mit einer röntgenologischen Verlaufskontrolle herangezogen.
Neben iatrogenen Faktoren, wie unzureichende prothetische Versorgungen, nicht vollständig entfernte Zementreste, ungünstige Implantatpositionierung und operative Komplikationen, spielt die bakterielle Besiedelung freiliegender Implantatoberflächen eine wichtige Rolle bei der Entstehung periimplantärer Erkrankungen. Der therapeutische Ansatz zur Behandlung einer Periimplantitis ist folglich in einer konsequenten Infektionskontrolle durch Biofilmentfernung und in weiteren antientzündlichen Maßnahmen zu finden. Aufgrund der Morphologie der Implantatoberflächen sind jedoch neben einer konservativen Therapie häufig chirurgische Maßnahmen indiziert. Hierzu können resektive oder regenerative Verfahren angewendet werden, um einen weiteren Gewebeverlust im Bereich der Implantate zu vermeiden. Nicht zuletzt stellt jedoch eine konsequente, systematische Vorbehandlung der Patienten vor Implantation und hier insbesondere die Diagnostik einer persistierenden Parodontalerkrankung einen wichtigen Aspekt dar, um den Erfolg einer zahnärztlichen Therapie mit Implantaten sicherzustellen.
Die Versorgung zahnloser Kieferkammregionen und fehlender Zähne durch Implantate stellt seit vielen Jahren eine klinisch bewährte Behandlungsoption dar. Insbesondere unter wehrmedizinischen und einsatzspezifischen Gesichtspunkten kann eine Pfeilervermehrung durch zahnärztliche Implantate einen festsitzenden Zahnersatz ermöglichen.
Aufgrund etablierter Therapieprotokolle bezüglich notwendiger augmentativer Maßnahmen, wie z.B. Sinusbodenelevationen oder der Einsatz unterschiedlicher Implantattypen
(z. B. Kurzimplantate), nimmt die Indikationsbreite für eine Implantatinsertion zur Wiederherstellung der Ästhetik und Kaufunktion stetig zu. Hierdurch gelangen jedoch auch zunehmend Erkrankungen des periimplantären Gewebes in den Fokus der truppenzahnärztlichen Tätigkeit.
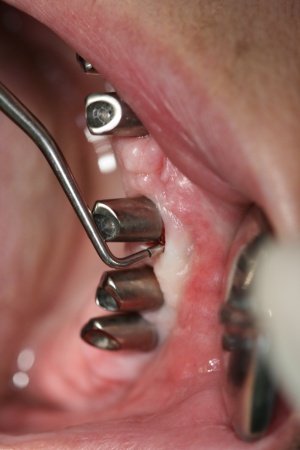
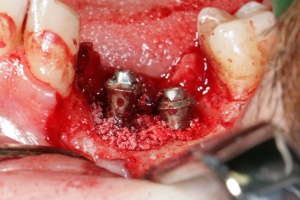
Hierbei muss eine Mukositis, die in Analogie zu einer Gingivitis gesehen werden kann, von einer Periimplantitis abgegrenzt werden. Während bei einer Mukositis lediglich eine Entzündung des periimplantären Weichgewebes mit zumeist vorhandener intrasulkulärer Blutung nachzuweisen ist, zeigt eine Periimplantitis zusätzlich eine Mitbeteiligung des periimplantären Knochengewebes (Abb.1).
Die erhöhte Anfälligkeit inserierter Implantate für periimplantäre Infektionen beruht auf grundsätzlichen Unterschieden insbesondere der Durchtrittsstelle zur Mundhöhle zwischen natürlichen Zähnen und Implantaten. So zeigen histologische Untersuchungen einen vertikalen Kollagenfaserverlauf mit hohem Kollagenanteil im Bereich des Weichgewebssaumes um die Implantatschulter. Aufgrund der fehlenden desmodontalen Verankerung und der damit verringerten Durchblutung zeigt sich eine verminderte Immunabwehr im Bereich der osseointegrierten Implantate, woraus die erhöhte Anfälligkeit für Infektionen der periimplantären Gewebe resultiert.
Die Prävalenz periimplantärer Infektionen wird mit 28 - 43 % angegeben. Als ursächlich gilt neben einer Vielzahl von Risikofaktoren, wie Rauchen, schlechte Mundhygiene, Diabetes mellitus oder persisitierende Parodontitis, die Biofilmbesiedelung der Implantatoberfläche. Hierbei zeigt sich eine ähnliche Zusammensetzung der bakteriellen Flora wie bei natürlichen parodontal erkrankten Zähnen. So lassen sich durch spezifische Verfahren anaerobe Bakterien, Spirochäten und Fusobakterien nachweisen, die eine proinflammatorische Wirtsantwort im Sinne einer Ausschüttung von Interleukin-1 (IL-1) und Tumornekrosefaktor alpha (TNF alpha) auslösen. Diese Mediatoren stimulieren u unter anderem Fibroblasten zur Produktion von Prostaglandinen (PGE-2) und Metallomatrixproteinasen (aMMP-8), welche zu einem Abbau von Alveolarknochen führen.
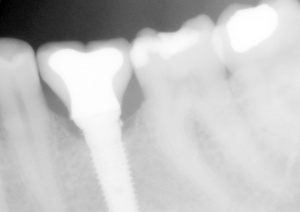
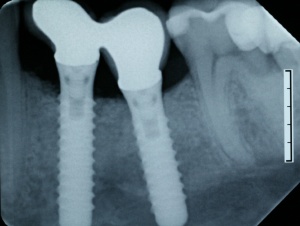
Im Hinblick auf eine erfolgreiche Implantattherapie ist es folglich unabdingbar, eine konsequente Vorbehandlung im Sinne einer systematischen Parodontaltherapie bei einer parodontal erkrankten Bezahnung vor Implantatinsertion durchzuführen. Weitere Faktoren, die eine Periimplantitis begünstigen, sind insuffiziente Suprakonstruktionen (okklusale Fehlbelastungen, eingeschränkte Hygienefähigkeit), ungünstige Implantatpositionen und chirurgische Komplikationen. Eine besondere Bedeutung kommt intrasulkulär verbliebenen Zementresten bei zementierten Suprakonstruktionen zu, die ähnlich wie Konkremente bei natürlicher Bezahnung eine Entzündungsreaktion hervorrufen und einen periimplantären Knochenabbau begünstigen können. Durch eine Röntgenaufnahme nach prothetischer Versorgung lassen sich verbliebene Zementreste erfolgreich erkennen und entsprechend beseitigen (Abb. 2).
Diagnostik
Einer frühzeitigen Diagnostik periimplantärer Infektionen kommt im Hinblick auf die oben geschilderten histologischen Besonderheiten eine wichtige Rolle zu. Hierzu ist es notwendig, regelmäßige klinische und, wenn erforderlich, röntgenologische Befunde zu erheben, um eine frühzeitige Therapie zu ermöglichen. Als entscheidender klinischer Parameter gilt dabei die Messung der Sondierungstiefen. Die Messung kann mit normalen Parodontalsonden mit einer Kraft von 0,2 N erfolgen, wobei keine Schädigung des periimplantären Gewebes eintritt. Um alle Flächen zu berücksichtigen, sollte auch hier eine 6-Punkt-Messung durchgeführt werden. Bei „Platform-Switch“-Implantaten muss bei der Sondierung auf eine streng vertikale Orientierung der Parodontalsonde geachtet werden, um nicht im Bereich der Implantatschulter auf die positive Stufe zwischen Implantat und Abutment aufzutreffen. Erhöhte Sondierungstiefen (> 5 mm) können dabei auf einen periimplantären Knochenabbau hinweisen.
Im Zuge der Sondierungstiefenmessung erfolgt gleichzeitig die Erhebung des Entzündungsparameters „Bluten auf Sondieren“ (Bleeding on Probing = BoP). Als weiterer Parameter kann ebenfalls eine Exsudation oder Suppuration am Implantat erfasst werden, die neben einer vorhandenen Blutung auf ein Voranschreiten der Periimplantitis hinweisen kann. Weitere klinische Kennzeichen einer Periimplantitis können eine Retraktion der Gingiva, Fistelbildungen, periimplantäre Schwellungen oder eine Mobilität des Implantates sein.
Ergeben sich bei der klinischen Untersuchung Auffälligkeiten (erhöhte Sondierungstiefen, Blutung, Suppuration), sollte ergänzend eine Röntgenkontrolle der Implantatregion erfolgen. Als Referenzaufnahme für die Beurteilung des periimplantären Knochenabbaus sollte dabei ein nach Eingliederung der Suprakonstruktion angefertigtes Röntgenbild dienen. Der Zeitpunkt nach Eingliederung der prothetischen Versorgung kann hierbei als Abschluss der osseointegrativen Vorgänge gesehen werden und stellt somit eine Nulllinie bezüglich des postprothetischen Knochenabbaus (postloading) dar. Dieser sollte nach dem Abschluss der Einheilvorgänge und nach prothetischer Versorgung maximal 0,2 mm pro Jahr betragen.
Im Rahmen einer systematischen Implantatnachsorge sollten mindestens einmal jährlich die inserierten Implantate klinisch kontrolliert und bei Bedarf eine röntgenologische Kontrolle durchgeführt werden.
Therapie
Aufgrund der initialen biofilmbedingten Entzündungsreaktion bei periimplantären Infektionen zielen die Therapiekonzepte für Mukositis und Periimplantitis auf eine Beseitigung des Biofilms ab. Hierbei stellt die Dekontamination der mikroporösen rauen Implantatoberfläche hohe Anforderungen an das Behandlungsteam, um eine Progression der Erkrankung zu vermeiden und gleichzeitig eine Regeneration der knöchernen Defektbereiche zu ermöglichen.
Um einen Therapieerfolg zu gewährleisten, sollte auch bei einer Mukositis/Periimplantitis ein systematisches Vorgehen gewählt werden. Da die Mukositis eine Vorstufe zur Periimplantitis darstellt, sollte selbst bei noch unauffälligen Sondierungstiefen und vorhandener periimplantärer Blutung die Beseitigung subgingivaler Plaque durchgeführt werden. Auch bei einer etablierten Periimplantitis gilt es, initial eine subgingivale Belagentfernung durchzuführen, um eine Infektionskontrolle durch Beseitigung des subgingivalen Biofilms zu erreichen. Verwendung finden hierfür Titanküretten oder Scaler, die eine effektive Depuration der Implantatoberfläche ermöglichen. Die Reinigung mit Kunststoffküretten schont zwar die Implantatoberfläche, führt jedoch zu Abrieb auf dem Implantat, wodurch es zu einer Persistenz des entzündlichen Geschehens kommen kann.
Des Weiteren kommen auch Pulverstrahlgeräte mit speziellen Agenzien (Glycinpulver) zur subgingivalen Reinigung zur Anwendung. Hierbei sind einer effektiven Reinigung jedoch bei sehr tiefen und schmalen periimplantären Defekten Grenzen gesetzt.
Für die Politur der Implantatschulter lassen sich handelsübliche Polierkelche mit niedrigabrasiven Polierpasten, die auch im Rahmen der Einsatzvorbereitenden Prophylaxe oder Professionellen Zahnreinigung Verwendung finden, einsetzen.
Aufgrund verschiedener Einflussfaktoren, wie dem Schweregrad der Periimplantitis oder der Beschaffenheit der Implantatoberfläche, ist die alleinige Anwendung nichtchirurgischer Verfahren nur begrenzt erfolgreich. Insbesondere bei Auftreten von Pus sind der nichtchirurgischen Therapie Grenzen gesetzt, wie in Untersuchungen gezeigt werden konnte. Jedoch kann eine vorübergehende Entzündungsfreiheit der periimplantären Weichgewebsmanschette durch den Einsatz topischer oder systemischer Antibiotika erzielt werden. Hierfür sollten allerdings eine gezielte Erregerbestimmung und gegebenenfalls ein Antibiogramm erstellt werden, um einen effektiven Antibiotikaeinsatz sicherzustellen. Nach der nichtchirurgischen Periimplantitistherapie sollten erneut die klinischen Parameter Sondierungstiefen, Bluten nach Sondieren und Suppuration erhoben werden, um die weitere Therapieplanung zu ermöglichen. Zeigen sich im Rahmen dieser Reevaluation stabile, das heißt entzündungsfreie periimplantäre Verhältnisse, so sollte eine engmaschige Nachsorge mit subgingivaler Biofilmentfernung an allen Implantaten und der natürlichen Dentition durchgeführt werden, um eine Reinfektion zu verhindern.
Stellen sich jedoch auch nach der nichtchirurgischen Therapie weiterhin erhöhte Sondierungstiefen, vorhandene periimplantäre Blutungen und gegebenenfalls Suppurationen an den Implantaten dar, so schließt sich die Notwendigkeit einer chirurgischen Periimplantitistherapie an. Hierfür werden in der Literatur verschiedene Therapieoptionen angegeben. Entscheidend für die Auswahl des therapeutischen Verfahrens scheint die Defektkonfiguration zu sein. Die Defekte können dabei circumferent um das erkrankte Implantat angelegt sein mit unterschiedlichen Ausprägungen der vertikalen Komponente (schüssel-, spalt- oder trichterförmig). Des Weiteren kann es zu Kombinationsdefekten mit horizontalem Knochenabbau und zumeist bukkal gelegenen Dehiszenzen kommen. In Untersuchungen konnte gezeigt werden, dass schüsselförmige Knochendefekte mit nur gering ausgeprägter horizontaler Komponente ein größeres regeneratives Potential aufweisen als Kombinationsdefekte.
Zur Defektdarstellung wird ein Zugangslappen präpariert, um unter Sicht eine Beseitigung des Granulationsgewebes und die Reinigung der Implantatoberfläche durchzuführen. Dieser Zugangslappen kann dann nach apikal reponiert werden, um eine Hygienefähigkeit der freiliegenden Implantatanteile zu gewährleisten. Bei Anwendung dieses Verfahrens in Ergänzung mit einer systemischen Antibiose zeigte sich bei 60 % der betrachteten Fälle eine Stabilisierung der periimplantären Läsionen.
Für die Dekontamination der Implantatoberfläche können unterschiedliche Verfahren angewendet werden. So lassen sich Auflagerungen wie im Rahmen der nichtchirurgischen Therapie durch Küretten, Scaler, Lasersysteme und/oder Pulverstrahlgeräte entfernen. Ergänzt werden kann die Reinigung der freiliegenden Implantatwindungen durch Touchierungen mit in Kochsalzlösung oder Zitronensäure getränkten Schaumstoffpellets. Bezüglich der Effektivität der einzelnen Verfahren lassen sich derzeit allerdings keine Unterschiede zwischen der Anwendung von Laser/Pulverstrahlgeräten im Vergleich mit Kochsalzlösung oder Zitronensäure nachweisen.
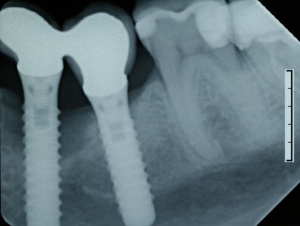
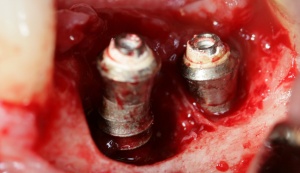
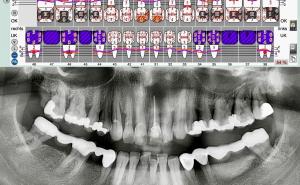
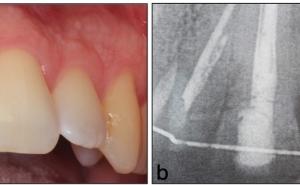
Zur Defektfüllung finden je nach Konfiguration zahlreiche Materialien wie autologes oder xenogenes Knochenmaterial und verschiedenste Membrantypen ihre Anwendung. Eine erfolgreiche Anwendung regenerativer Materialien konnte in einzelnen Fallbeschreibungen gezeigt werden (Abb. 3, 4, 5, 6).
Bei Verlust an horizontaler Knochenkomponente und umfangreichen Dehiszenzen ist eher ein resektives Vorgehen indiziert. Hierbei wird ergänzend zum Zugangslappen eine Bearbeitung der Implantatoberfläche durchgeführt (Implantatplastik). Die Gewindegänge des Implantats werden mit rotierenden Ins-trumenten entfernt und das Implantat im Bereich der periimplantären Läsion geglättet, um eine verbesserte Hygienefähigkeit zu gewährleisten. Zur Bearbeitung eignen sich diamantierte Instrumente (Finierdiamanten), die niedrigtourig verwendet werden sollten, um eine Überhitzung des Implantats zu verhindern. Bei der Bearbeitung sollte eine Kontamination des umliegenden Weichgewebes mit Titanspänen vermieden werden, um ein weiteres Entzündungsrisiko zu minimieren.
Bezüglich der Evidenz nicht-chirurgischer und chirurgischer Therapieverfahren zur Behandlung einer Periimplantitis lässt sich aus der vorhandenen Literatur zurzeit nur ein uneinheitliches Bild ableiten. So stehen Langzeitergebnisse systematischer Studien lediglich über maximal zwölf Monate zur Verfügung und die verschiedentlich publizierten Konzepte beruhen zumeist auf Fallberichten.
Neben den verschiedenen Therapieoptionen spielt jedoch die Vermeidung periimplantärer Erkrankungen eine entscheidende Rolle. Hierbei müssen bereits vor der Implantation unterschiedliche Parameter beachtet werden. So ist neben zahlreichen anderen eine persistierende Parodontitis ein entscheidender Risikofaktor für die Entstehung einer Periimplantitis. Durch eine konsequente parodontale Diagnostik der gesamten Dentition im Rahmen der präimplantologischen Planung kann dieses Risiko deutlich reduziert werden. Nach Implantation und insbesondere nach einer erfolgten Periimplantitistherapie sollte ein ausreichend engmaschiges Nachsorgeintervall (drei bis zwölf Monate) unter Berücksichtigung der Risikofaktoren, wie Allgemeinerkrankungen (Diabetes mellitus) Tabakkonsum, klinische Parameter, gewählt werden, um einer Erkrankung der periimplantären Gewebestrukturen oder einem Rezidiv vorzubeugen.
Datum: 28.06.2013
Quelle:
Wehrmedizin und Wehrpharmazie 2013/2
Wehrmedizin und Wehrpharmazie 2013/2