ENTZÜNDLICHE ZAHNBETTERKRANKUNGEN BEI SOLDATEN
AKTUELLE PARODONTALE BEHANDLUNGSZIELE UND BEHANDLUNGSMÖGLICHKEITEN UNTER BEACHTUNG VON KOSTEN-NUTZEN-ASPEKTEN
Die Identifikation und schnelle Behandlung von Hochrisikopatienten für Karies und Parodontitis ist das wichtigste Ziel des zahnärztlichen Dienstes einer modernen einsatzorientierten Armee im Heimatland. In der Bundeswehr wird durch die jährliche einsatzbezogene Untersuchung zur Dentalen Fitness ein wichtiger Beitrag zu dieser nicht zivil dargestellten zahnmedizinischen Diagnostik geleistet.
Seit Ende der 80er Jahre ist in Deutschland durch freiwillige frühkindliche Untersuchungen, Kindergartenbetreuung durch Zahnärzte, Bewerbung und Verbreitung von fluoridierter Zahnpasta und Interdentalraumreinigung mit Zahnseide oder Zwischenraumbürsten sowie Einführung kostenfreier individualprophylaktischer Leistungen für Kinder und Jugendliche ein erheblicher erfreulicher Kariesrückgang eingetreten. Als zahnmedizinische Volkskrankheit Nr.1 rückte damit die Parodontitis, die inzwischen bis zum 65. Lebensjahr für den größten Teil des Zahnverlustes verantwortlich ist, in den Vordergrund des vorbeugenden Behandlungsbedarfes in Deutschland.
Durch die Einführung der Parodontologie neben der Oralchirurgie als eigenständige fachzahnmedizinische Disziplin Anfang der 90er Jahre wurde dieses frühzeitig durch den Sanitätsdienst der Bundeswehr berücksichtigt. Für die drei Spezialisten für Parodontologie an den Bundeswehrkrankenhäusern Berlin, Hamburg und Koblenz steht seit Jahren die Weiterentwicklung der Zahnerhaltungsfähigkeit durch Truppenzahnärzte zur Vermeidung von Zahnverlust im Vordergrund der Bemühungen. Durch curriculare mehrwöchige Fortbildung entsprechend den Vorgaben der Bundes- und Landeszahnärztekammern werden jährlich 18-24 Allgemeinzahnärzte an der Sanitätsakademie der Bundeswehr im zahnärztlichen Dienst der Bundeswehr hierfür fortgebildet. Durch Allgemeinzahnärzte sollen damit zukünftig alle leichten und mittelschweren Parodontalerkrankungen am Heimatstandort behandelt werden können. Die nach Zahnentfernung häufig notwendige kostenund zeitintensive Versorgung von Zahnlücken mit Zahnersatz und Zahnimplantaten, die im Auslandseinsatz nicht durchgeführt werden kann, tritt bei immer höheren Auslandseinsatzbelastungen damit zunehmend in den Hintergrund.
Die Bedeutung ihrer Parodontalerkrankungen für das tägliche Leben und die militärische Einsatzfähigkeit wird heute von kritischen Patienten höher eingeschätzt als vor 25 Jahren Zahnbeweglichkeit und (rezessionsbedingte Dentin)-Hypersensibilität, genauso wie funktionelle Kau-Limitationen als Folge erhöhter Zahnbeweglichkeit und Überempfindlichkeit, Dyskomfort durch Schmerz oder Dys- Stress z.B. bei verändertem Lächeln, Behinderung (physisch, psychosozial und sozial) durch Mundgeruch spielen eine große Rolle bei der Nachfrage nach Therapie (O’Dowd et al. 2010). Im Sanitätsdienst ist derzeit eine Betreuungssituation von einem Fachzahnarzt/ Spezialisten für Parodontologie für 35.000 Soldaten zur Behandlung schwerer Parodontalerkrankungen und Entzündungen an Implantaten vorgesehen. Eine kassenzahnärztliche zivile Abstützung ist derzeit aufgrund der fehlenden flächendeckenden Versorgungssituation in Deutschland (ca.150 Fachzahnärzte/Spezialisten) nicht gegeben.
Ätiologie und Pathogenese der Parodontitis
Eine Parodontitis ist eine Entzündung des Zahnhalteapparates. Sie gehört zu den häufigsten Erkrankungen des Menschen. Die Entstehung einer Parodontitis beruht auf dem Zusammentreffen ungünstiger Faktoren des individuellen Lebensstiles (Rauchen, Stress, Bluthochdruck, Ernährung, Übergewicht, Diabetes, medikamentenbedingte Mundtrockenheit), umgebungsbedingter Einflüsse in der Ausbildung einer bakteriellen Infektion durch die Bildung und Wirkung von Biofilmen auf der Zahnwurzel, das umgebende Bindegewebe und parodontalen Knochen sowie genetischer Einflüsse zur Infektionsantwort des menschlichen Wirtes.
Seltene aggressive Formen der Parodontitis führen unbehandelt schon bei jungen Erwachsenen zu Zahnverlust. Ansonsten tritt dieser erst später auf, wenn die Parodontitis nicht erkannt und behandelt wird. Dies dürfte bei ca. 80% der zivilen deutschen Bevölkerung derzeit der Fall sein. Eine Parodontitis beginnt immer mit einer Zahnfleischentzündung (Gingivitis). Diese ist für den Patienten nur schwer zu erkennen. Am ehesten bemerkt er eine erhöhte Neigung zu Zahnfleischbluten, auch kann das Zahnfleisch geschwollen sein und an den Zähnen ist oft ein verfärbter bakterieller Belag zu sehen.
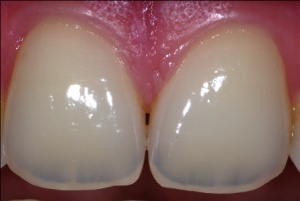
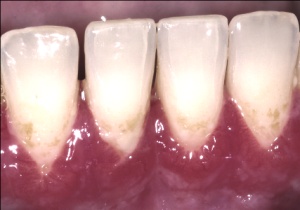
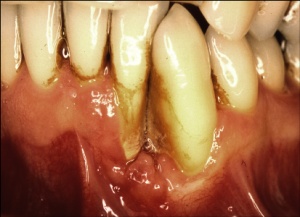
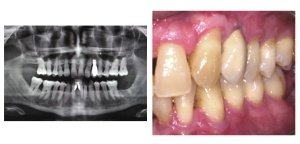
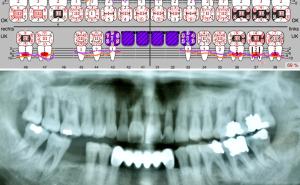
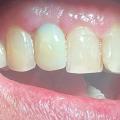
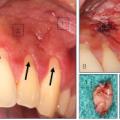
Aus der Gingivitis kann sich eine Parodontitis entwickeln, ohne dass die Patienten deutliche Zeichen davon wahrnehmen (Abb.1, 2, 3). Außer gelegentlich blutendem Zahnfleisch treten evtl. auf: Mundgeruch, Änderung der Zahnstellung, länger werdende und gelockerte Zähne sowie gelegentlich Schmerzen. Parodontitis wird häufig erst im Alter von 40 oder 50 Jahren entdeckt, obwohl die ersten Krankheitszeichen durch jeden curricular fortgebildeten Zahnarzt früher feststellbar sind.
Wird die Entzündung nicht gestoppt, kann sie auf den Kieferknochen übergreifen und schubweise zu dessen Abbau führen. Es kommt zum Zahnverlust. Parodontitis ist die häufigste Ursache für Zahnverlust mit all seinen Konsequenzen.
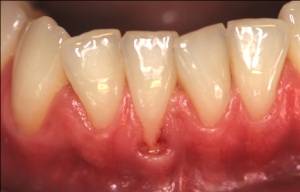
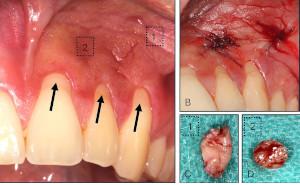
Unbehandelter Zahnverlust ist im sichtbaren Bereich neben der Beeinflussung der Sprachund Lautbildung mit erheblichen ästhetischen Einbußen verbunden (Abb. 3, 4). Zahnverlust im Seitenzahnbereich kann zur Veränderung der Nahrungsaufnahme führen. Die Folge von Zahnverlust ist daher häufig die Notwendigkeit von kostspieligen und zeitaufwendigen Zahnersatzanfertigungen (Brücken, Prothesen) oder chirurgischen Maßnahmen zum Einsetzen künstlicher Zahnwurzeln (Implantate) (Abb. 5).
Weitere Folgen einer unbehandelten Parodontitis können ein erhöhtes Risiko für Komplikationen während der Schwangerschaft (Präeklampsie, Frühgeburten und niedriges Geburtsgewicht) sowie ein erhöhtes Risiko für Herzerkrankungen und Diabetesentwicklung besonders bei übergewichtigen Personen sein.
Eine nicht behandelte Parodontitis hat ebenfalls Einfluss auf rheumatische Erkrankungen, Osteoporose und einige Tumorerkrankungen.
Moderne parodontale Diagnostik
Subjektive klinische Untersuchung
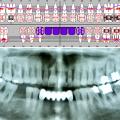
Basis der Parodontaldiagnostik ist die Erhebung der parodontalen Sondiertiefen, Attachment- Level, Plaque-Index, Bluten nach Sondieren und die radiologische Darstellung des parodontalen Knochenabbaus. Vorteile dieser Untersuchungsverfahren sind die schnelle Information bezüglich des aktuellen Schweregrades der Parodontalerkrankungen (Polson AM und Goodson JM 1985). Eine Zunahme parodontaler Sondiertiefen im Zeitraum von 12 Monaten wurde für Bundeswehrsoldaten mit geringer Parodontitis ohne parodontale Therapie in einem Anteil von 39%, bei schwerer Parodontitis in 78% dargestellt (Müller HP et al. 1997).
Fehlendes Bluten nach Sondieren gilt als bester Hinweis für fehlende aktuelle Parodontitisprogression (Morohai N et al. 2007). Nachteile sind allerdings, dass diese Verfahren zeitintensiv und wenig Aussagen zur Krankheitsaktivität z.B. in einem Auslandseinsatz möglich sind sowie eine geringe Akzeptanz (aufgrund limitierter Honorierung) in der allgemeinzahnärztliche Praxis vorliegt (Morgan RG J 2001). Die fehlende / Unter-Diagnostik führt zu geringer Therapiehäufigkeit.
Biomarker-Nachweis
In der subgingivalen Plaque wurden bis heute über 1200 hauptsächlich orale Bakterien mit 19.000 Phylotypen (Keijser BJ 2008) nachgewiesen (Tab. 1). Spezifische Parodontalpathogene erklären meist nur die ca. 20% schweren und akuten Parodontitisfälle (Grossi SG et al.JP1994:65:260-267). Für die Identifikation komplexer normalerweise nicht-pathogener Bakterien, die für die individuelle Pathogenese verantwortlich sind, werden heute mit verschiedenen kommerziellen Testverfahren 8- 10 Tage benötigt. Hierdurch ist die Beobachtung von dynamischen mikrobiologischen Veränderung möglich geworden.
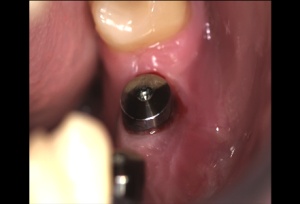
Unter der verschiedenen genetischen Biomarkern (Tab. 2) ist derzeit die Prevalenz des Interleukin 1 (IL-1) Polymorphismus bei verschiedenen Parodontalerkrankungen am besten untersucht. Bei 26% 18-25 jähriger Soldaten mit nur geringer Parodontitis, 49% der Patienten mit schwerer Parodontitis (Eger et al. 2002) und 54% Patienten, die an Zahnimplantaten eine Periimplantitis (Abb. 6) entwickelt haben, wurden Risikoallele in den Genen für das entzündungsfördernde Interleukin1 (IL-1A/B) gefunden. Im Gen für den entzündungshemmenden Interleukin-1-Rezeptorantagonisten (IL-1RN) wurde ein entsprechendes günstiges Risikoallel bei 38% der Periimplantitispatienten, 41% der Patienten mit schwerer Parodontitis, aber 52,9% unserer jungen Soldaten mit nur geringer Parodontitis festgestellt.
Aktuelle epidemiologische Daten zur Häufigkeit und Schweregrad der chronischen Parodontitis
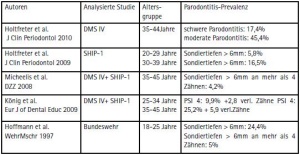
Entsprechend der aktuellen epidemiologischen Untersuchungen durch die Bundeszahnärztekammer / IDZ Köln (DMS IV-Studie), der Europäischen Union in Pommern (SHIP-1) und bundeswehreigener Datenerhebungen ergibt sich derzeit der Anhalt für eine Parodontitishäufigkeit von 4-10% schweren Erkrankungsfällen für die Bundeswehr relevanten Altersgruppen von 18-45 Jahren (Tab. 3). Zusammenfassend wird von den verschiedenen Autoren festgehalten, dass die Prevalenz Deutschland der behandlungsbedürftigen schweren und moderaten Parodontitis höher als in Westeuropa und den USA ist (Holtfreter et al. 2009, 2010). Die Anzahl der durchgeführten Parodontalbehandlungen ist in Deutschland sehr gering.
Derzeit geht die Bundeszahnärztekammer und Kassenzahnärztliche Bundesvereinigung davon aus, dass lediglich ca. 10% der notwendigen Parodontalbehandlungen durch Zahnärzte in Deutschland durchgeführt werden. Gründe hierfür sind z.B. die unzureichende Honorierung parodontaltherapeutischer Maßnahmen und die geringe Zahl an dreijährig in Vollzeitform weitergebildeten Fachzahnärzten für Parodontologie/DGP-Spezialisten für Parodontologie (König et al. 2009). Für die USA wurde aktuell eine ideale Versorgungssituation von einem Parodontologen auf ca. 30.000 erwachsene Einwohner empfohlen, um Zahnverlust und kostenintensiven prothetischen Versorgungen vorzubeugen (Waldman et al. 2009).
Ziele moderner risikoorientierter parodontaler Therapie
Adaequate Therapie und risikoorientierte Nachsorge über 15 Jahre führen bei Patienten mit niedrigem und hohem Risiko zu keinem nennenswerten Zahnverlust (Rosling B et al. 2001). Die WHO formuliert für Gesundheitssysteme wie in Deutschland, dass 20 Zähne über das gesamte Leben erhalten werden können. Das Behandlungsziel jeder zahnärztlichen Behandlung ist daher auf die Vermeidung von Zahnverlust ausgerichtet.
Auf den einzelnen Soldaten und seine Auslandsdienstverwendungsfähigkeit bezogen gilt als parodontales Behandlungsziel, dass keine Zahnfleisch-Resttaschen über 5 mm, kein Pusaustritt, nur gelegentliches Bluten nach Sondieren (< 25%), niedriger Plaquebefall (< 30%), eine nur geringfügige Beeinträchtigung der Ästhetik, Schmerzfreiheit und befriedigende Funktion bestehen. In Fällen in denen auf keine fach- und truppenzahnärztliche Behandlung zurückgegriffen werden kann, sind ungünstigere Parameter in Kauf zu nehmen, die mit einem deutlich erhöhten Risiko für zahnärztliche Notfälle im Einsatz behaftet sind.
Parodontale Therapie
Es gibt keine einheitliche Meinung, wie der Behandlungserfolg erzielt wird. Die Therapie umfasst heute schwerpunktmäßig folgende Maßnahmen:
- Spülung der Wurzeloberfläche um Endotoxine abzuwaschen (Moore J et al. 1986)
- Reduzierter Instrumentenanpressdruck auf der Wurzeloberfläche (Ultraschall etc) (Smart GJ et al. 1990), um eine ergonomische Arbeitssituation mit längerer Nutzungszeit durch Vermeidung von Zwangshaltungen beim Behandlungsteam zu erzielen (Wunderlich et al. 2010)
- Full-mouth one-stage Disinfection – um Rekolonisation von Bakterien zu erschweren (Quirynen M et al. 1995) – um Behandlungszeit zu verkürzen (Tomasi C, Wennström JL. 2009)
- Reduktion oder idealerweise Elimination von Parodontalpathogenen (Socransky SS und Haffajee AD 2005)
- Systemische Antibiose bei Aggregatibacter actinomycetemcomitans, P. gingivalis und T. forsythia assoziierter Parodontitis zusätzlich zur mech. Biofilmentfernung (rev. Herrera D et al. 2008)
- Photodynamische Therapie z.B. zur Behandlung von Fusobacterium nuclatum assoziierten Parodontalerkrankungen (Sigusch et al. 2010)
- Einsatz von Probiotika: Die Kombination von S. sanguis, S. salivarius und S. mitis nach der Wurzelglättung kann die Rekolonisation von Parodontalpathogenen verzögern
- Prebiotika (nichtverdaubare Kohlenhydrate) zur Erleichterung der Ansiedelung von probiotischen Spezies (rev. Stamatova I und Meurman JH 2009)
- Stimulation von körpereigenen oralen antimikrobiellen Peptiden (Peptidantibiotika).
Der hierfür benötigte Zeitansatz liegt bei Behandlung in den hierfür ausgestatteten parodontologischen Behandlungszentren der Bundeswehr bei 8-11 Wochen und ist damit ca. 50% durch strukturelle und organisatorische Maßnahmen kürzer als im zivilen kassenzahnärztlichen Versorgungsbereich.
Kosten-Nutzen-Relation parodontaler Therapie unter wehrmedizinischen Aspekten
Erfolgreiche Parodontitis-Therapie berücksichtigt verändernde "Lifestyle‘s" im Leben, da das Risiko für das Wiederauftreten einer Parodontitis immer von einem empfänglichen Wirt abhängt: Komplexe Behandlungsanforderungen bestehen und psychologische Aspekte der Wertigkeit von zahnärztlicher Therapie verändern sich (Burke BL 2004, Rubak C et al. 2005). Geringere Kosten, feste Zähne, eine gute Kaufähigkeit und die Vermeidung von Zahnersatz gelten weltweit für die Patienten als günstige Parameter zum Vergleich verschiedener Therapieverfahren. Höhere Kosten, Dentinhypersensibilität, die Gefahr von Antibiotikaresistenzen und eine ungünstige Ästhetik sollten aus Patientensicht vermieden werden. Mittels klinischer Parameter wie z.B. dem Entzündungsparameter Bluten nach Sondieren, der parodontalen Sondiertiefe / Klinischer Attachmentlevel und stabilem röntgenologischen Attachmentlevel sowie der beanspruchten Behandlungszeit erfolgt zumeist die Relationsbewertung durch die zahnärztlichen Behandler (Brägger U 2005, Antczak-Bouckoms AA und Weinstein MC 1987).
Parodontitisaufklärung und Life-Style- Faktor: Mundhygienemotivation und Instruktion
Bisher wurde nur selten die exakte Zeit berechnet, die notwendig ist, um Parodontitispatienten eine gute Mundhygiene beizubringen. Der durch Bellini (1973) unabhängig von der Zahnzahl erfasste Zeitansatz 72 Minuten für Erlernung einer effektiven Mundhygiene bei Erwachsenen kann durch Information der Massenmedien heute in westlichen Ländern ggf. reduziert werden (Gjermo P. JCP 2005). Eine nur geringe Zeitersparnis wird durch zusätzliche Gruppenaufklärung, Elterneinbindung gegenüber vereinfachten Programmen erzielt (Buischi Y et al. 1994, Hugoson A et al. 2003, Mayer MPA et al. 2003). Motivations- Interviews erzielen ähnliche Ergebnisse zur Complianceverbesserung (rev.: Burke BL et al. 2004, Rubak S et al. 2005). Elektrische Zahnbürsten haben effektivere häusliche Hygienemaßnahmen zur Folge (rev.: Robinson PG et al. 2005, Roscher T et al. 2004). Allerdings sind im Einsatz elektrische Zahnbürsten, insbesonders aufgrund ihrer Größe, nur eingeschränkt nutzbar.
Parodontitisaufklärung und Life-Style- Faktor: Ernährung
Für Soldaten im Einsatz ist von größter Bedeutung, sich über mehrwöchige Zeiträume auch ohne Mundhygieneartikel und mit einfachen Nahrungsmitteln zu ernähren. Wenn hierbei für bis zu 4 Wochen auf raffinierte Zucker z.B. im Rahmen einer Steinzeitdiät verzichtet werden kann, sind eine Reduktion der parodontalen Entzündungsreaktion auf Sondieren und keine Sondiertiefenerhöhung trotz stärkerer subgingivaler Plaquebildung gezeigt worden (Baumgartner et al. 2009).
Parodontitisaufklärung und Life-Style- Faktor: Rauchen
Raucher erkranken deutlich häufiger an einer Parodontitis als Nichtraucher. Zahnfleisch und auch Knochentransplantate sowie künstliche Zahnwurzeln (Implantate) heilen bei Rauchern wesentlich schlechter ein als bei Nichtrauchern. Der Verlauf der Parodontitis ist bei Rauchern deutlich schwerer; der Gewebeabbau erfolgt bei ihnen wesentlich schneller. Dadurch werden die Zähne schneller locker und gehen häufiger verloren. Raucher sprechen auf die Behandlung der Parodontitis schlechter an als Nichtraucher. Es gibt Parodontitisfälle, die trotz Behandlung nicht ausheilen. Bei mehr als 90 % dieser Fälle handelt es sich um Raucher.
Rauchentwöhnung über einen Zeitraum von 12 Monaten nach Parodontaltherapie führt zwar zu keiner zusätzlichen Reduktion von Sondiertiefen, aber zu einer Zunahme an verschiedenen anderen günstigen Bakterienarten (Fullner et al. 2009).
Subgingivale Zahnsteinentfernung
Eine bestehende Parodontitis kann durch eine systematische Behandlung meist zum Stillstand gebracht werden. Grundlage jeder Behandlung ist dabei die vollständige Beseitigung der verursachenden bakteriellen Plaque.
- Ultraschallanwendung ist bei einwurzeligen Zähnen schneller als mit Handinstrumenten (rev.: Tunkel et al. 2002).
- Zusätzlicher Einsatz lokaler (teuer) und systemischer (preiswert) Antibiotika verbessert (geringgradig) Kosten-Nutzen-Relation bei schwerer und refraktärer Parodontitis (rev. Herrera D et al. 2008, Mombelli A 2008, Niederman R et al. 2002).
- Full mouth Disinfection mit system. Antibiose verbessert Kosten-Nutzen-Relation (Lang NP et al. 2008: 35, Mestnik MJ et al. 2010).
- Access-Lappen-OP: Korrektive (chirurgische) Phase: In manchen Fällen ist ein kleiner chirurgischer Eingriff notwendig, um Zahnsteinreste und Bakterien, die in schwer zugänglichen Zahnfleischtaschen und Wurzelgabelungen (Furkationen) verblieben sind, zu entfernen. Hierbei werden in örtlicher Betäubung die Wurzeloberflächen unter Sicht gereinigt, um möglichst jeden Bakterienschlupfwinkel zu erfassen. Bei größerem Knochenverlust besteht dabei außerdem die Möglichkeit, diesen durch spezielle Behandlungsmethoden teilweise zu reparieren (sog. regenerative Verfahren). Der wichtigste postoperative Erfolgsfaktor ist optimale Plaquekontrolle (Rosling B et al. 1976) und der wichtigste postoperative Misserfolgsfaktor eine mangelhafte Plaquekontrolle (Nyman S et al. 1977). Das einfachste und preiswerteste OP-Verfahren bei mangelhafter Plaquekontrolle ist daher die Gingivektomie. OP-Verfahren sind auch abhängig von zu erwartender Dentinhypersensibilität und Ästhetik zu wählen. Heute meist nur bei fachzahnärztlicher Therapie mögliche Gewinne von über 4 mm Attachment mit Regeneration von Zahnhalteapparat setzen ein hohes Maß an Übung sowie meist mikrochirurgische Techniken und ein stringentes postoperatives Behandlungsmanagement (häufig 7 Nachsorgetermine in den ersten 12 postoperativen Wochen) und einen vollständigen Verzicht auf Tabak voraus. Derzeit ist diese Therapie im Einzugsbereich der Bundeswehrkrankenhäuser möglich.
Unterstützende Parodontitistherapie (UPT)
Eine lebenslängliche risikoorientierte UPT ist bei ehemaligen Parodontitispatienten notwendig, um Zahnverlust zu vermeiden (Eickholz P et al. 2008). Der langfristige Erfolg der Parodontalbehandlung hängt von der Mitarbeit bei der täglichen Mundhygiene und von der regelmäßigen Betreuung durch das zahnärztliche Praxisteam ab. Im Rahmen der Nachsorgeuntersuchungen werden Zähne und Zahnfleisch kontrolliert (z. B. Messung der Zahnfleischtaschen) und professionell gereinigt. Die Patienten erfahren dabei auch, an welchen Stellen sie Ihre Mundhygiene noch verbessern sollten. Die Häufigkeit der Nachsorgetermine richtet sich nach dem Schweregrad der Erkrankung und dem individuellen Erkrankungsrisiko des Patienten.
Bei guter Mundhygiene können jährliche Intervalle mit subgingivaler Reinigung ausreichen (Beirne P et al. 2007).
Bessere Behandlungsergebnisse werden in (Parodontitis-risikoorientierten) Spezialistenpraxen gegenüber Generalistenpraxen erzielt (Gaunt F et al. 2008: 35). Noncompliance führt aber auch bei Behandlung durch Spezialisten zum Misserfolg (Nyman S et al. 1977).
Eine Risikokalkulation zwischen den verschiedenen Behandlungssitzungen erfolgt unter Berücksichtigung des prozentualen Anteils des Blutens nach Sondieren, der Anzahl von Sondiertiefen >5mm, der Zahl der verlorenen Zähne (max. 28), des Attachmentverlusts von Zahnflächen mit >4mm auf Röntgenaufnahmen (RAL) sowie vorhandener genetischer Risikofaktoren und des Tabakkonsums. Bei Verschlechterung der Parameter erfolgt eine Verkürzung der Behandlungsabstände, bei Verbesserung eine Verlängerung.
Lokale Antibiose in der UPT erhöht den Preis und das Risiko für Antibiotikaresistenzen (Slots J und Jorgensen MG 2000). Sie sind daher auf die Akutbehandlung z.B. vor und während Auslandseinsätzen zu beschränken, wenn keine erregerassoziierte behandlungsbegleitende systemische Antibiose möglich ist. Von einem Parodontologen können in Zusammenarbeit mit einer Dentalhygienikerin ca. 375 Patienten mit vormaliger Parodontitis langjährig nachgesorgt werden (30 Jahres- Ergebnisse n. Axelsson et al. 2004).
Langfristige parodontale Behandlungsergebnisse bei Soldaten mit schwerer chronischer oder aggressiver Parodontitis
Aus der Vielzahl subgingivaler Bakterienspezies weisen einige biochemische Eigenschaften auf, die für die Pathogenese entzündlicher Parodontalerkrankungen entscheidend sind.
Die mikrobiologische Diagnostik dient im wesentlichen zur Auswahl einer auf die vorliegende Infektion abgestimmten Antibiotikatherapie.
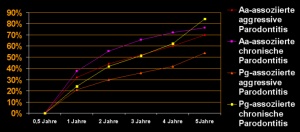
Ziel einer Untersuchung war es, die Bedeutung prospektiver longitudinaler mikrobiologischer Nachweise von Aggregatibacter actinomycetemcomitans (Aa) und Porphyromonas gingivalis (Pg) auf klinische Untersuchungsparameter für den langfristigen Erfolg systematischer Parodontaltherapie fünf Jahre nach mechanischer antiinfektiöser Therapie mit begleitender systemischer Antibiose bei aggressiver und chronischer Parodontitis zu bestimmen (Weyer et al. 2007).
Im Rahmen der systematischen nicht-chirurgischen Parodontalbehandlung wurden 289 Patienten (261 Männer, 28 Frauen) mit aggressiver (n: 139) oder generalisierter schwerer chronischer Parodontitis (n: 150) nach mikrobiologischem Erregernachweis (IAI-Padotest 4.5, Zuchwil, CH) zusätzlich zur nichtchirurgischen Parodontaltherapie (Full Mouth Scaling and Root Planing und zusätzlicher 6- wöchiger häuslicher Chlorhexidin Anwendung) unterstützend antibiotisch behandelt. Im Falle des Nachweises von Aa erfolgte die Antibiose mittels Amoxicillin (3x500mg/Tag) und Metronidazol (3x400mg/Tag) für eine Woche, bei Nachweis einer Infektion mit Pg (ohne Aa-Nachweis) mit Metronidazol (3x400mg für 10 Tage). Bei allen Patienten erfolgte nach 6 Wochen und später in 3-6 monatigen Abständen die unterstützende Parodontitistherapie (UPT) mit mikrobiologischen Untersuchungen.
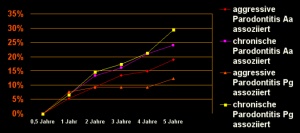
In 19% einer vormals Aa-assoziierten aggressiven und 24% einer chronischen Parodontitis konnte postoperativ nach mehr als 6 Monaten Aa erneut nachgewiesen werden und kam es in der Folge zu einem klinischen Rezidiv. In 12% einer vormals Pg-assoziierten aggressiven und 29% einer chronischen Parodontitis wurden spätere Aa-Infektionen nachgewiesen, die ebenfalls mit einem klinischen Rezidiv verbunden waren, das umgehend therapiert wurde. Pg-Nachweise waren unabhängig vom Antibioseschema in der Mehrheit der Fälle innerhalb eines Jahres wieder positiv und ohne Aa-Nachweis in 7% innerhalb von 5 Jahren mit einem Parodontitisrezidiv assoziiert (Abb. 7 und 8).
Eine mikrobiologische Diagnostik ist in der klinischen Praxis nur dann sinnvoll, wenn sich aus ihr bei Vorliegen eines lokalen Parodontitis- Rezidives eine therapeutische Konsequenz ergibt und eine günstige Kosten-Nutzen-Relation gewahrt bleibt. Positive Nachweise von Aa sind in allen Untersuchungsgruppen mit klinischen Rezidiven verbunden gewesen. Eine Elimination von Pg war mit beiden systemischen Antibiotikaschemata nur in wenigen Fällen langfristig möglich.
Zur frühzeitigen Erkennung und Vermeidung von Parodontitisrezidiven ist bei Patienten mit vormals weit fortgeschrittener Aa und Pg-assoziierter Parodontitis eine risikoorientierte zeitgerechte unterstützende Parodontitistherapie mit Dokumentation von Sondiertiefen und Attachmentwerten zur Vermeidung von Parodontitisrezidiven und damit möglichem Zahnverlust sinnvoll.
Folgerungen und Vorschläge zur Verbesserung der Dentalen Fitness der Soldaten
Das Wissen in der Parodontologie gemessen an der Zahl an Publikationen in peer-reviewed Fachzeitschriften verdoppelte sich 1950 nach 25 Jahren, im Jahre 2010 bereits alle 4-5 Jahre (Chapple et al. 2010). Die erfolgreiche Parodontalbehandlung umfasst heute die Einflechtung verschiedener internistischer Befunde in das Behandlungskonzept. Erfolgreiche Parodontaltherapie hat durch die Reduktion von Entzündungsparametern günstige Einflüsse auf Herz-Kreislauferkrankungen, Diabetes- und Rheumatherapie ebenso wie die Vermeidung vor Frühgeburten. Ergebnisse der Grundlagenforschung müssen daher ortsnah in die klinische truppen(zahn)medizinische Praxis von DGP-Spezialisten/ Fachzahnärzten für Parodontologie durch Fortbildung für Truppenzahnärzte als Generalisten "übersetzt" werden. Hierzu dienen zunächst die parodontologischen Behandlungszentren an den Bundeswehrkrankenhäusern Berlin, Hamburg und Koblenz.
Die Kosten-Nutzen-Effektivität für Spezialisten und Generalisten ist unterschiedlich und muss für jedes neue und zusätzliche Therapieverfahren ständig neu bewertet werden. Dies gilt insbesonders bei der Behandlung von Patienten mit allgemeinmedizinischen Risikofaktoren, aggressiver Parodontitis und Patienten, bei denen eine Regeneration von Zahnhalteapparat zum langfristigen Zahnerhalt notwendig ist.
Psychologie, Patientenverhalten und Compliance sollten zur Verbesserung parodontaler Behandlungsergebnisse im Rahmen eines Qualitätsmanagements praxisspezifisch berücksichtigt werden (Chapple ILC 2009).
In der ganzheitlichen Zahnmedizin ist der mündige Patient im Zentrum der Aufmerksamkeit. Zahnärztliche Diagnostik und Therapie berücksichtigen das individuelle Schicksal, dienstliche Anforderungen und Pflichten sowie die individuellen Möglichkeiten des kranken und hilfsbedürftigen Soldaten.
Datum: 17.01.2011
Quelle: Wehrmedizin und Wehrpharmazie 2010/4