Auswirkungen des Designs von Anti-G-Anzügen auf die Lungenfunktion bei Piloten von Hochleistungsflugzeugen
Influence of anti-G suit-design on pulmonary function of fighter pilots
Aus der Fachabteilung I¹, Fürstenfeldbruck (Kommissarischer Leiter: Oberstarzt Dr. A. Grove) des Zentrums für Luft- und Raumfahrtmedizin der Luftwaffe, Köln (Generalarzt der Luftwaffe: Oberstarzt Prof. Dr. R. Schick) und dem Zentrum für Weltraummedizin² (Leiter: Prof. Dr. H-C. Gunga) der Medizinischen Fakultät der Charité – Universitätsmedizin Berlin
Eckard Glaser¹, ², André Gens¹, Hanns-Christian Gunga², Carla Ledderhos¹
WMM 59. Jahrgang (Ausgabe 12/2015; S. 382-389)
ORIGINALARBEIT
Zusammenfassung
Einleitung: Bei Piloten von Hochleistungskampfflugzeugen kann es durch die während des Fluges auftretenden Beschleunigungskräfte zur Ausbildung von Atelektasen kommen. Diese entstehen durch das Kollabieren der basalen Lungenabschnitte und äußern sich symptomatisch durch Brustschmerzen, Husten und Kurzatmigkeit. Das Auftreten von Atelektasen wird durch Atmung von reinem Sauerstoff und die Nutzung von Anti-G Schutzanzügen weiter gefördert.
Ziel dieser Studie war es, die Veränderungen der Lungenfunktion in Abhängigkeit vom Design des verwendeten Anti--G-Anzuges zu untersuchen und dabei neben der Ventilation auch die Diffusion und die Perfusion zu erfassen.
Methodik: Insgesamt absolvierten 18 Luftfahrzeugführer (LFF) in der Humanzentrifuge (HZF) des Flugmedizinischen Instituts[1] der Luftwaffe in Königsbrück 236 Zentrifugenläufe. Dabei trugen sie zwei verschiedene Anti-G-Schutzanzüge: eine weiterentwickelte Version des Libelle G-Multiplus® Anzuges der Firma Autoflug (Enhancement-Libelle (E-LIB)) und die im Eurofighter zugelassene Anti-G-Schutzausrüstung Air Crew Equipment Assembly (AEA, Hersteller: BAe Systems), allerdings ohne die im Realflug benutzte positive Druckbeatmung (O-AEA). Mit jedem Anzug wurden sieben unterschiedliche G-Belastungsprofile absolviert; bei drei davon wurde nach Beschleunigungsbelastung die Lungenfunktion untersucht. Hierbei wurden umittelbar nach jedem Zentrifugenlauf die Ventilationsparameter (Gesamtvolumen (TLCHe-SB), Vitalkapazität (VC), Residualvolumen (RVHe- SB)) erfasst. Nach Kenntnis der Autoren zum ersten Mal wurden auch das Alveolarvolumen (VA) sowie die Diffusionskapazität mit Hilfe von NO und CO im DLCO-DLNO single-breath Verfahren gemessen. Alle Lungenfunktionsdaten wurden mit den Ausgangsdaten, die vor Beginn der Zentrifugenläufe erhoben wurden, verglichen.
Ergebnisse: Die unterschiedlichen Gz-Profile hatten bei beiden Anti-G-Schutzanzügen Störungen von Ventilation, Perfusion und Diffusion zur Folge. Unabhängig vom Anzugtyp konnten bei den unmittelbar auf die Zentrifugenbelastung folgenden Messungen signifikante Abnahmen von TLC, VC und VA beobachtet werden. Ebenso führte bei beiden Anti--G--Schutzanzügen die Gz-Belastung zu einer signifikanten Abnahme von DLNO-SB und Dm und einer Zunahme von Vc.
Deutliche Unterschiede zwischen den beiden Anzügen fanden sich beim Verhalten des RV/TLC Quotienten. Hier kam es bei Benutzung des O-AEA zu einer statistisch signifikanten Zunahme gegenüber der Ausgangslage.
Schlussfolgerungen: Im Vergleich zu dem autonomen System E-LIB zeigt das bedruckte und mit Bauchblase ausgestattete System O-AEA nach Beschleunigungsbelastung erkennbar ausgeprägtere Störungen der Lungenfunktion.
Schlagworte: Beschleunigung, Atelektase, Lungenfunktion, Ventilation, Perfusion, Diffusionskapazität
Summary
Background: Fighter pilots develop acceleration atelectasis if exposed to +Gz-forces caused by collapse of basal lung tissue. The occurrence of atelectasis is characterized by chest pain, coughing and shortness of breath, and becomes aggravated when breathing 100 % oxygen and wearing anti-G suits (AGS).
The study was designed to investigate AGS design related changes of pulmonary function – including diffusion and perfusion.
Methods: 18 fighter pilots underwent a total of 236 centrifuge runs with seven acceleration profiles wearing two different types of anti-G suites (AGS): an enhanced variant of the Libelle G-Multiplus® AGS (E-LIB, manufacturer: Autoflug)) and the Aircrew Equipment Assembly (AEA, manufacturer: BAe Systems) – as approved for the Eurofighter – however without the use of assisted positive pressure breathing (O-AEA). Three of seven centrifuge runs absolved by each AGS/pilot combination were used to evaluate lung function after Gz loads. Before and immediately after these runs, parameters of ventilation (total lung capacity -(TLCHe-SB), vital capacity (VC), residual volume (RVHe-SB)) were recorded. Likewise and, as far as the authors know for the first time, alveolar volume (VA) and lung diffusing capacity for NO and CO were measured using the DLCO-DLNO single-breath technique. All lung function data were compared to the basic data registered before to the centrifuge runs.
Results: The different Gz-profiles resulted in disturbances of ventilation, perfusion and diffusing capacity of the lung for both AGS. Independent of the AGS used, significant decreases of TLC, VC, RV and VA were recorded immediately after centrifuge rides. DLNO-SB and Dm significantly decreased, whereas Vc increased for both systems following Gz-acceleration.
The increase of the RV / TLC ratio was statistically significantly higher if using the O-AEA.
Conclusions: Compared to the autonomous system E-LIB, the pressurized O-AEA with an abdominal bladder increased the degree of disturbances of lung function parameters accompanying acceleration forces noticeably.
Keywords: acceleration, atelectasis, lung function, ventilation, perfusion, diffusing capacity
Einführung
Das Einsatzspektrum des EUROFIGHTER als strahlgetriebenes Hochleistungskampfflugzeug der vierten Generation stellt hohe Anforderungen an die Piloten. Dabei sind in physiologischer Hinsicht besonders die Belastungen aufgrund der Einwirkung hoher Beschleunigungskräfte extrem und ohne ein leistungsfähiges Anti-G-Schutzsystem nicht zu bewältigen. Diese Systeme sollen der durch die positive Gz-Belastung[2] bedingten Verschiebung von Blutvolumen in die abhängigen, tieferliegenden Körperregionen entgegenwirken und den intrathorakalen Druck erhöhen, um so auch unter der Beschleunigungsbelastung eine hinreichende (suffiziente) Perfusion des Gehirns zu ermöglichen. Um dies zu erreichen, wird in der Bein- und Bauchregion mit zunehmender Gz-Belastung von außen ein wachsender Gegendruck auf den Körper aufgebracht. Verwirklicht wird dies üblicherweise durch den Einsatz von pneumatischen Systemen. Allerdings gibt es auch Systeme, die den Gegendruck beschleunigungsabhängig über hydrostatische Säulen erzeugen.
Im Hinblick auf die Gesundheit der Piloten gibt es Indizien, dass eine positive Druckbeatmung, wie sie heute von nahezu allen modernen Anti-G-Schutzsystemen genutzt wird, möglicherweise negative Langzeitfolgen insbesondere auf die Lungenfunktion der Piloten haben könnte. Systematische Studien, die detailliert Einflüsse unterschiedlicher Anti-G-Schutzanzüge sowie der positiven Druckbeatmung auf die Lungenfunktion untersuchen oder die auf Messdaten beruhende Vergleiche zwischen unterschiedlichen Anti-G-Schutzkonzepten ziehen, sind bisher kaum öffentlich zugänglich. Bekannt ist, dass hohe kopfwärts gerichtete Beschleunigungen (+Gz) in der Körperlängsachse durch den damit verbundenen fußwärts gerichteten Trägheitsvektor im Bereich der Lunge das ohnehin schon bestehende Missverhältnis von Ventilation und Perfusion weiter verstärken; in den apikalen Lungenbezirken kommt es bei Abnahme der Durchblutung zu einer Erhöhung der Ventilation, in den basisnahen Bereichen bei eingeschränkter Belüftung zu einer Zunahme der Perfusion. Dieser Effekt wird verstärkt durch die Wirkung von Anti-G-Anzügen, die durch Abdominalkompression mittels einer Bauchblase das Zwerchfell anheben und damit einhergehend das Residualvolumen vermindern. Hierdurch kann es bei Piloten von strahlgetriebenen Hochleistungskampfflugzeugen zum Kollaps der Alveolen an der Lungenbasis und zur Ausbildung sogenannter Gz-induzierter Atelektasen kommen, die gewöhnlich von intensiven Schmerzen im Brustraum, Hustenanfällen und Atemnot begleitet sind. All diese Faktoren können den Netto-Transport von Gas (O2, CO2) in das und aus dem Kreislaufsystem limitieren und zu einer, für den Piloten leistungsbegrenzenden, stagnierenden Hypoxie führen. Diese bisher nur unzureichend verstandenen Gz-induzierten Änderungen der Ventilation und des Gastransportes von der Lunge in die Kapillaren können mit der klassischen Spirometrie sowie unterschiedlichen Verfahren der Diffusionsmessung erfasst und quantifiziert werden. Während Studien zu Veränderungen der Ventilation bei unterschiedlichen Gz-Belastungen sehr deutliche Veränderungen der statischen Lungenparameter insbesondere bei der Vitalkapazität zutage gefördert haben [4, 5, 11, 12], sind Arbeiten, die eventuelle Veränderungen der Diffusionsleistung der Lunge charakterisieren, bisher nicht bekannt.
Für die Betrachtung der Wirkung von Beschleunigungen auf Piloten ist insbesondere die Körperlängs- oder z-Achse von Bedeutung. In Bezug auf die Lunge sind hier ihre größte morphologische Ausdehnung und damit der größte Effekt auf ihre Funktion zu erwarten. Zudem ist in z-Richtung bei typischen Flugmanövern (enge Kreise oder „Hochziehen“) mit der größten und am längsten anhaltenden Belastung auf den Piloten überhaupt zu rechnen. Durch die erhöhte, unidirektionale (Beschleunigungs-)Kraft kommt es zu Formveränderungen des Herzens mit Beeinflussung der kardialen Auswurfleistung sowie der Herzfrequenz und damit indirekt der Lungen- und Hirndurchblutung. Außerdem nimmt der hydrostatische Druck in Richtung der wirkenden Kraft zu; es kommt zur Ausbildung eines Druckgradienten entlang der z-Achse.
Im Rahmen dieser Arbeit wurden die Auswirkungen von Beschleunigungsbelastungen in der Körperlängsachse (sog. Gz--Beschleunigungen) auf die Lungenfunktion bei Benutzung zweier verschiedener von ihrem Wirkprinzip sehr unterschiedlicher Anti-G--Schutz-systeme untersucht. Erstmals erfolgten neben der Erfassung der statischen Lungenfunktionsparameter auch Messungen zur Bestimmung der Diffusionskapazität und des Membrantransferfaktors. Eines der beiden Systeme (Air Crew Equipment Assembly (AEA) der Firma BAe Systems) setzte auf eine Gz-abhängige, aktive Bedruckung von im Anzug befindlichen Kammern (pneumatisches Prinzip) sowie auf eine positive Druckbeatmung der Piloten. Bei dem in der vorliegenden Studie benutzten System wurde allerdings auf die im realen Flug eingesetzte positive Druckbeatmung verzichtet. Im Unterschied zum im Flugbetrieb eingesetzten AEA wird es im weiteren Verlauf dieser Arbeit deshalb O-AEA genannt (Abbildung 1).
Das andere, vom Luftfahrzeug unabhängige, autonome und passive System, nutzte den Gz-abhängig ansteigenden, hydrostatischen Druck von sogenannten „Fluid-Muskeln“, die in den Anzug eingearbeitet waren und deren Druckverlauf der Flüssigkeitssäule sich Gz-ab-hängig veränderte, um den G-Schutz zu verwirklichen. Es handelte sich dabei um eine weiterentwickelte Form des Libelle G-Multiplus® Anzuges der Firma Autoflug (im weiteren E-LIB genannt) (Abbildung 2).
Methoden
Probanden
An der Untersuchung nahmen 18 LFF im Alter von 36,1 ± 4,9 Jahren (Masse 86,4 ± 11.6 kg, Größe 179,7 ± 5,7 cm) teil. Nach mündlicher wie schriftlicher Aufklärung und schriftlich eingeholtem Einverständnis absolvierten sie nach einem festgelegten Testplan insgesamt 236 Zentrifugenläufe mit zwei verschiedenen Anti-G-Schutzanzügen.
Belastungsprofile
Mit jedem Anzugsystem wurden jeweils sieben Profile auf der HZF gefahren. Für die spätere Auswertung erfolgte dabei die Aufzeichnung der Gz-Belastung sowie weiterer physiologischer Parameter (EKG, Herzrate und Pulswelle).
Zwei Profile dienten der Familiarisierung der LFF mit dem entsprechenden zu testenden Anzug. Drei der restlichen Profile wurden dazu benutzt, unmittelbar im Anschluss an die Zentrifugenbelastung Parameter der Lungenfunktion mit ihren Teilprozessen Belüftung und Diffusion zu erheben. Diese wurden mit den Ausgangsdaten, die am ersten Tag dieser Vergleichserprobung vor Beginn der Zentrifugenläufe gewonnen wurden, verglichen.
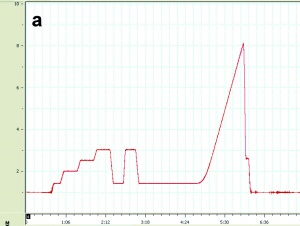
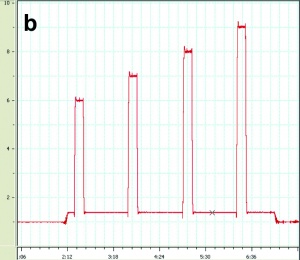
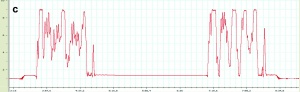
Beim ersten Wertungsprofil handelte es sich um einen Eingewöhnungslauf mit anschließendem Linearprofil (Abbildung 3a). Es war das einzige passiv gefahrene Profil[3]. Das Linearprofil diente dabei der Bestimmung der sogenannten „relaxed G-Toleranz“, also dem Gz-Wert, der in entspanntem Zustand mit Schutzanzug, aber ohne vom Piloten ausgeführtes Anti-G-Manöver erreicht wird. Als Endpunkt des Profils wurde der Verlust des peripheren Sehens gewertet. Dieser wurde verifiziert, indem der Pilot Lichtsignale, die ihm in der Zentrifugengondel im Bereich des peripheren Gesichtsfeldes eingespielt wurde, mit einem Knopfdruck beantworten musste. Blieb diese Antwortreaktion aus, wurde die Zentrifugenfahrt beendet. Die beiden anderen Profile (Stufenprofil und Flugprofil) wurden aktiv beziehungsweise interaktiv mit einer Onset Rate[4] von 6 Gz/s absolviert. Beim Stufenprofil steuerte der Proband die HZF zunächst auf ein G-Plateau von 6 Gz, auf dem er für 10 s verweilte. Danach wurde wieder auf „Baseline“ (1,4 Gz) gefahren. Nach einer einminütigen Pause erfolgte dann die nächste Gz-Belastung, die jeweils um 1 Gz höher lag, so dass bei diesem Profil stufenweise die Belastungen von 6 Gz bis 9 Gz gesteigert wurden (Abbildung 3b). Beim Flugprofil (Abbildung 3c) war es die Aufgabe des Probanden, nach einer sogenannten G-Awareness-Exercise die HZF aktiv zu steuern und einem Zielflugzeug (MIG 29) zu folgen, dessen Profil eingespielt wurde (sogenanntes interaktives Profil). Auf diese Weise wurden alle Probanden einer weitgehend gleichen Belastung unterzogen. Ein Verfolgungsflug dauerte etwa 60 s und wurde während eines Testlaufs zweimal absolviert. Die Pause zwischen beiden Verfolgungsläufen betrug zwei Min. In dieser Zeit befand sich die HZF auf Baseline (1.4 Gz).
Lungenfunktionsdiagnostik
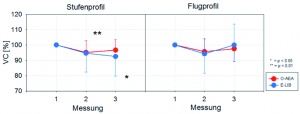
Ziel der Lungenfunktionsmessung im Rahmen dieser Studie war die Bestimmung von Ventilationsgrößen wie Totale Lungenkapazität (TLCHe-SB), Vitalkapazität (VC), Residualvolumen (RVHe-SB) und Alveoläres Volumen VA sowie des Quotienten RV/TLC vor und unmittelbar nach den unterschiedlichen Zentrifugenläufen mittels kombinierter single-breath Methode. Damit sollten Änderungen der Belüftung der Lunge als Folge von Zentrifugenbelastungen und bei unterschiedlichem Design von Anti-G-Schutzausrüstungen erfasst werden.
Daneben wurden Parameter des Gasaustausches zwischen Alveolen und Lungenkapillaren vor und nach Zentrifugenbelastung ermittelt. Aus der als kombinierte single-breath-Methode bestimmten Diffusionskapazität für CO (DLCO-SB) und der Diffusionskapazität für NO (DLNO-SB) konnten die Einzelkomponenten der Diffusion, der Membrananteil (Dm) und der Blutanteil (kapilläre Lungendurchblutung, Vc) abgeleitet werden.
Bei den in den Abbildungen 6 bis 14 aufgeführten Messungen gibt die Messung eins jeweils den in der Ausgangslage, das heißt vor Absolvieren der Belastungsprofile erhobenen Bezugswert wieder, während die Messungen zwei und drei die Ergebnisse der beiden unmittelbar aufeinanderfolgenden Messungen nach der Zentrifugenbelastung repräsentieren.
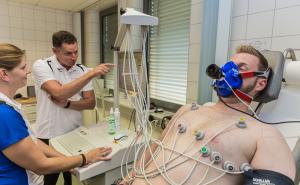
Gerätetechnisch kam ein handelsüblicher, zugelassener Mess-platz (Jaeger MasterScreen PFT Pro® (Cardinal Health Germany 234 GmbH, Höchberg) zum Einsatz. Da dieses Gerät aufgrund seiner Auslegung für den klinischen Alltag ohne Veränderungen nicht für diese Studie geeignet war, mussten wesentliche Anpassungen hinsichtlich der Mobilität des Gerätes, der Flexibilität des Messkopfes sowie der Robustheit des Aufbaues vorgenommen werden, um den Umgebungs- und Einsatzbedingungen im Arbeitsbereich der HZF gerecht zu werden. Dabei durften zulassungsrelevante Größen und insbesondere die Qualität der Messung betreffende Parameter nicht verändert werden. Da bisher kein kommerzielles Gerät bekannt und verfügbar war, das unverändert für die Klärung der Fragestellung in der Humanzentrifuge geeignet gewesen wäre, wurde es so angepasst, dass der Messkopf mit den Sensoren abnehmbar war und in die HZF hineingehoben werden konnte. Die Testgasflaschen wurden auf einem fahrbaren Wagen hinter der Datenerfassungseinheit des Messgerätes montiert. Das Mundstück wurde durch eine Atemmaske ersetzt, mit deren Umgang Piloten aus dem täglichen Flugbetrieb vertraut sind und die das Atemmuster weniger beeinflusst als das üblicherweise bei diesem Gerät benutzte Mundstück. (Abbildungen 5 und 6)
Statistische Datenauswertung und Datendarstellung
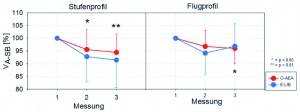
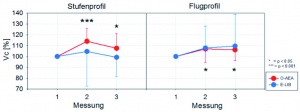
Die statistische Datenanalyse wurde mit dem Statistikpaket SPSS™ (Version 16.0) durchgeführt. Zur Analyse der Daten wurde ein t-Test oder, bei fehlender Normalverteilung, ein parameterfreies Äquivalent benutzt. Das Signifikanzniveau wurde auf p < 0,05 festgelegt. Alle Daten in dieser Arbeit sind jeweils als Mittelwert mit der zugehörigen Standardabweichung angegeben. Statistisch gesicherte Differenzen im Vergleich zur Ausgangslage sind in den Abbildungen mit * (* = p < 0.05; ** = p < 0.01; *** = p < 0.001) gekennzeichnet, bei Unterschieden zwischen beiden Systemen wurde ein # verwendet. Dargestellt sind die Änderungen der jeweiligen Größen [in %] im Vergleich zur Ausgangslage, die am ersten Tag vor Beginn der Vergleichserprobung durch Doppelbestimmung erhoben wurde.
Ergebnisse
Unabhängig von der Art des gefahrenen Profils und des benutzten Anti-G-Schutzanzuges führten alle Beschleunigungsbelastungen zu deutlichen Änderungen sowohl bei der Lungenbelüftung als auch beim Diffusionsverhalten der Lunge, die häufig in einem statistisch zu sichernden Bereich lagen. Beim Vergleich beider Anzüge fiel vor allem das unterschiedliche Verhalten des Residualvolumens und des auf die Totalkapazität normierten Residualvolumens auf.
Veränderungen der Ventilation nach Zentrifugenbelastung
Bei beiden betrachteten Anti-G-Anzügen wurden unmittelbar nach den Zentrifugenprofilen signifikante Abnahmen der totalen Lungenkapazität (TLC), Vitalkapazität (VC), des Residualvolumens (RV) und der alveolären Ventilation (VA) (Abbildungen 6, 7, 8, 9) beobachtet, die größtenteils auch statistisch zu sichern waren.
Veränderungen der Diffusion und Perfusion nach Zentrifugenbelastung
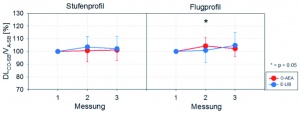
Abbildung 10 gibt das Verhalten des sogenannten Krogh-Faktors, KCO-SB = DLCO-SB/VA-SB nach den Beschleunigungsbelastungen wieder. Sein Anstieg beim Flugprofil deutet auf Veränderungen hin, die als funktioneller Verlust von Lungengewebe interpretiert werden müssen. Dabei gab es keine Unterschiede zwischen beiden Anzügen.
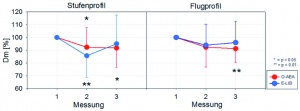
Ebenso führten bei beiden Anti-G-Schutzanzügen die Gz-Belastungen zu einer in den meisten Fällen statistisch zu sichernden Abnahme der NO Diffusion und des Membranfaktors (Dm) (Abbildung 11). Die auf die alveoläre Ventilation normierte NO-Diffusion, DLNO-SB/VA-SB (Abbildung 12) nahm dabei ebenfalls tendenziell ab.
Die kapilläre Lungendurchblutung zeigte bei beiden Anzügen einen zum Teil sehr klaren Anstieg (Abbildung 13), ohne dass dabei ein systematischer Unterschied zwischen den beiden betrachteten Systemen nachweisbar war. Dieser Anstieg lässt sich mit der deutlichen Zunahme des hydrostatischen Druckes insbesondere in den basalen Lungenabschnitten unter der unmittelbar vorangegangene Gz-Belastung erklären, der über die Zeit der Gz-Belastung hinaus noch persistiert.
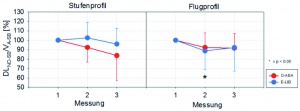
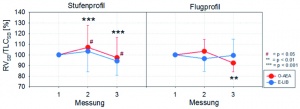
Die Beschleunigungsbelastungen führten bei beiden Anzügen zu einem Anstieg des prozentualen Anteils des Residualvolumens an der totalen Lungenkapazität (RVSB/TLCSB) (Abbildung 14). Statistisch signifikant war dieser allerdings nur bei Benutzung des O-AEA.
Der Unterschied der Reaktion beider Systeme ließ sich beim Stufenprofil auch statistisch sichern.
Diskussion
Ziel der Untersuchungen war es, die bei Piloten von Hochleistungskampfflugzeugen durch hohe Beschleunigungen ausgelösten Veränderungen der Lungenfunktion in Abhängigkeit vom Design des verwendeten Anti-G-Anzuges zu untersuchen. Dabei ist das Hauptaugenmerk nicht nur auf den Teilprozess der Ventilation sondern, nach Wissen der Autoren erstmals, auch auf die sich anschließenden Prozesse der Diffusion und Perfusion gelegt worden.
Wenn auch Belüftungsstörungen der Lunge bei Gz-Belastungen verschiedenster Art bereits von anderen Autoren beschrieben wurden [4, 5, 11, 12], stand ein Vergleich der Auswirkungen verschiedener Anti-G-Schutzanzüge mit unterschiedlichen Wirkkonzepten auf die Ventilation bisher immer noch aus. Zu den Veränderungen des alveolo-kapillären Gasaustausches bei Beschleunigungsbelastungen gab es bislang noch gar keine Untersuchungen.
Der Gasaustausch zwischen Alveolen und Kapillaren – neben der Ventilation eine zentrale Aufgabe der Lunge – wird in der klinischen Diagnostik seit vielen Jahren mittels der sogenannten Diffusionskapazität quantifiziert [7, 8, 13]. Die zentrale Schwierigkeit bei der Bestimmung des Diffusionsvermögens von Sauerstoff ist dabei allerdings der nicht-verschwindende endliche Sauerstoffpartialdruck in den Lungenkapillaren, der einer direkten Messung, die noch dazu einfach zu handhaben und nicht-invasiv ist, nicht zugänglich ist. Man hilft sich, indem man das Diffusionsvermögen von anderen Gasen bestimmt, die dieses Problem nicht haben, und bei denen man aus dem Diffusionsvermögen des verwendeten Gases auf das Diffusionsvermögen von Sauerstoff schließen kann. Dabei kann man anhand des Verteilungsgrades von CO und NO auf die Diffusionskapazität der Lunge für CO, NO und indirekt auch auf die für Sauerstoff schließen [1, 14, 15, 16].
Nach unterschiedlichen Ansätzen der Vergangenheit hat sich heute die single-breath-Technik nach dem von Ogilvie et al. modifizierten Verfahren von Marie und August Krogh in der Klinik nach und nach durchgesetzt und ist von der breiten Fachwelt inzwischen akzeptiert [7, 8]. Seit den Arbeiten von Roughton und Forster, die die Diffusion in zwei wesentliche Schritte, nämlich den an der alveolo-kapillären Membran (sogenannter Membranfaktor) und den sich innerhalb des Blutes abspielenden Prozessen (Blutfaktor) unterteilten, hat sich durch die vorgenommenen Verbesserungen der Technik ein klinisch taugliches Verfahren zur Erfassung der Diffusionsleistung der Lunge etablieren können. Dieses von der gemeinsamen Taskforce der European Respiratory Society (ERS) und der American Thoracic Society (ATS) erarbeitete und empfohlene Verfahren [8] der kombinierten DLCO-DLNO Messung im single-breath-Verfahren ist in der vorliegenden Studie – vor und nach Zentrifugenfahrten, jeweils als Doppelbestimmung durchgeführt – angewendet worden.
Beim eigentlichen Test haben die Probanden nach maximaler Inspiration eines Helium-CO-NO-Gemisches für fünf Sekunden ihren Atem angehalten. Anschließend wurde die Verteilung der Indikatorgase in ihrer Ausatemluft analysiert. Dabei diente das CO zur Bestimmung der Diffusionkapazität (DLCO) der Lunge. Der Einsatz von NO als Indikatorgas ermöglichte die Unterscheidung, ob die Alveolen unzureichend durchblutet waren, oder aber ob eine Störung der Diffusion durch die Membran vorgelegen hatte. Darüber hinaus bot NO die Vorteile vereinfachter Messmanöver sowie verkürzter Messzeit und ermöglichte die Bestimmung des Blutvolumens in den Lungenkapillaren (Vc) und des Membranfaktors (Dm) innerhalb eines Messvorganges. Die zusätzliche Verwendung von Helium ermöglichte die Bestimmung des Residualvolumens und die Aufdeckung möglicher Verteilungsstörungen.
Die bereits in der Methodik beschriebene Anpassung des Gerätes an die Verhältnisse in der Humanzentrifuge hat sich bei der Versuchsdurchführung ohne Einschränkungen bewährt. Vor allem ermöglichte dies eine Erfassung der Lungenfunktion der Probanden direkt im Anschluss an die Zentrifugenfahrt, ohne dass sie die Zentrifuge verlassen und sich bewegen mussten. Die eingesetzte Methode war daher grundsätzlich dafür geeignet, bislang nicht erfassbare Auswirkungen hoher Gz-Belastungen auf die Lunge zu untersuchen.
Sowohl unmittelbar nach dem Stufenprofil als auch nach dem Flugprofil kam es im Vergleich zur Ausgangslage zu deutlichen Störungen der Ventilation mit signifikanten Abnahmen aller Ventilationsgrößen (TLC, VC, RV, VA). Da dieses Phänomen bei beiden Anti-G-Anzügen gleichermaßen aufgetreten ist, muss es als Folge der Beschleunigungsbelastung gewertet Im Hinblick auf Änderungen der Vitalkapazität sind ähnliche Befunde bereits von anderen Autoren erhoben worden [11], die Veränderungen der Totalen Lungenkapazität, des Residualvolumens und der alveolären Ventilation nach G-Beschleunigungen sind nach Kenntnis der Autoren dagegen erstmalig beschrieben worden.
Die Diffusionskapazität für CO – normiert auf das Alveolarvolumen – (DLCO-SB/VA-SB, sogenannter Krogh-Faktor, KCO-SB, Abbildung 10) blieb nach den unterschiedlichen G-Belastungen nahezu unverändert oder stieg leicht an. Im Zusammenhang mit der deutlich reduzierten alveolären Ventilation (Abbildung 9) ist dies ein klares Indiz für einen merklichen Verlust an funktionellem Lungenparenchym („loss of lung units“) in Form von Atelektasebildung durch die vorangegangene Gz-Belastung. Hierbei kommt es zum Kollabieren von Lungenabschnitten durch Aneinanderlegen der Alveolarwände. Je nach Größe der Atelektasen ist die für den Gasaustausch zur Verfügung stehende Oberfläche verringert und damit auch die Sauerstoffaufnahme reduziert. Beim Flugprofil war dieser Verlust bei O-AEA gegenüber der Ausganglage auch statistisch zu sichern. Beide betrachteten Systeme, O-AEA und E-LIB, zeigten dabei ein ähnliches Verhalten.
Die in der vorliegenden Untersuchung bei beiden Anzügen beobachteten deutlichen Abnahmen der NO-Diffusion und des Membranfaktors (Dm) (Abbildung 12) sowie die zumindest in der Tendenz vorhandene Reduktion der auf die alveoläre Ventilation normierten NO-Diffusion, DLNO-SB/VA-SB (Abbildung 11) müssen als deutlicher Hinweis auf einen erhöhten Diffusionswiderstand über der alveolo-kapillären Membran mit nachfolgenden Einschränkungen des Gasaustausches auf dieser Ebene durch die +Gz-Belastungen gewertet werden.
Hinweise auf Unterschiede zwischen beiden Systemen fanden sich vor allem hinsichtlich des prozentualen Anteils des Residualvolumens an der totalen Lungenkapazität (RVSB/TLCSB), wie Abbildung 14 zeigt. Hier scheint der im Vergleich zu E-LIB höhere RVSB/TLCSB-Quotient beim O-AEA insbesondere nach dem Stufenprofil auf eine Behinderung der Atmung durch die Bauchblase der Anti-G-Hose hinzudeuten, welche die Dehnbarkeit der Lunge beziehungsweise einzelner Abschnitte einschränkt und die Luftverteilung stört.
Folgerungen
Um einen verlässlichen Anti-G-Schutz auch bei den modernen Kampfflugzeugen zu realisieren, verwenden neuere Anti-G-Anzüge, und so auch das im Eurofighter eingesetzte AEA, eine Überdruckbeatmung, deren G-toleranzsteigernde Wirkung unumstritten ist, deren Auswirkungen auf die Lungenfunktion der Piloten in der Fachwelt aber kontrovers diskutiert werden. Bedenkt man, das in der vorliegenden Studie der pneumatische Anzug, anders als im realen Flugbetrieb, ohne die sonst übliche Überdruckbeatmung verwendet wurde, so ist dringend zu empfehlen, die Veränderungen der Lungenfunktion auch bei Benutzung der positiven Druckbeatmung zu untersuchen. Außerdem sollte der Lungenfunktion von Eurofighter-Piloten zukünftig auch bei der jährlichen Untersuchung auf Wehrfliegerverwendungsfähigkeit (WFV) eine vermehrte Aufmerksamkeit geschenkt werden. Sinnvoll wäre es, die Veränderungen der Lungenfunktion im Verlauf der Berufskarriere eines LFF mittels Bodyplethysmographie mit Erhebung der CO-NO-Diffusionswerte sorgfältig zu erfassen und zu dokumentieren, um so mögliche Veränderungen frühzeitig erkennen und, wenn nötig, geeignete präventive Maßnahmen ergreifen zu können.
Kernaussagen
In der vorliegenden Studie wurden die Auswirkungen von Gz-Beschleunigungen auf die Lungenfunktion von Kampf-piloten bei Nutzung zweier unterschiedlicher Anti-G-Anzüge untersucht.
Dazu musste ein klinisch übliches Messverfahren an die Versuchsbedingungen in der Humanzentrifuge angepasst werden.
Bei beiden Anzügen kam es zu einer G-induzierten Beeinflussung von Ventilation, Diffusion und Perfusion.
Daneben gab es deutliche Belege für eine Behinderung der Atmung durch die Bauchblase des pneumatischen Systems.
Mögliche zusätzliche Auswirkungen auf die Lungenfunktion durch die bei neueren Anti-G Schutzsystemen genutzte Überdruckbeatmung müssen noch untersucht werden.
Literatur
- Criée C-P. Lungenfunktion – Empfehlungen der Deutschen Atemwegsliga Dustri-Verlag Dr. Karl Feistle, 2006.
- DeHart, R. L.: Fundamentals of Aerospace Medicine/edited by Williams & Wilkins, 2nd ed. Baltimore, 1996.
- Ernsting, J., Nicholson, A. N. and D. J. Rainford: Aviation Medicine. Butterworth-Heinemann, 3rd ed., Oxford, 1999.
- Green ND: Lung volumes during +Gz acceleration and the effects of positive pressure breathing and chest counter pressure. J Gravit Physiol 1994; 1(1): 41-44.
- Haswell MS, Tacker W A, Balldin UI et al.: Influence of Inspired Oxygen Concentration on Acceleration Atelectasis. Aviat Space Environm Med 1986; 57: 432-437.
- Hinkelbein, J. und E. Glaser (Hrsg).: Lehrbuch der Flugmedizin. 1. Aufl., Uni-Med Science Bremen, 2007.
- Hughes, J.M.B. and D.V. Bates: Historical review: the carbon monoxide diffusing capacity (DLCO) and its membrane (DM) and red cell (θ*Vc) components. Respiratory Physiology & Neurobiology 138, 115-142, 2003.
- MacIntyre, N, R.O. Crapo, G. Viegi, D.C. Johnson, C.P.M. van der Grinten, V. Brusasco, F. Burgos, R. Casaburi, A. Coates, P. Enright, P. Gustafsson, J. Hankinson, R. Jensen, R. McKay, M.R. Miller, D. Navajas, O.F. Pedersen, R. Pellegrino and J. Wanger: Standardisation of the single-breath determination of carbon monoxide uptake in the lung. SERIES “ATS/ERS TASK FORCE: STANDARDISATION OF LUNG FUNCTION TESTING” Edited by V. Brusasco, R. Crapo and G. Viegi Number 4 in this Series, Eur Respir J 26: 720- 735, 2005.
- Pappenheimer J. R.: Standardization of definitions and symbols in respiratory physiology. Fed Proc 1950; 9: 602-605.
- Pongratz, H.: Kompendium der Flugmedizin. 6. Aufl. Fürstenfeldbruck, 2002.
- Tacker, WA, Balldin UI, Burton RR et al.: Induction and prevention of acceleration atelectasis. Aviat. Space Environm. Med. 1987; 58: 69-75.
- Tikhonov MA, Kondakov AV: Effect of gravitational atelectasis of the lungs on expiratory airway closure. Bull Eksp Biol Med 1981; 92(12): 663-666.
- West, J. B.: Respiratory Physiology. The essentials. Lippincott Williams Wilkins. 7.ed., 2004.
- West J. B.: Understanding pulmonary gas exchange: ventilation-perfusion relationships J Appl Physiol 2004; 97: 1603-1604.
- Zavorsky, G. S., K. Badra Quiron, P. S. Massarelli and L. C. Lands: The relationsship between single breath diffusion capacity of the lung for nitric oxide and carbon monoxide during various exercise intensities. Chest 2004; 125(3): 1019-1027.
- Zavorsky, G. S. and J. M. Murias: A small amount of inhaled nitric oxide does not increase lung diffusing capacity. ERJ Express. Published on March 15, 2006.
Interessenkonflikt: Die Verfasser erklären, dass gemäß den Regeln des International Committee of Medical Journals kein Interessenkonflikt besteht.
Ethik-Votum: Für das Monitoring ausgewählter physiologischer Parameter der Herz,- Kreislauf- und Lungenfunktion bei Belastung von Luftfahrzeugführernin der Humanzentrifuge im Zusammenhang mit Zentrifugenfahrten liget ein postives Votum der Ethikkommission der Sächsischen Landesärztkammer vor (EK-BR-29/08-1 vom 23.07.2008)
Bildquellen: Alle Fotos: Zentrum für Luft- und Raumfahrtmedizin der Luftwaffe
Originalarbeit
Manuskriptdaten:
Eingereicht: 24.09.2015
Revidierte Fassung angenommen: 09.11.2015
Zitierweise:
Glaser E, Gens A, Gunga HC, Ledderhos C: Auswirkungen des Designs von Anti-G-Anzügen auf die Lungenfunktion bei Piloten von Hochleistungsflugzeugen. Wehrmedizinische Monatsschrift 2015; 59(12): 382-389.
[1]
Heute umgegliedert in Zentrum für Luft- und Raumfahrtmedizin der Luftwaffe
[2]
In der Flugmedizin wird zur einfacheren Beschreibung der auf den Körper einwirkenden Beschleunigungskräfte ein Koordinatensystem verwendet, bei dem die z-Richtung in Richtung der Körperlängsachse zeigt. Einen Überblick hierüber und eine Einführung in die Auswirkungen von Beschleunigungen auf den menschlichen Körper findet man unter anderem in [2, 3, 4, 8].
[3]
Bei einem passiven Profil wird der Zentrifugenlauf von außen gesteuert, während der Proband bei einem aktiven Profil durch entsprechende Bewegungen des Steuerknüppels in der Zentrifugengondel die Beschleunigungsabläufe selbst bestimmt.
[4] Onset-Rate: Zunahme der Beschleunigung pro Zeiteinheit
Datum: 23.12.2015
Quelle:
Wehrmedizinische Monatsschrift 2015/12
Wehrmedizinische Monatsschrift 2015/12