METHODEN ZUM NACHWEIS DER VERGIFTUNG MIT CHEMISCHEN KAMPFSTOFFEN: ZUSAMMENARBEIT MIT DER ORGANISATION FÜR DAS VERBOT CHEMISCHER WAFFEN (OVCW)
Methods for Verification of Poisoning by Chemical Warfare Agents: Collaboration with the Organisation for the Prohibition of Chemical Weapons (OPCW)
Aus dem Institut für Pharmakologie und Toxikologie der Bundeswehr, München (Leiter: Oberstarzt Prof. Dr. H. Thiermann)
Marianne Koller, Horst Thiermann, Harald John
WMM, 58. Jahrgang (Ausgabe 9/2014; S. 310-315)
Zusammenfassung:
Hintergrund: Chemische Kampfstoffe (CKS) wurden erstmals vor gut 100 Jahren im Verlaufe des Ersten Weltkrieges eingesetzt und in den folgenden Jahrzehnten weiterentwickelt. Im Jahr 1997 trat das Chemiewaffenübereinkommen in Kraft, welches unter anderem Herstellung und Einsatz der CKS verbietet und die Vernichtung der Restbestände vorsieht.
Die Organisation für das Verbot Chemischer Waffen (OVCW, Friedensnobelpreisträger von 2013) überwacht die Umsetzung dieses Abkommens. Dazu werden auch hoch moderne und zuverlässige instrumentell analytische Methoden benötigt, die in ausgewiesenen Speziallaboratorien nationaler Institutionen weltweit entwickelt und erprobt werden. Über regelmäßige Ringversuche (Biomedical Exercises) eruiert die OVCW geeignete Partner, die auch in biomedizinischen Proben (Blut, Urin, Gewebe) die Kampfstoffexposition nachweisen können (Verifikation). Das Institut für Pharmakologie und Toxikologie der Bundeswehr (Inst- PharmToxBw) ist für die Bundesrepublik Deutschland regelmäßiger erfolgreicher Teilnehmer an diesen Übungen.
Dieser Artikel berichtet über die aktuelle Problematik chemischer Kampfstoffe, stellt die Zusammenarbeit von OVCW und InstPharmToxBw vor, skizziert die Besonderheiten und Herausforderungen der Kampfstoffanalytik in biologischen Proben und gibt einen Einblick in die Anforderungen und Resultate der bisherigen Übungen.
Schlussfolgerungen: Die Fähigkeiten zur Verifikationsanalytik dienen besonders den Soldaten und Soldatinnen der Bundeswehr im Einsatz, um justiziabel eine mögliche Vergiftung mit CKS nachweisen zu können. Die Kompetenz auf diesem Sektor und die Qualität der Analytik wird durch die Akkreditierungen nach DIN/EN/ISO 17025 und 15189 durch die Deutsche Akkreditierungsstelle (DAkkS) dokumentiert und in den Übungen der OVCW auf internationalem Expertenniveau unter Beweis gestellt.
Schlagworte: Akkreditierung, Chemische Kampfstoffe, Biomedical Exercises, biomedizinische Verifikation, OVCW
Summary
Background: Chemical warfare agents (CWA) were used for the first time about 100 years ago during World War I and further developed in the following decades. In 1997 the Chemical Weapons Convention has entered into force, amongst others prohibiting production and use of CWA and destroying remaining stockpiled material. The Organisation for the Prohibition of Chemical Weapons (OPCW, Nobel Peace Prize Laureate 2013) controls and supervises the implementation of this convention. Therefore, ultra-modern and reliable instrumental analytical procedures are required, world- wide elaborated and established in designated specialized laboratories being part of national authorities. By continuous round robin tests (biomedical exercises) the OPCW elicits convenient and eligible partners who are qualified for analyzing biomedical samples (blood, urine, tissue) to detect CWA (verification analysis). The Bundeswehr Institute of Pharmacology and Toxicology (InstPharmToxBw) is a successful participant in these exercises and the national representative of the Federal Republic of Germany.
This article reports on the actual problems concerning CWA, presents the collaboration between OPCW and InstPharm- ToxBw, outlines the characteristics and challenges of CWA analysis in biological specimen, and provides an insight into the requirements and results of previous exercises.
Conclusions: Qualification for performing reliable verification analysis is of important use especially for Bundeswehr soldiers on deployment abroad as it allows justiciable confirmation of alleged CWA poisoning. Competence in this field and quality of performance are documented by the accreditation by the German Accreditation Body according to the international standards DIN/EN/ISO 17025 and 15189 and proved on international expert level by the OPCW exercises.
Keywords: accreditation, chemical warfare agents, biomedical exercises, biomedical verification, OPCW
Einführung
Die diesjährigen Gedenkfeiern zum Ausbruch des Ersten Weltkriegs vor 100 Jahren rücken auch die Geburtsstunde der chemischen Kriegführung neuerlich in das öffentliche Interesse. Nach der Verwendung einiger Reizstoffe wurden beispielsweise 1915 mit Chlor und Phosgen und 1917 mit Schwefellost (früher als Senfgas bezeichnet) erstmals reine synthetische Chemikalien zu kriegerischen Zwecken eingesetzt, um den Gegner zu vergiften und damit kampfunfähig zu machen oder zu töten (chemische Kampfstoffe, CKS). Trotz des Einsatzverbotes durch die Haager Deklaration von 1899 und das Genfer Protokoll von 1925 wurden auch in den folgenden Jahrzehnten beispielsweise mit dem Hautkampfstoff (HKS) Lewisit und den Nervenkampfstoffen (NKS) Tabun, Sarin, Soman und VX neue CKS waffenfähig entwickelt.
Bis heute stellen die Restbestände, insbesondere der HKS und NKS, eine ernstzunehmende Bedrohung für Militär und Zivilbevölkerung dar. Da ferner die Herstellung der toxischen Chemikalien in kleinem Maßstab schon mit eher moderatem Fachwissen möglich ist, repräsentieren diese Gifte besonders in Anbetracht asymmetrischer Bedrohungsszenarien eine reale Gefahr. Der Einsatz von CKS im Iran/Irak Krieg 1988, beim Terroranschlag in der Tokioter U-Bahn 1995 sowie erst jüngst im Syrienkonflikt 2013 verdeutlichen die Gegenwärtigkeit dieser todbringenden Gifte.
In dem Bestreben, die Proliferation der CKS zu unterbinden und vorhandene Bestände zu vernichten, trat 1997 das internationale Chemiewaffenübereinkommen (CWÜ) nach Ratifizierung durch 65 Unterzeichnerstaaten - darunter auch die Bundesrepublik Deutschland - in Kraft [1]. Durch das CWÜ werden Entwicklung, Herstellung, Lagerung und Einsatz chemischer Waffen verboten und ihre Vernichtung vorgeschrieben. Seit dieser Zeit wird die Einhaltung des Abkommens durch die Organisation für das Verbot Chemischer Waffen (OVCW) mit Sitz in Den Haag (NL) überwacht [2]. Die OVCW Mitgliedsstaaten repräsentieren heute ungefähr 98 % der globalen Bevölkerung und Landmasse sowie 98 % der weltweiten chemischen Industrie.
Internationale Chemiewaffenkontrolle
Organisation für das Verbot Chemischer Waffen
Die Bedeutung der OVCW für die Sicherung des Friedens wurde eindrücklich im Jahr 2013 unterstrichen, als die Organisation für ihre „extensiven Bestrebungen zur Vernichtung chemischer Waffen“ mit dem Friedensnobelpreis ausgezeichnet wurde (Abb. 1) [3]. Die Überwachungs- und Kontrolltätigkeit umfasst unter anderem die weltweite regelmäßige Entsendung von Inspektoren zu Produktions- und Lagerstätten der Industrie sowie zu Kampfstoffvernichtungs- und Entsorgungsanlagen. So wird derzeit auch die Vernichtung der CKS aus Syrien auf dem speziell ausgerüsteten US-amerikanischen Containerschiff „MV Cape Ray“ im Mittelmeer begleitet. Bei dieser Operation beteiligt sich auch die Bundeswehr an der militärischen Sicherung auf See durch die Fregatte „Augsburg“ und mit fachlichen Beratungstätigkeiten durch das InstPharmToxBw in Fragen des medizinischen C-Schutzes.
Im Hinblick auf methodisches Vorgehen und benötigte Gerätschaften kann sich die Analyse von Umweltproben deutlich von der Untersuchung biomedizinischer Proben (beispielsweise Blut, Plasma, Urin, Gewebe) unterscheiden. Die Untersuchung von Körperflüssigkeiten und Gewebe ist mit ganz eigenen wissenschaftlichen und technischen Herausforderungen verbunden. Aus diesem Grund sondiert die OVCW seit einigen Jahren auch für die Analyse biomedizinischer Proben geeignete Laboratorien und etabliert ein entsprechendes internationales Netzwerk. Seit Ende 2009 werden daher „Confidence-building Exercises for Biomedical Sample Analysis“ oder kurz „Biomedical Exercises (BME)“ durchgeführt, an denen auf freiwilliger Basis Laboratorien teilnehmen können. Die OVCW beabsichtigt, diese Übungen im Jahr 2016 in Ringversuche analog zu den Proficiency Tests für Umweltproben übergehen zu lassen, um dann für den biomedizinischen Sektor designierte Laboratorien zu identifizieren. Das InstPharmToxBw hat sich schon von der ersten Übung an mit Erfolg an allen vier bislang durchgeführten Biomedical Exercises beteiligt.
Institut für Pharmakologie und Toxikologie der Bundeswehr
Das InstPharmToxBw in München ist das nationale Kompetenzzentrum in allen Fragen des medizinischen Schutzes vor CKS und verwandten Giften. Es besitzt für diesen Zweck als einziges Institut in Deutschland die Erlaubnis zum Umgang mit CKS. Neben der Beratung politischer und militärischer Entscheidungsträger ist es auf die Optimierung vorhandener Therapien bei entsprechenden Vergiftungen sowie die Entwicklung neuer therapeutischer Ansätze und Wirkstoffe (Antidote) fokussiert. Zudem ist eine Vielzahl analytischer Methoden etabliert, die den Nachweis der CKS in biologischen Proben erlauben. Mit Hilfe gewachsener fachlicher Expertise der Mitarbeiter und modern ausgestatten Laboratorien wird das Spektrum der Analyseverfahren kontinuierlich erweitert, optimiert und an den Stand von Wissenschaft und Technik angepasst. Diese Methoden dienen vor allem der Verifikation von Vergiftungen durch CKS und stellen somit ein entscheidendes Fundament für die Zusammenarbeit mit der OVCW dar.
InstPharmToxBw ist seit 2010 gemäß der Forensiknorm DIN/ EN/ISO 17025 und der Norm für Medizinische Laboratoriumsdiagnostik DIN/EN/ISO 15189 durch die Deutsche Akkreditierungsstelle (DAkkS) akkreditiert [4]. Im Sommer diesen Jahres gelang die bestätigende Reakkreditierung für beide Normen, wodurch die Konstanz in Leistung und Kompetenz des Institutes bestätigt wurde. Das zugehörige Leistungsverzeichnis des Qualitätsmanagementsystems (QMS) liefert eine Aufstellung aller am InstPharmToxBw etablierten und akkreditierten Verfahren und kann im Bedarfsfall angefordert werden. So lassen sich im Fall einer Vergiftung deutscher Soldaten mit NKS oder HKS beispielsweise während eines Auslandseinsatzes biomedizinische Proben justiziabel analysieren, um eine Giftinkorporation zu belegen. Das etablierte DIN/EN/ISO QMS stellt neben der nationalen Reputation auch ein wichtiges Kriterium für den Status eines designierten Laboratoriums der OVCW dar. Denn zusätzlich zur Analyse interner Ringversuchsproben repräsentiert insbesondere die Teilnahme an den BME der OVCW eine externe Qualitätskontrolle zur Überprüfung der Verifikationsmethoden. So erlaubt die Zusammenarbeit mit der OVCW eine nachhaltige Sicherung der Methodenkompetenz. Ferner ermöglicht die Teilnahme an den Abschlussbesprechungen der jeweiligen BME einen vertieften Austausch mit den Spezialisten anderer Nationen und ermöglicht den Zugriff auf Informationen, die sonst nicht zugänglich wären. Diese Tagungen finden im Hauptquartier der OVCW in Den Haag im Kreise aller Wissenschaftler, die sich weltweit an der Übung beteiligt haben, statt. Nachfolgend möchten wir in Auszügen einen Einblick in die Anforderungen und Inhalte der bisherigen BME, an denen Inst- PharmToxBw teilgenommen hat, geben. Zum besseren Verständnis der Ausführungen sei jedoch an dieser Stelle in Kürze auf einige Grundlagen der Vergiftung, Toxikokinetik und chemischen Eigenschaften von CKS eingegangen.
Wirkung, Abbau und Nachweis chemischer Kampfstoffe im Körper
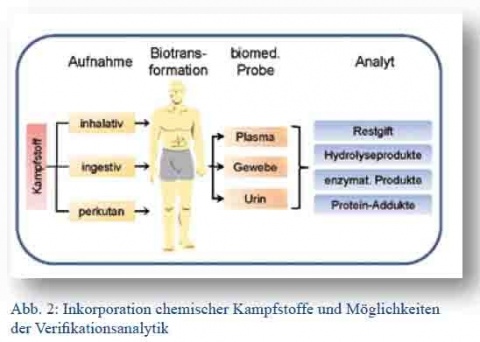
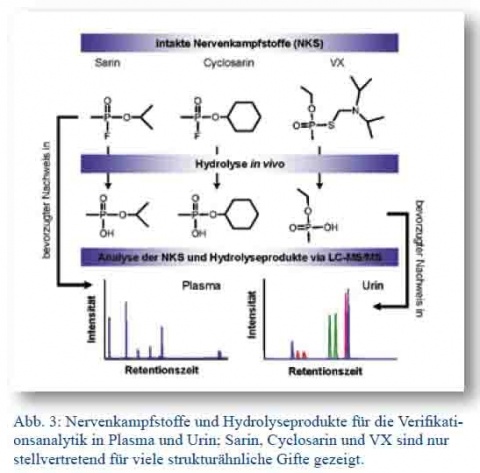
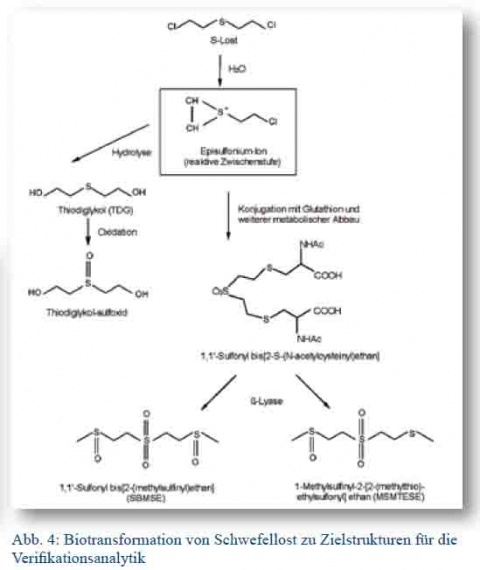
Gelangen CKS durch Inhalation der Umgebungsluft in die Lunge, durch Verschlucken in den Gastrointestinaltrakt oder penetrieren nach direktem Kontakt die Haut, durchlaufen sie nicht nur während der systemischen Verteilung über die Zirkulation vielfältige chemische Reaktionen (Biotransformation) (Abb. 2). Diese Umsetzungen können einerseits die Ursachen der Vergiftung darstellen (Hemmung der Acetylcholinesterase durch NKS, Alkylierung von Proteinen und DNA gefolgt von Blasenbildung durch HKS) oder andererseits den Abbau des Kampfstoffes zu weit weniger giftigen Produkten bewirken (Hydrolyse durch Reaktion mit Wasser oder Enzymen, Bindung an körpereigne Proteine zu Protein-Addukten) [5]. Die benannten Vorgänge verlaufen in vivo mit unterschiedlichen Geschwindigkeiten, verändern die chemische Struktur des Giftes und verursachen eine zum Teil sehr schnelle Konzentrationsabnahme im Blut. Hydrolysierte CKS sind deutlich polarer als die originären Gifte und gelangen somit wie andere Fremdstoffe oder endogene Phase II Metabolite über die Niere in den Urin (Abb. 3).So gibt es beispielsweise bei Schwefellost zwei verschiedene Abbaureaktionen (Abb. 3): Die nicht-enzymatische Hydrolyse unter Bildung von Thiodiglycol (TDG) und die durch das Enzym ß-Lyase katalysierte Umsetzung zu 1-Methylsulfinyl- 2-[2-(methylthio)-ethylsulfonyl]ethan (MSMTESE) und 1,1‘Sulfonyl bis[2-(methylsulfinyl)ethan] (SBMSE) nach Aktivierung des Schwefellosts über Glutathion (siehe Abb. 4). TDG allein repräsentiert nur einen bedingt geeigneten Expositionsbiomarker, weil es auch bei nicht-exponierten Personen im endogenen Stoffwechsel gebildet und über den Urin ausgeschieden wird [6]. Es ist zwar zu erwarten, dass die Ausscheidung nach einer Schwefellost-Vergiftung deutlich höher sein sollte, dennoch berichten Wils et al. [7] dass die TDG-Konzentrationen von Patienten aus dem Iran-Irak-Krieg der 1980er Jahre geringer waren als bei einer nicht-exponierten Kontrollgruppe. Im Gegensatz dazu sind die ß-Lyase-Produkte hoch spezifische Biomarker und damit sehr wichtige Analyten für die Verifikation einer Schwefellost-Vergiftung [8]. Da beide Reaktionswege in vivo beschritten werden, können alle benannten Produkte dem Nachweis der Schwefellost-Inkorporation dienen.
Die resultierende kurze Halbwertzeit des Giftes stellt eine wesentliche Herausforderung für den analytischen biomedizinischen Nachweis der Vergiftung dar. Sie bestimmt die Auswahl der Probenmatrix (Plasma, Urin, Gewebe), der Analyten (intaktes Gift oder dessen Addukte und Abbauprodukte) und der instrumentellen Analysemethode. Ist der unveränderte Kampfstoff nur wenige Minuten bis Stunden nach Exposition im Blut (Plasma oder Serum) detektierbar, sind seine Hydrolyse- und Biotransformationsprodukte bis zu wenigen Tagen im Urin zu fassen (Abb. 3). Die längste Verweilzeit von einigen Wochen nach Exposition haben in vivo jedoch die Protein-Addukte, die sich im Plasma finden lassen. Bieten sich für die eher unpolaren intakten Gifte gaschromatographische Nachweisverfahren (GC-MS) an, sind für die Hydrolyseprodukte und insbesondere die Protein-Addukte flüssigchromatographische Methoden erforderlich (LC-MS/MS) [9, 10]. Zudem unterscheiden sich die Verfahren der Probenvorbereitung zur Extraktion und Aufarbeitung der unterschiedlichen Analyten in den jeweiligen Matrizes erheblich [11]. All diese Spezifika sind für eine erfolgreiche Analyse zu berücksichtigen und werden in den BME durch die OVCW abverlangt. Dies erfordert hoch spezialisierte Laboratorien, die ortsfest in eine funktionierende Institutsinfrastruktur eingebunden sein müssen und daher nicht ins Feld transferierbar sind.
Biomedical Exercises der OVCW
Um einen näheren Einblick in die analytische Methodik und die besonderen Anforderungen der vier bislang absolvierten BME zu geben, werden nun ausgewählte Aspekte vorgestellt.
Im Rahmen der 1. BME, die Ende 2009 absolviert wurde, galt es in (künstlichem) Urin die Hydrolyse- und enzymatischen Produkte von NKS und Schwefellost nachzuweisen.
Wegen ihrer hohen Polarität und geringen Flüchtigkeit lassen sich diese Analyten nicht mittels Gaschromatographie erfassen und werden deshalb über LC-MS/MS nachgewiesen (Abb. 3). Während zum damaligen Zeitpunkt die Methode zur Bestimmung der NKS-Hydrolyseprodukte bereits auf einer neuen LC-MS-Anlage etabliert war [12], fehlte eine entsprechende Methodik noch für die Schwefellost-Produkte. Dennoch gelang es trotz des immensen Zeitdruckes, kurzfristig zusätzliche Methoden für TDG, sein Oxidationsprodukt TDG-Sulfoxid und die ß-Lyase-Produkte zu etablieren. So war es termingerecht möglich, alle von der OVCW geforderten Analyten zu erfassen und erfolgreich die Übung zu absolvieren.
Die aus der 1. BME von den partizipierenden Laboratorien aber auch der OVCW gesammelten Erfahrungen flossen in die 2. BME im Februar 2012 ein. Zwar galt es, neuerlich dieselben Analyten zu detektieren, doch waren deren Konzentrationen nun um den Faktor 10 geringer (1-10 ng/ml Urin), was deutlich höhere Ansprüche an einen erfolgreichen Nachweis stellte. Des Weiteren handelte es sich diesmal um natürlichen Urin, der mit den CKS Analyten versetzt war. Die vorherige Verwendung einer künstlichen Matrix hatte bei den Analysen für untypische störende Artefakte und Interferenzen gesorgt, die beispielsweise zu einer Zersetzung (In-Quellen Oxidation) des TDG während der Messung führten. Im Rahmen dieser Übung wurde bei InstPharmToxBw erstmalig eine weitere Methode zum Nachweis für ß-Lyase-Produkte eingesetzt, bei der MSMTESE und SBMSE in einem Ansatz mit Titan-(III)-chlorid zu SBMSE reduziert wurden, um den Nachweis der Schwefellost Inkorporation zu führen (Abb. 4).
Dazu wurde Plasma mit einem Überschuss an Fluorid behandelt, wodurch der an Butyrylcholinesterase (BChE) gebundene Nervenkampfstoff wieder abgelöst wurde und aus dem Plasma extrahiert werden konnte. Die extrahierten fluoridierten Kampfstoffe und Kampfstoffederivate sind lipophil und flüchtig und ließen sich daher abschließend mittels GC-MS identifizieren [12]. Bereits nach dem Sarin-Anschlag in der U-Bahn von Tokyo 1995 [13] wurde diese Methode zur Verifikation des Sarin-Einsatzes genutzt [14].
In Ergänzung dieser Methode gelang im Plasma zudem der Nachweis der CKS-Hydrolyseprodukte und erlaubte so neuerlich, ein umfassendes und richtiges Bild der Kampfstoffpräsenz zu zeichnen.
Während die bisherigen Übungen den Nachweis der kleinen Moleküle, also der intakten Gifte oder ihrer Hydrolyseprodukte notwendig machten, wurde bei der 4. BME im März 2014 erstmalig der direkte Nachweis von Protein-Addukten zweier Nervenkampfstoffe gefordert.
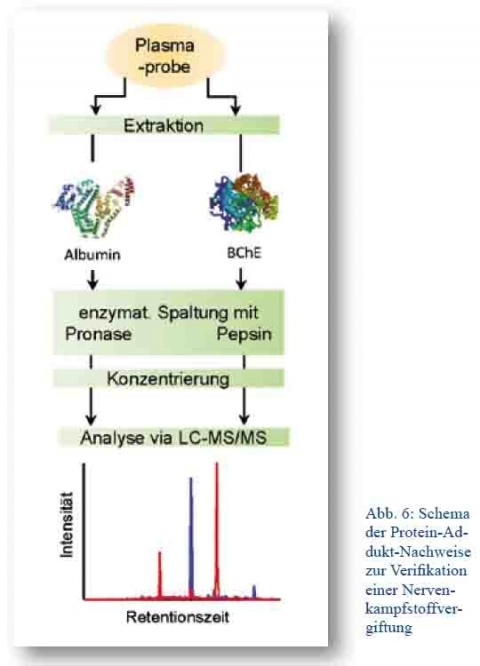
In einem fiktiven Szenario, das jedoch den Vorkommnissen in Syrien 2013 sehr ähnelte, wurde in einer Krisenregion die Ausbringung der Nervenkampfstoffe VX und Soman vermutet. Umweltanalysen an Munitionsteilen und im Boden hatten die Präsenz von VX bereits bewiesen. Unklar aber war, ob Bewohner der Region durch Aufnahme der Kampfstoffe nicht-letal vergiftet worden waren. Diesen Personen wurde Blut entnommen, um die Plasmafraktion zu gewinnen, die anschließend den teilnehmenden Laboratorien zugesandt wurde. Nun galt es durch Detektion der Protein-Addukte, welche VX und Soman mit der BChE oder dem Albumin bilden können, eine Giftinkorporation nachzuweisen. Die zugehörige Analytik unterschied sich im methodischen Vorgehen deutlich vom Nachweis der kleinen Moleküle. Wie in Abbildung 6 skizziert, wurden in einem initialen Schritt die als Adduktbildner bekannten Proteine selektiv mittels Affinitätschromatographie aus dem Plasma extrahiert. Nach einem Konzentrierungsschritt wurden die Protein- Addukte mit geeigneten Enzymen proteolytisch gespalten, um kleine peptidische Spaltprodukte zu erhalten. Diese Inkubationsmischung wurde nach neuerlicher Aufkonzentrierung anschließend flüssigchromatographisch (LC) getrennt und online mittels Tandem-Massenspektrometrie (MS/MS) hoch-selektiv detektiert.
Dieses Vorgehen erlaubte in allen Proben, denen zuvor durch die OVCW VX oder Soman zugesetzt worden war, fehlerfrei die BChE-Addukte und ihre gealterte Spezies nachzuweisen.
Die beschriebene Methodik erwies sich als höchst wertvoll und leistungsfähig, da sie erlaubte, auch deutlich sub-letale Konzentrationen der Gifte nachzuweisen (1 - 10 ng zugesetzt/ml Plasma).
Schlussfolgerungen
Wie die Gesamtheit der berichteten Übungen verdeutlicht, war InstPharmToxBw in allen Fällen in der Lage, mit großem Erfolg den Anforderungen der OVCW zu entsprechen und Proben zu analysieren, die auch in realen Expositionsszenarien auftreten können. In dem Bestreben, diese Kompetenzen zu ergänzen, ist es auch zukünftig notwendig, das Methodenspektrum zu erweitern. So gilt es, die apparativen analytischen Fähigkeiten mit modernsten Geräten auszubauen und die Qualifikation des spezialisierten Fachpersonals auf hohem Niveau zu halten. Das Gütesiegel der nationalen Akkreditierung durch die DAkkS sowie die Teilnahme an den externen Übungen der OVCW helfen dabei, einem maximalen Anspruch an Qualität und Zuverlässigkeit gerecht zu werden.
Literaturverzeichnis
- Das Chemiewaffenübereinkommen http://www.ausfuhrkontrolle. info/ausfuhrkontrolle/de/cwue/; Accessed : August 2014
- Organisation für das Verbot Chemischer Waffen www.opcw.org
- Friedensnobelpreis 2013 für die OVCW http://www.nobelprize. org/nobel_prizes/peace/laureates/2013/opcw-facts.html; Accessed: August 2014
- Tenberken O, Niessen K, John H, et al.: Akkreditierung des Instituts für Pharmakologie und Toxikologie der Bundeswehr in den Bereichen Forensik und medizinische Laboratoriumsdiagnostik. Wehrmed Mschr 2011; 55: 27-29.
- John H, Balszuweit F, Kehe K, Worek F, Thiermann H: Toxicokinetics of chemical warfare agents: nerve agents and vesicants. In: Gupta R (ed): Handbook of Toxicology of Chemical Warfare Agents. Amsterdam, Academic Press/Elsevier 2009; 755-790.
- Pristoupilov K, Pristoupil TI, Navratil T, Heyrovsky M, Senholdova Z, Pelclova D: Daily rhythm of urinary excretion of thiodiglycolic acid (TDGA) in humans under different health conditions and treatment. Anal Lett 2005; 38: 613-627.
- Wils ERJ, Hulst AG, de Jong AL, Verweij A, Boter HL: Analysis of thiodiglycol in urine of victims of an alleged attack with mustard gas. J Anal Toxicol 1985; 9: 254-257.
- Reddy MK, Nixon, C, Wyatt SA, Croley TR: A robust high-throughput sample preparation and liquid chromatography – tandem mass spectrometry method for the quantitation of ß-lyase metabolites of sulfur mustard as 1,1’-sulfonylbis-[2-(methylthio)ethane] in human urine. Rapid Commun Mass Spectrom 2013; 27: 1128- 1134.
- John H, Worek F, Thiermann H: LC-MS based procedures for monitoring of toxic organophosphorus compounds and the verification of pesticide and nerve agent poisoning. Anal Bioanal Chem 2008; 391: 97-116.
- John H, Thiermann H: Relevance of bioanalytical methods for the medical chemical defense – a review. Challenge 2012; 1: 9-13.
- John H, Thiermann H: Die Rolle und Methoden der Bioanalytik im medizinischen Schutz vor chemischen Kampfstoffen und ähnlichen Giften. Wehrmed Mschr 2009; 53: 330-336.
- Koller M, Becker C, Thiermann H, Worek F: GC-MS and LC-MS analysis of nerve agents in body fluids: Intra-laboratory verification test using spiked plasma and urine samples. J Chromatogr B 2010; 878: 1226-1233.
- Tu AT: Basic information on nerve gas and the use of sarin by Aum Shinrikyo. J Mass Spectrom Soc Jpn 1996; 44: 293-320.
- Polhuijs M, Langenberg JP, Benschop HP: New method for retrospective detection of exposure to organophosphorus antichlolinesterases: Application to alleged sarin victims of Japanese terrorists. Toxicol Appl Pharmacol 1997; 146: 156-161.
Bildquellen:
Abb. 1 a und b: Dr. John, InstPharmToxBw, privat
Abb. 5: Dr. Koller, InstPharmToxBw
Abb. 1 a): Logo der Organisation für das Verbot Chemischer Waffen am Eingangsportal des Hauptquartiers in Den Haag (NL)
Abb. 1b): Urkunde und Medaille zum Friedensnobelpreis 2013, ausgestellt im OVCW Hauptquartier
Abb. 2: Inkorporation chemischer Kampfstoffe und Möglichkeiten der Verifikationsanalytik
Abb. 3: Nervenkampfstoffe und Hydrolyseprodukte für die Verifikationsanalytik in Plasma und Urin; Sarin, Cyclosarin und VX sind nur stellvertretend für viele strukturähnliche Gifte gezeigt.
Abb. 4: Biotransformation von Schwefellost zu Zielstrukturen für die Verifikationsanalytik
Abb. 5: Plasma- und Urinproben der 3. Biomedical Exercise der OVCW
Abb. 6: Schema der Protein-Addukt- Nachweise zur Verifikation einer Nervenkampfstoffvergiftung
Datum: 22.09.2014
Quelle: Wehrmedizinische Monatsschrift 2014/9