HYPERHIDROSIS
Aus der Abteilung II – Allgemein-, Viszeral-, Gefäß-, Thoraxchirurgie und Plastische und Handchirurgie (Leitender Arzt: Flottenarzt Dr. S. Lenz) des Bundeswehrkrankenhauses Berlin (Chefarzt: Flottenarzt W. Titius, MBA)
von Yvonne Funke, Björn Dirk Krapohl und André Lieber
Eine unphysiologisch intensive sympathische Reaktion auf unter anderem emotionalen Stress kann ein sehr intensives regionales Schwitzen der Handinnenseiten und der Axillarregion bewirken.
Das kann so ausgeprägt sein, dass es für den Einzelnen Krankheitswert besitzt.
Methoden:
Internetbasierte Literaturrecherche und Auswertung von in der Chirurgischen Abteilung am Bundeswehrkrankenhaus Berlin mittels thorakoskopischer Sympathektomie behandelten Patienten.
Ergebnisse:
Vorstellung und Diskussion des Krankheitsbildes der primären Hyperhidrosis, diagnostischer und therapeutischer Möglichkeiten, deren Vor- und Nachteile sowie eigener Erfahrungen bei der Behandlung der primären Hyperhidrosis mittels thorakoskopischer Sympathektomie
Schlussfolgerungen:
„Schwitzen mit Krankheitscharakter – die Hyperhidrosis“– ist behandelbar. Es stehen konservative und operative Therapieoptionen zur Verfügung. Die thorakoskopische Sympathektomie stellt nach Ausschöpfung der konservativen Behandlungsoptionen der primären Hyperhidrosis eine Behandlungsmöglichkeit mit andauerndem Therapieerfolg dar. Bei neurovaskulären Erkrankungen (Morbus Raynaud) oder dem Chronic Regional Pain Syndrome (CRPS) kann dieses Verfahren ebenso zur Anwendung kommen und so zum Bespiel den die Komplikation einer Fraktur unterhaltenden Circulus vitiosus schnell und wirkungsvoll unterbrechen. Entsprechend der internationalen Studienlage lassen sich die Hyperhidrosis der Extremitäten und der Axillen mittels einer thorakoskopischen Sympathektomie (ETS – endoscopic thoracic sympathectomy) am besten behandeln.
Hyperhidrosis
Summary
Backgrund:
An unphysiologically pronounced sympathetic reaction on e.g. emotional stress can initiate a very intensive regional perspiration of the palms and armpits. This can be excessive thus bearing genuine illness value for the individual.
Methods:
Internet based research and evaluation of patients treated with thoracoscopic sympathectomy in the Department of Surgery at the Berlin Bundeswehr Hospital.
Results:
Presentation and discussion of the disease pattern hyperhidrosis, diagnostic and therapeutic options including advantages and disadvantages, as well as own experience in the treatment of primary hyperhidrosis by thoracoscopic sympathectomy.
Conclusions:
Pathologically excessive sweating – hyperhidrosis – is treatable by means of conservative and operative treatment modalities. In case of failure of conservative measures, thoracoscopic sympathectomy offers an option with permanent effect. In neurovascular diseases such as Raynaud’s disease and Chronic Regional Pain Syndrome (CRPS) this operative procedure is an option to instantly and reliably interrupt the vicious circle that may follow complicated courses of bone fractures. With reference to international studies, hyperhidrosis of the extremities and of the axillae is most effectively treated with endoscopic thoracic sympathectomy.
1. Einleitung
Ist Hyperhidrosis „Normal … ein Zeichen von Angst … oder vielleicht doch eine Krankheit?“
„Schwitzen ist gesund.“ – Den Satz hat jeder von uns sicherlich schon mehrfach in seinem Leben gehört, zumindest wenn es darum ging, zu körperlicher Ertüchtigung oder Arbeit zu motivieren. Schwitzen ist eine natürliche Körperfunktion. Es dient insbesondere zur Kühlung des Körpers. Die Verdunstung des Schweißes entzieht dem Körper Wärme und ist damit Bestandteil der Mechanismen zur Thermoregulation. Der Organismus wird somit vor Überhitzung geschützt.
Schwitzen kann jedoch auch zur Belastung werden, genau dann, wenn es nicht physiologisch angemessen auftritt. Menschen, die an unkontrollierbarem und übermäßigem Schwitzen (Hyperhidrosis) leiden, fühlen sich ob des Geruchs, der immer feuchtschweißigen Hände sowie der Schweißflecken in der Kleidung in Gesellschaft abstoßend und meiden daher oft gesellschaftliche Kontakte. Das vermeintlich „Gesunde“ wird für den Einzelnen zum Leid, das offenbar weitaus stärker verbreitet ist, als allgemein angenommen. So schrieb Bock im Jahr 2000: „… Rund eine Million Menschen in Deutschland sollen an „Hyperhidrosis“ leiden – an krankhaftem Schwitzen. Obwohl der Schweiß den Betroffenen das Leben zur Hölle macht, war Hyperhidrosis bisher selbst unter Medizinern kein Thema...“ (12)
Die Inzidenz der Hyperhidrosis hängt vom Kulturkreis, dem Klima und verschiedenen subjektiven Bedingungen ab. Es wird angenommen, dass die idiopathische fokale Hyperhidrosis (primäre Hyperhidrosis) bei 1-3 % einer Population auftritt. Die Häufigkeit nimmt mit der Nähe zum Äquator zu (16, 17).
2. Klinik
• Definition
Pro Tag können mehrere Liter Schweiß produziert werden. Die Hyperhidrosis beschreibt eine lokale oder generalisierte Steigerung der Schweißsekretion mit Krankheitswert. Die zugrunde liegende Dysfunktion der ekkrinen Schweißdrüsen begründet sich auf eine Übererregbarkeit des sympathischen Nervensystems und nicht auf eine Vermehrung der Schweißdrüsen. Sie kommt bei ca. 1 % der Bevölkerung vor (3, 9).
• Einteilung
Die Hyperhidrosis kann nach ihrer Ursache und der Lokalisation unterteilt werden. Kausal werden folgende Formen unterschieden:
- Primäre Hyperhidrosis Dies ist eine Ausschlussdiagnose, denn die Patienten sind ansonsten gesund. Die genaue Ursache ist nicht bekannt. Meist beginnt die Erkrankung ab der Pubertät und zeigt lebenslange Persistenz. Auslöser sind neben erhöhter Umgebungstemperatur und geringfügiger körperlicher Anstrengung insbesondere Stress und Nervosität. Gelegentlich tritt die Erkrankung spontan auf (3, 9).
- Sekundäre Hyperhidrosis Hier liegt der vermehrten Schweißproduktion eine andere Krankheit zugrunde. Sie ist somit als Symptom einer Grunderkrankung zu sehen und tritt meist generalisiert auf. Mögliche Ursachen sind (9):
• Malignome,
• Hormonelle Erkrankungen, unter anderem Hyperthyreose, Diabetes mellitus, Phäochromozytom, • Adipositas,
• Klimakterium / Menopause,
• Neurologische Erkrankungen, unter anderem Sympathikusschädigung oder Parkinson,
• Infektionskrankheiten (Tbc, Malaria),
• Medikamente,
• Psychische Belastungen (Schmerz, Stress, Panik und Angst).
Es gibt verschiedene Lokalisationen, jede Zone des Körpers kann betroffen sein. Unterschieden werden fokale Formen wie die palmare („Schweißhändchen“), axilläre („Schweißachsel“), faziale („Blushing“) und plantare („Schweißfuß“) Hyperhidrosis sowie eine generalisierte Form. Am häufigsten sind die beiden erstgenannten. Die Behandlung der primären Hyperhidrosis muss sich daher am Ausprägungsgrad und -muster orientieren (5, 9).
• Symptomatik
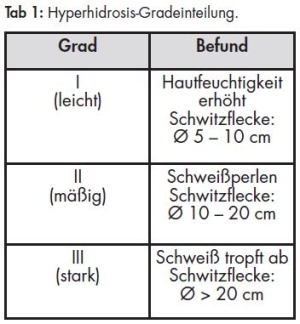
Bei Hyperhidrosis-Patienten tritt anfallartig ein verstärktes Schwitzen auf, das über die Erfordernisse der Wärmeregulation hinausgeht. Verstärkt wird dieser Effekt während des Anfalles durch das Gefühl und die Angst, das Schwitzen nicht kontrollieren zu können. So kann diese Fehlfunktion zu erheblichen sozialen und beruflichen Einschränkungen führen und damit eine ausgeprägte Verminderung der Lebensqualität hervorrufen (3). Die Hyperhidrosis wird aufgrund klinischer Befunde in drei Grade eingeteilt (Tab 1).
3. Labordiagnostik
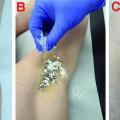
Spezielle Labor- oder Messwerte zum Nachweis einer Hyperhidrosis als Entität gibt es nicht. Eine gezielte Anamnese hingegen ist entscheidend bei der Abgrenzung einer primären von einer sekundären Hyperhidrosis. Ergeben sich Hinweise für das Vorliegen einer Grunderkrankung, so sind Diagnostik und Therapie individuell auf diese auszurichten. Als diagnostische Tests dienen der Jod-Stärke-Test nach Minor und die Gravimetrie zur Messung des transepidermalen Wasserverlustes. Beide Methoden sind hilfreich zur Verlaufsdokumentation in Therapiestudien. Ihre Aussagekraft ist allerdings aufgrund des anfallsartigen Auftretens der Hyperhidrosis eingeschränkt (9, 11).
4. Therapie
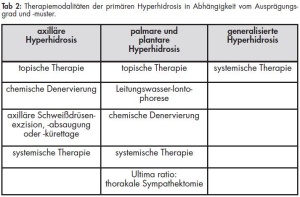
Bei der sekundären Hyperhidrosis steht die Behandlung der Grundkrankheit im Vordergrund. Die Therapie der primären Hyperhidrosis kann konservativ und auch operativ erfolgen. Vor dem Einsatz eines chirurgischen Verfahrens steht immer eine konservative Therapie. Welche Behandlungsmethode am besten geeignet ist, sollte individuell auf jeden Patienten sowie die Lokalisation abgestimmt werden und muss sich, wie in Tabelle 2 dargestellt, am Ausprägungsgrad und -muster orientieren.
4.1 konservative Therapie
Mögliche Therapieverfahren sind:
• topische Therapie mit Antiperspirantien,
• Leitungswasser-Iontophorese,
• Chemodenervierung mit Botulinumtoxin A,
• systemische Therapie: Salbei, Anticholinergika, Psychopharmaka, Tranquilizer, Sedativa, Betablocker,
• Psychotherapie.
Diese Therapieverfahren sind sehr vielfältig, oft langwierig, gelegentlich ohne anhaltenden Erfolg und insgesamt nur begrenzt langfristig erfolgversprechend (9). Lediglich milde Formen der primären Hyperhidrosis haben gute Erfolgsaussichten (2). Es handelt sich bei diesen Behandlungen in der Regel um eine Dauertherapie. Nur der Verschluss der Schweißdrüsengänge mit dem Antitranspirant Aluminiumchloridhexahydrat (AlCl3(OH)6) kann zumindest zum mehrmonatigen Versiegen der Schweißsekretion führen. Hierbei müssen die in den handelsüblichen Deos verwendeten Dosen weit überschritten werden. Eine effektive Konzentration liegt bei 20 % AlCl3(OH)6. In dieser Konzentration wirkt die Substanz oft stark hautreizend, was Therapiepausen notwendig macht und oft zum Abbruch der Behandlung zwingt.
4.2 Konventionelle operative Therapie
• Lokale Schweißdrüsenexzision
Über mehrere Hautinzisionen erfolgt eine radikale Exzision des schweißdrüsentragenden Hautareals bei einzeitigem Wundverschluss. Nachteile: Wundheilungsstörung, Hautnekrosen, hypertrophe Narben mit Tendenz zur Kontraktur, dehiszente, kosmetisch störende Narben, Restschwitzen des nicht exzidierten Randareals. Fazit: Aufgrund der Nachteile und im Vergleich zu anderen lokal-chirurgischen Maßnahmen ist diese Methode nur im Einzelfall zu empfehlen.
• Subkutane Schweißdrüsenkürettage
Über ein oder mehrere Hautinzisionen erfolgt die Unterminierung des schweißdrüsentragenden Hautareals mit anschließender Kürettage der Schweißdrüsenknäuel und Nervenausläufer an der Dermisunterseite (13, 15). Nachteile: Wundheilungsstörung, Hautnekrosen, Hämatome, Lymphfistelund Lymphzystenbildung. Fazit: Es besteht eine erhöhte Rezidivgefahr durch inkomplette Entfernung.
• Subkutane Saugkürettage
Über Hautinzisionen erfolgt eine fächerförmige Unterminierung des schweißdrüsentragenden Hautareals. Anschließend wird das Unterhautfettgewebe inklusive der Nervenausläufer abgesaugt. Die Schweißdrüsen können zusätzlich kürettiert und abgesaugt werden (14, 15). Nachteile: Hämatome, Lymphfistel- und Lymphzystenbildung, selten Wundheilungsstörungen oder Hautnekrosen. Fazit: Es besteht eine erhöhte Rezidivgefahr durch inkomplette Entfernung. Streng genommen handelt es sich bei unzureichendem langfristigem Therapieerfolg nicht um ein Rezidiv sondern um eine initial unzureichend behandelte Erkrankung.
• CT-gesteuerte perkutane Sympathikolyse
Zur Ausschaltung der Ganglien wird CT-gesteuert konzentrierter Alkohol injiziert. Diese Methode beruht auf dem gleichen Prinzip wie die thorakoskopische Sympathektomie (8). Die lokale periphere Sympathektomie wurde in Einzelfällen beim Morbus Raynaud an der Hand angewandt (13). Hierbei wurde der arterielle Plexus sympathicus an den Arterien des distalen Unterarmes und/oder der Hand durch Strippen der Adventitia entfernt. Da diese Technik einen nicht unerheblichen Weichteileingriff in einer Belastungszone, nämlich der Hand, darstellt, sind die Indikationen hierfür als limitiert anzusehen. Beschreibungen bei palmarer Hyperhidrosis fehlen bei dieser Methode, die nur der Vollständigkeit halber nicht ungenannt bleiben soll.
4.3 Minimal invasive operative Therapie - Thorakoskopische Sympathektomie
Kux und Wittmoser beschrieben in den 50er und 60er Jahren erstmals ausführlich die thorakoskopische Sympathektomie und ihre weitläufigen Indikationen. In Folge dessen wurde diese Methode mit anhaltendem Erfolg durchgeführt und weiterentwickelt. Seit Jahren ist sie als operative Methode anerkannt und die Methode der Wahl bei therapieresistenter Hyperhidrosis der oberen Extremität (4, 5).
In minimal invasiver Technik erfolgt mittels videoassistierter Thorakoskopie die Darstellung und Blockade des Truncus sympathicus (9). Der Eingriff kann einzeitig auf beiden Seiten durchgeführt werden.
• Operationsindikation
Eine Indikation zur endoskopischen Blockade von sympathischen Nervenfasern im Thoraxbereich stellt die primäre lokale Hyperhidrosis mit ausgeprägtem Leidensdruck des Patienten dar. Konservative Behandlungsmethoden waren nicht oder nur unzureichend erfolgreich (2, 18). Weitere in der Literatur beschriebene Indikationen sind die Erythrophobie und periphere Angiopathien, zum Beispiel Morbus Raynaud oder Morbus Bürger sowie das CRPS (Chronic Regional Pain Syndrome; frühere Synonyma: Morbus Sudeck, Algodystrophie, sympathische Reflexdystrophie) (3, 5). Insbesondere bei Morbus Sudeck stellt die Sympathektomie eine gemessen an den Folgen der Erkrankung einfache, schnelle und wirkungsvolle Methode dar, um den Circulus vitiosus zu unterbrechen, der die Komplikation einer Fraktur unterhält.
• Formen der thorakoskopischen Sympathektomie
In der Literatur finden sich folgende Optionen (3, 8, 10, 18):
- Sympathikotomie: Durchtrennung des Truncus sympathicus, am ersten Ganglion zur Behandlung der fazialen Hyperhidrosis und Erythrophobie,
- Sympathektomie (ETS): Partielle Resektion des Truncus sympathicus des zweiten bis maximal fünften Brustganglions zur Behandlung der palmaren und axillären Hyperhidrosis, - thermische Inaktivierung des Ganglions: Zerstörung entweder elektrisch oder durch Ultrazision,
- Sympathikus-Clipping (ETSC): Blockade mittels Titan-Clips in Höhe des 1. / 2. Brustganglions bei fazialer und palmarer Hyperhidrosis und in Höhe des 3. Ganglions bei axillärer Hyperhidrosis; grundsätzliche Möglichkeit der Reversibilität durch Entfernung der Clips in einem sehr kurzen postoperativen Zeitintervall. Da allen genannten Eingriffen am Sympathikus die Blockade der Nervenimpulse gemeinsam ist, hat sich die Bezeichnung „endoskopische Sympathikusblockade“ (ESB) etabliert.
Das Ausmaß und die Höhe der Resektion werden in der Literatur schon seit Jahren breit diskutiert. Laut aktueller Studienlage erzielt die Sympathektomie im Bereich von T3 und T3-5 sowohl für die palmare als auch für die axilläre Hyperhidrosis sehr gute Ergebnisse und kann der Sympathektomie von T2-4 vorgezogen werden. Hinsichtlich der Höhenangaben bezieht man sich dabei auf die jeweilige Rippe (18).
Postoperativ wurden bei einer ETS von T3-4 weniger Fälle von kompensatorischem Schwitzen beobachtet. Das Risiko einer Läsion des Ganglion stellatum konnte so ebenfalls erheblich reduziert werden (7, 10).
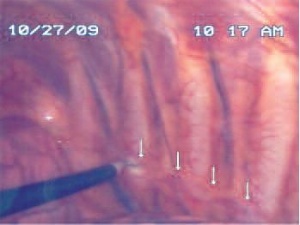
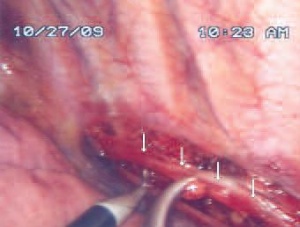
• Operationstechnik
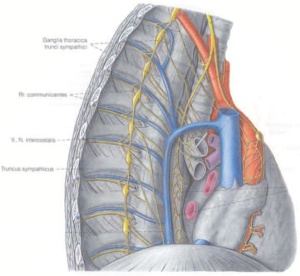
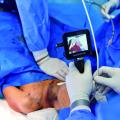
Da das autonome Nervensystem symmetrisch- paarig angelegt ist, geschieht der Eingriff nacheinander beidseits in gleicher Art und Weise. Über zwei bis drei kleine Hautschnitte am lateralen Thorax werden in die Axilla und kaudal davon 5-mm-Trokare interkostal platziert. Über diese werden eine 5- mm-Optik und die Instrumente eingebracht. Der sympathische Grenzstrang schimmert durch die transparente Pleura parietalis hindurch und liegt gut sichtbar an der Thoraxhinterwand. Die Pleura wird in diesem Bereich eröffnet und der Sympathikus freigelegt. Nun erfolgen die Durchtrennung, die teilweise Resektion, die Blockade mit Metall- Clips oder die Inaktivierung durch Elektrokauterisation. Dabei wird das Ganglion über dem ersten Rippenköpfchen geschont, da seine Schädigung zu einem Horner-Syndrom führen kann. Das Ausmaß der Sympathektomie richtet sich hauptsächlich nach der Lokalisation der Hyperhidrosis (18). Vor Entfernung der Trokare wird über diese beidseits jeweils ein Pleuracath-Katheters eingelegt. Über diese Katheter kann ein verbliebener pleuraler Resthohlraum drainiert werden. Abschließend wird die Wunde mittels Subkutannaht und Steri-Strips verschlossen. Der Patient kann bei komplikationslosem Verlauf und Ausschluss eines Pneumothorax nach Entfernung der Drainagen gegebenenfalls auch am ersten postoperativen Tag entlassen werden.
• Risiken und Komplikationen
Nutzen und Risiko müssen auch bei diesem elektiven Eingriff eingehend mit den Patienten erörtert und im Konsens mit Alter, Konstitution, Vorerkrankungen sowie Art und Ausprägung der Hyperhidrosis – eben der Bestimmung des individuellen Leidensdruckes – abgewogen werden. Neben den allgemeinen Operationsrisiken wie Blutung, Verletzung von Nachbarstrukturen, Infektion, Wundheilungsstörung, Thrombose und Embolie gibt es wenige besondere Komplikationen. Die sicher beeindruckendste Komplikation besteht in der Ausbildung eines Horner-Syndroms (Symptomenkomplex aus Miosis, Ptosis und Enophthalmus). Sie ist mit 0,7 % (18) relativ selten und wurde in der eigenen Einrichtung noch nicht beobachtet. Dieses Syndrom kann bei Schädigung von Nervenfasern des untersten Halsganglions (Ganglion cervicale inferius, in der Regel Teile des Ganglion stellatum) entstehen, insbesondere bei Verwachsungen mit dem ersten Brustganglion. Ein unmittelbar postoperativ auftretender residueller Pneumothorax wird mittels Pleuracath- Katheter drainiert. Sollte dies nicht ausreichen und der pleurale Hohlraum persistent sein (1,1 %), kann die Einlage weiterer Pleuradrainagen erforderlich werden.
Des Weiteren können intrathorakale Veränderungen postinflammatorisch oder nach früheren Operationen wegen teilweise ausgedehnter pleuraler Adhäsionen die Durchführung des Eingriffes erheblich erschweren oder unmöglich machen. Dadurch kann letzten Endes der Erfolg dieser Operationsmethode präoperativ nie garantiert werden (9, 10).
• Nebenwirkungen
Eine Nebenwirkung ist nicht mit einer Komplikation gleichzusetzen! Vorhersehbare mögliche postoperative Nebeneffekte werden der aktuellen Studienlage zufolge vom Patienten als weniger gravierend empfunden als die Ausgangssymptome. Die häufigste Nebenwirkung stellt mit über 50 % das kompensatorische Schwitzen, zum Beispiel am Rumpf, dar (5, 7). Gelegentlich (4,6 %) entwickelt sich auch ein gustatorisches Schwitzen bei bestimmten Geruchs- und Geschmackswahrnehmungen (10). Durch eine CT-gestützte vorübergehende Sympathikusblockade kann diese Hauptnebenwirkung aber bereits präoperativ abgeschätzt werden (8).
• Vorgehen am BwKrhs Berlin
Patienten mit ausgeschöpfter konservativer Behandlung der axillären und palmaren Hyperhidrosis und ausgeprägtem Leidensdruck werden nach gegebenenfalls nochmaliger konsiliarischer Vorstellung in der FU III (Ambulanz der Abteilung Dermatologie) über plastisch- chirurgische Vorgehensweisen und die thorakale Sympathektomie (ETS) aufgeklärt. Eine Gravimetrie oder Sudometrie wird nicht durchgeführt. Bei einer Entscheidung für die ETS erfolgt die allgemeine thoraxchirurgische Risikoabklärung und OP-Vorbereitung.
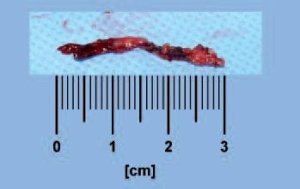
Bei der thorakoskopischen Sympathektomie, die seit 2008 ausschließlich mit 5-mm-Instrumenten und einer 5-mm-Optik durchgeführt wird, werden zwei bis drei Segmente des Truncus sympathicus reseziert und zur histologischen Untersuchung gegeben. Es wird angestrebt, anlässlich einer Operation beide Seiten zu behandeln. Von 1998 - 2001 erfolgte die Behandlung in zwei Operationen mit einem zeitlichen Abstand von ca. 6 Wochen. Seit 2001 werden beide Seiten in einer Narkose operiert. Die Pleuradrainagen (beidseits je ein Pleuracath-Katheter) können regelhaft am ersten postoperativen Tag wieder entfernt werden. In fast allen Fällen berichteten die Patienten bereits bei der Umlagerung vom OP-Tisch in das Pflegebett von trockenen warmen Handinnenflächen.
Bisher wurden am Bundeswehrkrankenhaus Berlin insgesamt 104 Patienten mit Hyperhidrosis mittels einer thorakoskopischen Sympathektomie behandelt. Bei allen Patienten stellte sich der angestrebte Behandlungserfolg sofort, das heißt, innerhalb circa einer Stunde nach der ETS, ein. Bei 7 der von 2006 - 2010 operierten 61 Patienten musste eine intensivierte postoperative Schmerztherapie für einen Zeitraum von bis zu 5 Tagen durchgeführt werden. 4 Patienten beklagten ein kompensatorisches Schwitzen (Bauch, Füße). Ein Horner-Syndrom, Herzrhythmusstörungen, ein Pleuraerguss oder ein persistierender postoperativer Pneumothorax wurden im Zusammenhang mit einer thorakoskopischen Sympathektomie nicht beobachtet.
Die thorakoskopische Sympathektomie erfordert nach der Entlassung aus der stationären Behandlung keine speziellen Maßnahmen im Rahmen der Rekonvalezenz. Die Patienten sind bei unkompliziertem Verlauf nur kurzzeitig in ihrer Dienstausübung eingeschränkt. Bei speziellen Verwendungen muss jedoch die Durchführbarkeit des Verfahrens unter der Frage einer möglichen langfristigen Einschränkung der speziellen Tauglichkeit und Eignung erfolgen (Taucherverwendung, spezielle fliegerische Verwendungen) individuell beurteilt werden.
• Prognose
Das thorakoskopische Vorgehen erreicht nach Angaben in der Literatur in mehr als 90 % der Fälle eine dauerhafte erfolgreiche Behandlung der fazialen Hyperhidrosis und in 98 % der palmaren. Bei der axillären Hyperhidrosis wird eine dauerhafte Erfolgsrate von 70 bis 75 % beschrieben. Begleitend ist bei 50 % der Patienten eine Verbesserung der plantaren Hyperhidrosis in der Literatur beschrieben (18), was jedoch neurophysiologisch noch unklar ist. Die Rezidivrate beträgt 0 bis 5 % (6). Die CT-gestützte Sympathikolyse erreicht ebenfalls eine Erfolgsrate von 70 bis 80 %, allerdings ist dieser Erfolg meist nicht von Dauer (1).
• Vorteile
Die thorakoskopische Sympathektomie weist im Vergleich zu anderen operativen Methoden folgende Vorteile auf (5):
• Senkung der postoperativen Morbidität,
• Senkung der Hospitalisierungszeit,
• Senkung der Arbeitsunfähigkeitszeit,
• besseres kosmetisches Ergebnis.
5. Schlussfolgerungen
Die primäre Hyperhidrosis kann nach Ausschöpfung konservativer Behandlungsverfahren mittels der thorakoskopischen Sympathektomie erfolgreich behandelt werden. Die am Bundeswehrkrankenhaus Berlin erzielten Ergebnisse sowie die Komplikationsrate und Nebenwirkungen seit Einführung dieses Verfahrens entsprechen den in der Literatur mitgeteilten Ergebnissen. Das Verfahren kann zur Behandlung weiterer Erkrankungen (Morbus Sudeck, Morbus Raynaud) den Patienten als therapeutische Alternative angeboten werden.
Fotos (Abb. 2, -5): Oberstarzt Dr. Lieber, Abteilung II, BwKrhs Berlin
Literatur:
- Adler OB, Engel A, Rosenberger A, Dondelinger R: Palmar hyperhidrosis CT guided chemical percutaneous thoracic sympathectomy. Rofo Fortschr Geb Rontgenstr Neuen Bildgeb Verfahr 1990; 153: 400–403.
- Claes G, Drott C: Hyperhidrosis. Lancet 1994; 343: 247–248.
- Dewey TM, Herbert MA, Hill SL, Prince SL, Mack MJ: One-Year Follow-Up After Thoracoscopic Sympathectomy for Hyperhidrosis: Outcomes and Consequences. Ann Thorac Surg 2006; 81: 1227-1233.
- Edmonson RA, Banerjee AK, Rennie JA: Endoscopic transthoracic sympathectomy in the treatment of Hyperhidrosis. Ann Surg 1992; 215(3):289-293.
- Ghisletta N, Habicht J, Stulz P.: Videoassistierte thorakoskopische Sympathektomie: Indikationsspektrum und eigene Resultate (1995-1997). Schweiz Med Wochenschr 1999;129:985-992.
- Herbst F, Plas EG, Függer R, Fritsch A.: Endoscopic thoracic sympathectomy for primary hyperhidrosis of the upper limbs: a critical analysis and long-term results of 480 operations. Ann Surg 1994;220:86–90.
- Li X, Tu YR, Lin M, Lai FC, Chen JF, Dai ZJ.: Endoscopic Thoracic Sympathectomy for Palmar Hyperhidrosis: A Randomized Control Trial Comparing T3 and T2-4 Ablation. Ann Thorac Surg 2008;85:1747-1751.
- Miller DL, Force SD.: Temporary Thoracoscopic Sympathetic Block for Hyperhidrosis. Ann Thorac Surg 2008;85:1211-1216.
- O. Schega, W. Frank.: Thorakoskopische Therapie der Hyperhidrosis. Brandenburgisches Ärzteblatt 8/2004;14:253.
- Schmidt J, Bechara FG, Altmeyer P, Zirngibl H.: Endoscopic Thoracic Sympathectomy for Severe Hyperhidrosis: Impact of Restrictive Denervation on Compensatory Sweating. Ann Thorac Surg 2006;81:1048-1055.
- Tetteh HA, Groth SS, Kast T et al.: Primary Palmoplantar Hyperhidrosis and Thoracoscopic Sympathectomy: A New Objective Assessment Method. Ann Thorac Surg 2009; 87: 267-275.
- Bock C.: Eine Million Menschen schwitzen krankhaft. Spiegel Online 07/2000 at: www.spiegel.de/wissenschaft/mensch/ 0,1518,85730,00.html.
- Balogh B, Mayer W, Vesely M, Mayer S, Partsch H, Piza-Katzer H.: Adventitial stripping of the radial and ulnar arteries in Raynaud's disease. J Hand Surg Am. 2002;27(6):1073-1080.
- Vorkamp T, Foo FJ, Khan S, Schmitto JD, Wilson P.: Hyperhidrosis: evolving concepts and a comprehensive review. Surgeon 2010; 8(5):287-292.
- Schlereth T, Dieterich M, Birklein F.: Hyperhidrosis--causes and treatment of enhanced sweating. Dtsch Arztebl Int 2009;106(3):32-37.
- Adar R, Kurchin A, Zweig A, Mozes M.: Palmar hyperhidrosis and its surgical treatment: a report of 100 cases. Ann Surg 1977; 186: 34-41
- Leung AK, Chan PY, Choi MC.: Hyperhidrosis. Int J Dermatol 1999; 38: 561-7
- Cerfolio RJ, Milanez De Campos JR, Bryant AS, Connery CP, Miller DL, DeCamp MM, McKenna RJ, Krasna MJ.: The Society of Thoracic Surgeons Expert Consensus for the Treatment of Hyperhidrosis. AnnThorac Surg 2011; 91:1642-8
- Benninghoff; Drenckhahn: Anatomie Band 2, 16.Aufl: Makroskopische Anatomie, Histologie, Embryologie, Zellbiologie. Urban und Fischer Verlag, Elsevier GmbH München 2004; 603
Datum: 31.01.2012
Quelle: Wehrmedizinische Monatsschrift 2011/10