UNTERSUCHUNGEN ZUR SICHERHEIT VON DERMOPHARMAZEUTIKA IN DER BUNDESWEHR
Aus der Laborabteilung II Veterinärmedizin (Abteilungsleiter: Oberstveterinär Dr. T. Reiche) des Zentralen Instituts des Sanitätsdienstes der Bundeswehr Koblenz, Außenstelle Mainz¹ (Institutsleiter: Flottenarzt Dr. H. Bergmann) und der Laborabteilung II Veterinärmedizin des Zentralen Instituts des Sanitätsdienstes der Bundeswehr Kiel² (Abteilungsleiter und Institutsleiter: Oberstveterinär Dr. H.-H. Pott)
von Mirko Köhler², Stefanie Hallack¹ und Daniel Werth¹
Zusammenfassung
Hintergrund:
Aufgrund einer Warnmeldung des Bundesinstituts für Risikobewertung bezüglich einer Keimbelastung von Duschgel mit Enterobacter gergoviae wurden die Laborabteilungen Veterinärmedizin aufgefordert,
mikrobiologische Untersuchungen von in den Bundeswehrapotheken selbst hergestellten, gleichartigen Produkten durchzuführen.
Methoden:
Nach einer Validierung der erforderlichen Prüfmethode, die in Anlehnung an das Europäische Arzneibuch (Ph. Eur. 2008) etabliert wurde, wurden sämtliche in den Sanitätseinrichtungen asservierten Chargen mikrobiologisch untersucht.
Ergebnisse:
Bei keiner Charge wurde eine Keimbelastung festgestellt.
Schlussfolgerungen:
Die Ergebnisse zeigen, dass sowohl im Hinblick auf die Herstellung als auch auf die mikrobiologische Untersuchung die Einrichtungen der Bundeswehr in der Lage sind, die geforderten Leistungen qualitätsgesichert zu bearbeiten.
Examination for pharmaceutical safety in the German Federal Armed Forces
Summary
Background:
Based on a warning message of the German Federal Institute for Risk Assessment (BfR) concerning microbiological exposure of shower gel with Enterobacter gergoviae, Veterinary Laboratory Sections were requested to perform microbiological testings of similar products, which were self-produced in pharmacies of the German Federal Armed Forces.
Methods:
According to the European Pharmacopoeia, after validating the required test method, samples of all retained batches in sanitary facilities became subject to a microbiological examination.
Results:
A microbiological exposure could be detected in none of the tested batches.
Conclusions:
These results confirm the quality assured performance of all required services provided by the facilities of the German Fe - deral Armed Forces, in view of both fabrication and microbiological controlling.
1. Einleitung
In den Laborabteilungen II – Veterinärmedizin der Zentralen Institute des Sanitätsdienstes der Bundeswehr werden routinemäßig biologische Prüfungen nach Europäischem Arzneibuch (EuAB) durchgeführt. Dies sind neben Untersuchungen zum Nachweis von Endotoxinen und anderen Fieber erzeugenden Stoffen auch alle erforderlichen mikrobiologischen Prüfungen. Sowohl die Prüfung auf Sterilität als auch die mikrobiologische Prüfung nicht steriler Produkte einschließlich des Nachweises spezifizierter Mikroorganismen werden dabei im Routinespektrum durchgeführt.
Hintergrund der im nachfolgenden beschriebenen Untersuchungen war eine Warnmeldung des Bundesinstituts für Risikobewertung (BfR) vom 13. Juli 2009 (1).
„Dem Bundesinstitut für Risikobewertung liegen Daten zu einer Charge Duschgel vor, die stark mit dem Keim Enterobacter gergoviae belastet war. Das Institut hat eine gesundheitliche Risikobewertung vorgenommen, um das Gefährdungspotenzial durch keimbelastetes Duschgel abzuschätzen und den zuständigen Behörden Bewertungshilfen zu geben....”
Bei der Bestimmung des Mikroorganismengehalts zeigte sich, dass die Probe mit 105 Kolonie bildenden Einheiten (KbE) belastet war. Es ist zwar davon auszugehen, dass die meisten Bakterien beim Abspülen des Duschgels von der Haut ebenso abgespült werden, eine Infektion über verletzte Haut oder empfindliche Schleimhautareale jedoch möglich ist. Enterobacter gergoviae gehören zu einer Bakterienart, die überall in der Umwelt vorkommt. Sie können bei gesundheitlich geschwächten Menschen oder bei Menschen nach einem chirurgischen Eingriff gelegentlich zu bakteriellen Infektionen führen. Die Keime sind oftmals gegen Antibiotika resistent, was eine Behandlung erschwert.
Das BfR kommt zu der Bewertung, dass ein Duschgel, das mit 105 KbE Enterobacter gergoviae pro Gramm belastet ist, zum einen den Grenzwert von 1x103 KbE/g oder ml für die mesophile, aerobe Gesamtkeimzahl für kosmetische Mittel des allgemeinen Gebrauchs entsprechend „The SCFP’s Notes of Guidance for the Testing of Cosmetic Ingredients and their Safety Evaluation“ nicht nur nicht einhält, sondern das Produkt auch als nicht sicher für die menschliche Gesundheit anzusehen ist (4, 11, 12, 13).“
Die Bakterien der Gattung Enterobacter gehören zur Familie der Enterobacteriacae. Es handelt sich um eine Gruppe von gramnegativen, fakultativ anaeroben, stäbchenförmigen Bakterien. Sie gehören der normalen Darmflora an, kommen darüber hinaus aber in fast allen Lebensräumen vor. Die Keime sind ubiquitär verbreitet und werden regelmäßig in Stuhl- beziehungsweise Kotproben von Mensch und Tier, in Pflanzen und Material von Pflanzen, in Wasser, in Insekten und in Milchprodukten festgestellt (3, 9). Ebenso gelang der Nachweis derartiger Mikroorganismen aus Kosmetika (2).
Hinsichtlich der Bewertung von Entero - bacter gergoviae kommt erschwerend hinzu, dass viele Stämme multiresistent gegen Antibiotika sind. In einer Studie in China wurde der Stamm Enterobacter gergoviae 3773 untersucht, der Resistenzen gegen Ampicillin, Piperacillin, Carbenicillin, Cephalothin, Cephaloridin, Cefazolin und Cefuroxin zeigte (6). Weitere Resistenzen bestanden gegenüber Streptomycin, Kanamycin, Gentamycin und Trimethoprim-Sulfamethoxazol (7, 8). In einer epidemiologischen Studie zu ESBL (Extended-Spectrum ß-Lactamase) bei Enterobacter-Isolaten in einem spanischen Krankenhaus wurde festgestellt, dass dort ein resistenter Enterobacter gergoviae- Stamm vorkam, der sich bereits seit mindestens 10 Jahren etabliert hatte. Dieser Stamm war auch der erste Enterobacter, bei dem ESBL festgestellt wurde (5). Von ähnlichen Problemen wurde auch aus einer Neugeborenenstation berichtet (10).
Von Seiten der Fachabteilungen VII und VIII im Sanitätsamt der Bundeswehr wurde nach Bekanntwerden der Warnmeldung des BfR umgehend eine Untersuchung sämtlicher aktuell im Umlauf befindlicher Chargen „alkalifreie Waschlotion“ angewiesen.
2. Methoden
2.1 Probenvorbereitung
Nicht sterile Arzneimittel sind Zubereitungen zur topischen oder andersartigen lokalen Anwendung, die laut Arzneibuch nicht steril sein müssen. Ebenso sind dies Zubereitungen zur oralen, rektalen und transdermalen Anwendung.
Zur Probenvorbereitung wird die für die Prüfung erforderliche Probenmenge unter Vermeidung einer versehentlichen Kontamination entnommen. Je nach Art des zu untersuchenden Produktes wird das Probenmaterial wie in der Verfahrensanweisung „Probenvorbereitung zur mikrobiologischen Prüfung nicht steriler Arzneimittel“ beschrieben aufgearbeitet. Im weiteren Verlauf der Prüfung kommt die als Flüssigkeit X bezeichnete Verdünnung zum Einsatz.
Alkalifreie Waschlotion wurde zur Untersuchung auf mikrobielle Verunreinigung bei nicht sterilen Produkten gemäß Ph.Eur. 2008 Kapitel 2.6.12 (Zählung der gesamten, lebensfähigen, aeroben Keimzahl) und Kapitel 2.6.13 (Nachweis spezifizierter Mikroorganismen) zum Ausschluss von Pseudomonas aeruginosa und Staphylococcus aureus sowie von höchstens 10 gegen Gallesalze resistente Bakterien je Gramm oder Milliliter des Arzneimittels untersucht. Hierbei kamen die nachfolgend beschriebenen, von den jeweiligen Kontrollleitern der Herstellung im Prüfauftrag angeforderten Prüfmethoden zur Anwendung.
Zur Probenvorbereitung werden sämtliche, für die Prüfung erforderlichen Behältnisse nach Zufallsverteilung ausgewählt und die erforderliche Probenmenge unter Vermeidung einer versehentlichen Kontamination entnommen. Dazu werden 10 ml des Produktes in Natriumchlorid- Pepton-Pufferlösung pH 7±0,5 zu 100 ml verdünnt. Der pH-Wert wird auf einen Wert zwischen 6 und 8 eingestellt. Die so hergestellte Mischung wird durch 10-maliges Rühren oder Schütteln homogenisiert und kann anschließend weiter verdünnt werden, zum Beispiel 10-1, 10-2 oder 10-3. Für den Nachweis von Gallesalz-resistenten Bakterien wird zur Verdünnung eine Casein-Sojapepton- Bouillon verwendet. Die Mischung 1 g Duschgel ad 9 ml Casein-Sojapepton-Bouillon wird homogenisiert (Flüssigkeit X) und bei 20 bis 25°C für 2 bis 5 Stunden bebrütet, um eventuell vorhandene Bakterien zu reaktivieren, ohne jedoch eine Vermehrung anzuregen. Diese Grundverdünnung kann anschließend ebenfalls weiter verdünnt werden, zum Beispiel 10-1, 10-2 oder 10-3.
2.2 Zählung der aeroben Mikroorganismen
Die Zählung der Bakterien oder Hefe- und Schimmelpilze erfolgt im Gussplattenverfahren. Falls erforderlich, wird das Produkt so verdünnt, dass eine voraussichtliche Zahl von höchstens 250 Kolonien (Zählung der TAMC) und 50 Kolonien (Zählung der TYMC) erhalten wird. Hierfür werden in je 2 leere Petrischalen je 1 ml des vorbereiteten Produktes oder der erforderlichen vorbereiteten Verdünnungen, zum Beispiel 10-1/10-2/10-3 mit 16 ml verflüssigtem und auf mindestens 45°C abgekühltem CASO-Agar oder Sabouraud- Agar gegossen. Der Probenansatz wird mit dem Agar durch Rotieren der Petrischale auf der Tischoberfläche in Form einer Acht vermischt. Die Bebrütung erfolgt beim Nachweis von Bakterien bei 30°C bis 35°C für 3 bis 5 Tage und beim Nachweis von Hefe- und Schimmelpilzen bei 20 bis 25°C für 5 bis 7 Tage, sofern eine kürzere Bebrütungszeit keine zuverlässigeren Ergebnisse ergibt.
Während und nach der Bebrütungszeit werden die Kulturen auf makroskopisch sichtbares Wachstum von Mikroorganismen überprüft. Wachstum von Mikroorganismen ist als kompakte Einlagerung im Nährmedium erkennbar. Die Kolonien, die sich entwickelt haben, werden gezählt. Die Ergebnisse werden aus den Platten errechnet, welche die meisten Kolonien aufweisen. Dabei ist zu berücksichtigen, dass weiniger als 250 Kolonien je Platte für die Zählung von Bakterien und weniger als 50 Kolonien je Platte für die Zählung von Hefe- und Schimmelpilzen das Maximum für eine zufriedenstellende Auswertung darstellen.
2.3 Nachweis spezifizierter Mikroorganismen
2.3.1 Nachweis Gallensalz-resistenter gramnegativer Bakterien
Zur Untersuchung auf Gallensalz-resistente gramnegative Bakterien wird das vorbereitete Produkt (=Flüssigkeit X) bei 20°C bis 25°C 2 bis 5 Stunden bebrütet. Die Flüssigkeit wird anschließend aufgeschüttelt. Davon wird eine Menge, die 1 g oder 1 ml Probe entspricht, in 100 ml MOSSEL-/MacConkey-Bouillon übertragen und für 24 bis 48 Stunden bei 30°C bis 35°C gebrütet. Subkulturen werden auf VRBD-/MacConkey-Agar angelegt und 18 bis 24 Stunden bei 30°C bis 35°C inkubiert. Aus jeder Kultur werden Subkulturen auf VRBD- /MacConkey-Agar angelegt, um die gewachsenen Mikroorganismen selektiv zu isolieren. 18 bis 24 Stunden lang wird bei 30°C bis 35°C bebrütet. Das Produkt entspricht der Prüfung, wenn sich keine Kolonie gramnegativer Bakterien auf einer der Platten entwickelt.
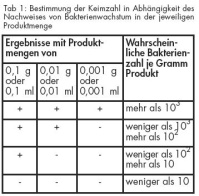
Zur qualitativen Bestimmung wird die vorbereitete Flüssigkeit X und/oder Verdünnungen dieser, die 1,0 g (= 10 ml Flüssigkeit X), 0,1 g (= 1 ml Flüssigkeit X), 0,01 g (= 0,1 ml Flüssigkeit X) oder 1,0 ml (= 10 ml Flüssigkeit X), 0,1 ml(= 1 ml Flüssigkeit X), 0,01 ml (= 0,1 ml Flüssigkeit X) des Produktes enthalten, in geeignete Mengen der MOSSEL-/MacConkey- Bouillon verimpft. Aus jeder Kultur werden Subkulturen auf VRBD-/MacConkey-Agar angelegt und anschließend wird für 18 bis 24 Stunden bei 30°C bis 35°C bebrütet. Ein Wachstum gut entwickelter, meist roter Kolonien gramnegativer Bakterien zeigt ein positives Ergebnis an. Die geringste Menge des Produktes, welche ein positives Ergebnis zeigt, ebenso die größte Menge, welche ein negatives Ergebnis zeigt, werden notiert. Die wahrscheinliche Zahl der Bakterien wird aus den Ergebnissen der Keimzählung wie folgt ermittelt (Tab 1):
2.3.2 Nachweis von Pseudomonas (P.) aeruginosa
100 ml CASO-Bouillon werden mit 10 ml der vorbereiteten Probe oder mit einer 1 g oder 1 ml entsprechenden Menge des Produktes beimpft. Nach Mischen wird 18 bis 24 Stunden bei 30°C bis 35°C bebrütet. Subkulturen werden auf Cetrimid-Agar angelegt und 18 bis 72 Stunden bei 30°C bis 35°C inkubiert. Bei Abwesenheit eines mikrobiellen Wachstums entspricht das Produkt der Prüfung. Wenn Kolonien mit meist unregelmäßigem Rand und häufig granulierter Oberfläche erscheinen, die grünlich sind, meist fluoreszieren und aus gramnegativen Stäbchen bestehen wird, eine Prüfung auf Oxidase durchgeführt und geprüft, ob bei 42°C in CASO-Bouillon ein Wachstum eintritt. Zusätzlich können die Bestimmung von Wachstum unter oxidativen (das heißt unter Zugabe von Luftsauerstoff) und/oder fermentativen Bedingungen (das heißt durch Unterbinden der Luftzufuhr = O/F-Test) sowie biochemische Bestätigungsreaktionen durchgeführt werden (api-Systeme). Das Produkt entspricht der Prüfung, wenn keine derartigen Kulturen beobachtet werden oder wenn die biochemischen Bestätigungsreaktionen negativ sind.
2.3.3 Nachweis von Staphylococcus (S.) aureus
Eine Anreicherungskultur wird, wie bei P. aeruginosa angegeben, angelegt. Subkulturen werden auf Mannitol-Salz-Agar, Baird-Parker- Agar oder Kranep-Agar angelegt. 18 bis 72 Stunden wird bei 30°C bis 35°C bebrütet. Bei Abwesenheit eines mikrobiellen Wachstums entspricht das Produkt der Prüfung. Auf dem Baird-Parker-Agar kann das Erscheinen von schwarzen Kolonien, die oft von einer klaren Zone umgeben sind und aus grampositiven Kokken bestehen, die Anwesenheit von S. aureus anzeigen. Dies kann an Katalase-positiven Kokken bestätigt werden zum Beispiel durch die Koagulase- und Desoxyribonukleasereaktion. Auf dem Kranep-Agar sehen die Kulturen wie folgt aus: weiß-gelbliche Kolonien mit 1-3 mm Durchmesser und häufig klarem Hof (Eigelbreaktion), glatter Rand, konvex, glatt, glänzend. Das Produkt entspricht der Prüfung, wenn die beschriebenen Kolonien nicht beobachtet werden oder die Bestätigungsreaktionen negativ sind.
Bevor das zu untersuchende Arzneimittel in der Prüfung eingesetzt werden kann, muss eine Validierungsuntersuchung darüber Aufschluss geben, inwieweit bestimmte Störfaktoren bei der Prüfung eine Rolle spielen. So könnten beispielsweise Hemmstoffe oder Matrixeffekte den Nachweis von Mikroorganismen mehr oder weniger beeinflussen. Zur Feststellung derartiger Effekte wird das zu untersuchende Produkt in An- und Abwesenheit von den jeweils nachzuweisenden Mikroorganismen untersucht. Im Einzelnen können die Störfaktoren entweder durch Verdünnung des Produktes oder den Zusatz von Enthemmern eliminiert werden. Aufgrund der ermittelten Validierungsdaten wurde die alkalifreie Waschlotion in einer Verdünnung von 1:100 mit einem Zusatz von 1 % Tween in den entsprechenden Verdünnungsmedien untersucht.
3. Ergebnisse
In eigenen Untersuchungen konnten in 19 aktuell im Gebrauch befindlichen Chargen alkalifreier Waschlotionen keine spezifizierten Mikroorganismen nachgewiesen werden. Die Zählung lebensfähiger aerober Mikroorganismen ergab keine Grenzwertüberschreitungen. Die Keimzahl aerob mesophiler Mikroorganismen lag in allen Fällen unterhalb der Nachweisgrenze, das heißt, <1,0x101 Kolonie bildenden Einheiten.
4. Diskussion und Schlussfolgerungen
Die Verwendung von Duschgel führt in der Regel nicht zu einem längeren Kontakt mit der Hautoberfläche, da es wieder abgewaschen wird. Trotzdem kann ein Kontakt mit Schleimhäuten und vorhandenen Wunden als mögliche Eintrittspforte für eine Infektion nicht vermieden werden. Darüber hinaus ist davon auszugehen, dass Duschgele auch von Personen benutzt werden, die aufgrund ihrer gesundheitlichen Situation als Risikogruppe anzusehen sind.
Die Laborabteilungen II der Zentralen Institute des Sanitätsdienstes der Bundeswehr sind in der Lage, jederzeit spezifische Untersuchungsanforderungen im Rahmen der Arzneimittelsicherheit zu übernehmen. Die Etablierung adäquater mikrobiologischen Untersuchungsverfahren in den Untersuchungseinrichtungen der Bundeswehr stellt einen wesentlichen Baustein im Zusammenhang mit der Arzneimittelsicherheit und dem Verbraucherschutz für die Soldaten der Bundeswehr dar. Die Herstellungspraxis in den Bundeswehrapotheken ist derart optimiert, dass es im Fall der Herstellung von alkalifreier Waschlotion zu keiner Verkeimung der Produkte kommt. Auch werden im Rahmen der Qualitätskontrolle bereits im Vorfeld mikrobiologische Untersuchungen der Ausgangsprodukte durch die jeweiligen Kontrollleiter angefordert, damit mögliche Risiken im Verlauf der späteren Herstellung bereits im Vorfeld ausgeschlossen werden können.
Literatur:
- anonym: Keime in Duschgel. Stellungnahme Nr. 036/2009 des BfR vom 13. Juli 2009.
- Anelich, LE: Survey of micro-organisms associated with spoilage of cosmetic creams manufactured in South Africa. Int J Cosm Sci. 1996; 18: 25-40.
- Brenner, DJ, Richard C, Steigerwalt, AG, Asbury, A, Mandel, A: Enterobacter gergoviae sp. nov.: a New Species of Enterobacteriaceae Found in Clinical Specimen and the Environment. Int J Syst Bacteriol 1980; 30: 1-6.
- Campana, R, Scesa, C, Vittoria, E, Baffone, W: Microbiological study of cosmetic products during their use by consumers: health risks and efficacy of preservative systems. Lett Appl Microbiol. 2006; 43: 301-306.
- Cantón, R, Oliver, A, Coque, TM, Varela, M C, Pérez-Díaz, J, Baquero, F: Epidemiology of Extended-Spectrum ß–Lactamase-Producing Enterobacter Isolates in a Spanish Hospital during a 12-Year Period. J Clin Microbiol. 2002; 40: 1237-1243.
- Chen, K-J, Yang, K-J, Sun, C-C, Yeung, L: Traumatic endolphtalmitis caused by Enterococcus raffinosus and Enterobacter gergoviae. J Med Microbiol. 2009; 58: 526-528.
- Cheng, Y, Chen, M: Extended-Spectrum ß-Lactamases in Clincal Isotates of Enterobacter gergoviae and Escherichia coli in China. Antimicrob Agents and Chemother. 1994; 38: 2838-2842.
- Davin-Regli, A, Chollet, R, J, Chevalier, J, Lepine, F, Pagès, JM: Enterobacter gergoviae and the prevalence of efflux in parabens resistance. J Antimicrob Chemother. 2006; 57: 757-760.
- Enterobacter infections, emedicine, emedicine.medscape.com.
- Ganeswire, R, Thong, KL, Puthucheary, D: Nosocomial outbreak of Enterobacter gergoviae bacteriaemia in a neonatal intensive care unit. J Hosp Infect. 2003; 53: 292-296.
- Lundov, MD, Zachariae, C: Recalls of microbiologically contaminated cosmetics in EU from 2005 to May 2008. Int J Cosm Sci. 2008; 30: 471-474.
- Okeke, IN, Lamikanra, A: Bacteriological quality of skin-moisturizing creams and lotions distributed in a tropical country. J Appl Microbiol, 2001; 91: 922-928. 13. Sanders, WE, Sanders, CC: Enterobacter spp.: Pathogens Poised to Flourish at the Turn of the Century. Clin Microbiol Rev. 1997; 10: 220-241.
Datum: 06.06.2011
Quelle: Wehrmedizinische Monatsschrift 2011/4