Aus der Forschung in die Praxis
Der Einsatz bioabsorbierbarer, magnesium-basierter Implantate in der Knochen-Chirurgie
Eine große Anzahl der jährlich über eine Million eingebrachten Implantate in der orthopädischen Chirurgie werden wieder entfernt, weil sie zu unerwünschten Reaktionen führen. Der Re-Eingriff ist stets mit potentiellen Risiken verbunden: Es können Gefäß- oder Nervenschädigungen auftreten, ebenso stellen Narkose und eine mögliche Infektion potentielle Gefahren dar, abgesehen von den auftretenden Schmerzen beim Patienten und den (durchschnittlich bis zu drei) Tagen der Abwesenheit vom Arbeitsplatz. Allein die Kosten für diese Materialentfernungen werden auf mehr als 500 Mio. € in Deutschland geschätzt. Neuartige Implantate machen einen Zweiteingriff obsolet.
Als nicht resorbierbare metallische Osteosynthesematerialien werden hauptsächlich Titan und Stahl eingesetzt. Gegenüber Knochen weisen diese Metalle eine sehr viel höhere Steifigkeit auf, was eine Belastungsabschirmung (Stress Shielding) bewirken kann. Durch die Inaktivierung des Knochenstoffwechsels in der Frakturzone wird das Remodeling behindert, was in einer Osteoporose resultieren kann. Permanente Implantate aus Titan oder Stahl erzeugen zudem Artefakte in der radiologischen Bildgebung, insbesondere im CT. Für die MRT sind sie gänzlich ungeeignet. Generell können Implantate im Körper Fremdkörperreaktionen und Allergien hervorrufen.
In der heutigen Zeit haben sich als resorbierbare Implantatmaterialien hauptsächlich Polymere (PLA/PGA) in der operativen Medizin etabliert. Doch ist deren Einsatz bei einer Vielzahl von Patienten mit Fremdkörperreaktionen verbunden, was ihre gute Verträglichkeit in Frage stellt. Die erzielbaren mechanischen Kennwerte erlauben den Einsatz bioresorbierbarer Polymere lediglich beim Auftreten geringer Zug-, Druck- und Scherbelastungen, wodurch das mögliche Indikationsspektrum stark eingeschränkt ist. Insbesondere in (teil-)belasteten Bereichen bei Osteosynthesen kommen Polymer-Implantate deshalb kaum zum Einsatz. Derzeitige Polymere zeichnen sich zwar durch eine Verwendbarkeit in CT und MRT aus, ihre Darstellbarkeit ist allerdings limitiert.
In diesem Zusammenhang konnte die grundsätzliche mechanische und korrosive Eignung einer Vielzahl von Legierungen für Implantatanwendungen nachgewiesen werden. Insbesondere konnte dabei auch die sehr gute Eignung Seltener Erden-haltiger Legierungen aufgezeigt werden. Die außerordentlich gute Biokompatibilitätseignung des Magnesiums resultiert insbesondere auch aus dem vergleichsweise hohen täglichen Bedarf des Menschen an Magnesium. Die empfohlene tägliche Zufuhr liegt zwischen 375 mg und 500 mg je nach Alter und Geschlecht. Innerhalb des Knochens liegt das Magnesium nicht fest gebunden vor, was es rasch verfügbar macht. Auf dieser Basis kann ein Magnesiumimplantat, das im Knochen degradiert auch als Quelle der essentiellen Magnesiumionen angesehen werden.
Im interdisziplinären Sonderforschungsbereich (SFB 599) an der Medizinischen Hochschule Hannover wurde zwölf Jahre lang an neuen Legierungen und Verfahren für resorbierbare Mg-Implantate gearbeitet. Hier gewonnene und publizierte Erkenntnisse sind u. a. auch in die Entwicklung eines magnesium-basierten Implantatmaterials am Materials Science and Engineering Werkstoffzentrum Clausthal (MSE) eingeflossen. Seit 2008 wurde hier zunächst eine Legierung entwickelt, die die Basis für den weltweit ersten metallisch-bioabsorbierbaren Implantat-Werkstoff in der orthopädischen Chirurgie darstellt: MAGNEZIX®. Das erste aus diesem Werkstoff hergestellte und seit Frühjahr 2013 CE-zugelassene Implantat ist die MAGNEZIX® CS (Compression Screw) 3.2 – eine kanülierte Frakturkompressionsschraube (Herbert-Schraube) mit einem Gewicht von zirka 150 Milligramm (Länge = 20 mm), einem Schaftdurchmesser von 2,4 Millimetern (Kanal: Ø 1,3 mm) und selbstschneidenden Gewinden. Dieses Implantat ist in Längen zwischen zehn und 40 Millimetern (in 2-mm-Schritten) erhältlich. Inzwischen sind drei Implantat-Dimensionen im Markt: MAGNEZIX® CS mit den Nenndurchmessern 2,0/2,7 und 3,2 Millimeter.
Diverse Forschungslegierungen aus Magnesium schienen aus verschiedenen Gründen nicht für den Einsatz am Menschen geeignet. Insbesondere die beim Prozess der Magnesium-Degradation entstehende Bildung von Korrosionsprodukten schien ein kritischer Faktor zu sein. Bei der Degradation von Magnesium bildet sich initial eine Magnesiumhydroxidschicht auf der Implantatoberfläche aus und gasförmiger Wasserstoff wird abgeschieden. Insbesondere die Wasserstoffgas-Bildung (H2) konnte bei MAGNEZIX® durch einen optimierten Herstellungsprozess und eine gezielte Auslegung der Legierungszusammensetzung auf ein Minimum reduziert werden. Der Werkstoff MAGNEZIX® zeigt eine exzellente Biokompatibilität, besitzt eine starke osteogene Potenz und wirkt über den Magnesiumabbau anti-infektiös (Verschiebung des pH-Wertes ins alkalische Milieu).
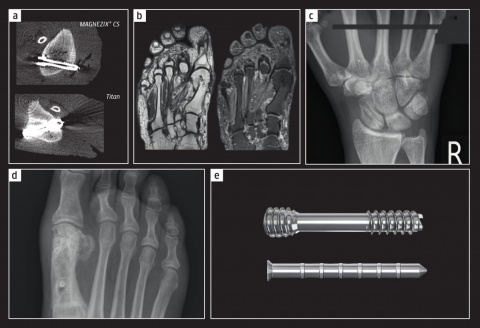
Das Material aus dem Legierungssystem MgYREZr nach DIN EN 1753 hat einen Magnesium-Anteil von über 90 Prozent, eine Partikelgröße von unter 10 µm und wird in einem sogenannten pulvermetallurgischen Prozess hergestellt, womit eine Zugfestigkeit erreicht wird, die deutlich höher liegt als die von Polymeren (PLA/PGA), etwas über der des kortikalem Knochens, jedoch unter der von Titan (Abb. 2). Diese Konstellation wirkt dem „Stress Shielding Effect“ entgegen, der zur Osteopenie führen kann. Verglichen mit einer herkömmlichen Titanschraube (TiCP/TAV, Schaftdurchmesser 2,0 mm), weist z. B. die MAGNEZIX® CS 3.2 durch das magnesiumspezifische Design nahezu identische mechanische Stabilitätswerte (Biegung, Zug, Torsion) auf.
Die osteogene Potenz von MAGNEZIX® zeigt sich bei in vitro-Versuchen zum einen durch eine hohe Vitalität humaner Osteoblasten und durch deren Stimulation in Proliferationstests. In histologischen Knochenschliffen mit verschiedenen Färbetechniken wurde sowohl die Degradation der Schraube als auch die Knochenneubildung (Osteoid) im ehemaligen Implantatlager nachgewiesen (Tierstudie am Kaninchen). Der Abbau der Schraube erfolgt auf dem Wege der Korrosion und nicht, wie bei Polymeren, im Wesentlichen über den Weg der Hydrolyse. Negative implantat-assoziierte Effekte wie Serombildungen oder Wundheilungsstörungen sowie zurückbleibende Hohlräume im Knochen wurden weder histologisch im Tier, noch radiologisch im Menschen beobachtet.
Für die Zulassung in Europa (CE-Label) wurde, neben Grundlagenforschung durch in vitro-Versuche und Tierstudien, eine klinische prospektiv-randomisierte und kontrollierte Zulassungsstudie an der Orthopädischen Klinik der Medizinischen Hochschule Hannover im Annastift durchgeführt (Windhagen et al., 2013). In dieser Studie konnte die Nicht-Unterlegenheit der MAGNEZIX®-Schrauben gegenüber einem herkömmlichen Titanimplantat bei Hallux valgus-Operationen (Chevron-Osteotomie) gezeigt werden. In einer weiteren Studie (Plaass et al., 2015) konnte eine sehr hohe Zufriedenheit bei mit MAGNEZIX®-Schrauben versorgten Patienten nachgewiesen werden. Seit der Markteinführung wurden mittlerweile in über 20 Ländern mehr als 17 000 Implantate in Verkehr gebracht.
Klinisch wurden bislang in fast allen Fällen (weit über 7 000) positive Resultate erzielt. Umfangreiche Vigilanzdaten zeigen in nahezu allen Fällen eine regelhafte knöcherne Ausheilung der nach Osteotomie oder Fraktur verschraubten Knochen. Bisherige Schwierigkeiten im Umgang mit dem Implantat oder unerwünschte klinische Ergebnisse waren vorwiegend auf eine unscharfe Indikationsstellung oder eine mangelhafte OP-Technik zurückzuführen (Seitz et al., 2015). In manchen Fällen treten im Röntgenbild mehr oder minder stark ausgeprägte Aufhellungszonen um das Implantat herum auf. Dieses Phänomen ist dem Abbau der Implantate durch Degradation geschuldet (Knochenumbauzone). Die MRT-Befunde nach drei Jahren Follow up zeigen eindeutig den Umbau der Schraube in kortikalis-ähnliches, körpereigenes Knochengewebe (Abb. 1b). Auch wenn die klassische Herbert-Schraube ihre primäre Indikation bei der Skaphoid-Fraktur hat (Abb. 1c), so ist das weltweit erste metallische bioabsorbierbare Implantat, die MAGNEZIX® Compression Screw (CS), bereits in den verschiedensten Körperregionen eingesetzt worden, u.a. bei den folgenden Indikationen: Hallux valgus (Abb. 1d), Klaviculafraktur, proximale Radiusfraktur (Radiusköpfchen), Unterarmfraktur, distale Radiusfraktur, Metakarpalefrakturen, Azetabulumfrakturen, Hüftkopffrakturen (Pipken), distale Femurfraktur, Patellafrakturen, Innen- und Außenknöchelfrakturen u. a. m.
Inzwischen haben sog. Knochen-Pins aus MAGNEZIX® die Zulassung für den CE-Raum erhalten, mit denen spezifische traumatologische Indikationen alternativ bedient werden können. Diese sind in 69 Größen verfügbar und – selbst in degradiertem Zustand (288 Stunden; in vitro) - um ein Vielfaches stabiler als Polymer-Pins vergleichbarer oder größerer Dimensionen (ohne vorherige Konditionierung). In Planung sind weitere Implantate, insbesondere Kortikalis-Schrauben und Interferenzschrauben für die Kreuzbandchirurgie.
Für den Einsatz im Sanitätsdienst werden magnesium-basierte Implantate (Abb. 1e) eine sinnvolle Alternative zum Schrauben aus Titan und Pins aus Polymeren darstellen, da sie neben den beschriebenen Eigenschaften, insbesondere für den Feldeinsatz den Vorteil bieten, als „ready to use“-Produkt geliefert zu werden, d. h. in steriler Verpackung. Die Implantate sind bis zu fünf Jahre haltbar. Die zugehörigen Instrumente sind platzsparend in kleinen Sieben sortiert.
Datum: 29.06.2016
Quelle: Wehrmedizin und Wehrpharmazie 2016/2