EINSATZ ANTIINFEKTIVER BESCHICHTUNGSLÖSUNGEN IN DER GELENKCHIRURGIE
Implantat-assoziierte Infektionen sind ein ernstzunehmendes Risiko in der Medizin. Ursache dafür ist die hohe Affinität von Implantaten, als Fremdkörper von Keimen in kürzester Zeit besiedelt zu werden.
Infektionen werden in bis zu 80% der Fälle perioperativ, also in erster Linie durch den chirurgischen Eingriff, gesetzt (1, 2). Dabei gelangen Keime während des chirurgischen Eingriffs ins operative Umfeld, besiedeln rasch die Implantatoberfläche und verursachen in der Folge eine Infektion. Implantatoberflächen können auch durch hämatogen streuende Keime kolonisiert werden. Post operativ dienen Implantate als Rückzugsort für Keime, von denen Rezidive ausgehen können. Implantat-assoziierte Infektionen können bereits durch niedrige Keimzahlen hervorgerufen werden (3). Bevorzugt handelt es sich dabei um Gram-positive Bakterien, wie Staphylococcus aureus und Staphylococcus epidermidis. Gram-negative Bakterien, wie Pseudomonas aeruginosa oder Acinetobacter baumanii, gewinnen mittlerweile ebenso an Bedeutung.
Infektionen in der Endoprothetik
Besonders in der Endoprothetik sind Implantat- assoziierte Infektionen schwerwiegende und daher gefürchtete Komplikationen. Hier sind Bakterien in der Lage, schnell die Implantatoberfläche zu besiedeln und einen Biofilm zu bilden. Durch solche bakteriellen Biofilme können sowohl Früh- als auch Spätinfekte entstehen. Insbesondere bei Spätinfekten bleiben die auf der Implantatoberfläche anhaftenden Keime im Biofilm lange inaktiv, so dass klassische Infektionszeichen nicht detektiert werden können. In der Folge werden diese sog. sessilen Bakterien im Biofilm vom körpereigenen Immunsystem nicht erkannt. Auch Antibiotika sind in diesem StaFettsäudium nahezu wirkungslos. Erst wenn einige Bakterien den Biofilm verlassen und in eine freibewegliche sog. planktonische Form übergehen, kann die Infektion klinisch manifest werden. Ziel umfangreicher Forschungen ist es daher, geeignete Maßnahmen zu entwickeln, die bereits perioperativ den Schutz der Implantatoberfläche vor einer Besiedelung von Bakterien ermöglichen. Eine Implantatbeschichtung zur lokalen Freisetzung von antimikrobiellen Substanzen im Implantat - umfeld erscheint daher sinnvoll, um prophylaktisch einer Kolonisation der Prothese durch Keime mit einer einhergehenden Biofilmbildung nachhaltig entgegen zu wirken.
Infektionsprohphylaxe in der zementierten Endoprothetik
In der zementierten Endoprothetik können PMMA-Knochenzemente als lokale Wirkstoffträger eingesetzt werden. Durch die lokale Antibiotikafreisetzung aus der Zementmatrix werden hohe lokale Wirkspiegel im Implantatlager erreicht, die die Besiedelung der Implantatoberfläche durch Bakterien unterbinden und so prophylaktisch einer Infektion bzw. Reinfektion entgegen wirken. Das bakterizide Antibiotikum Gentamicin aus der Gruppe der Aminoglykosid-Antibiotika findet aufgrund seines breiten Wirkspektrums seit Jahren erfolgreich Verwendung in PMMAKnochenzementen. In der Primärendoprothetik haben sich daher Knochenzemente mit dem Zusatz von Gentamicin (z. B. PALACOS® R+G) seit Jahrzehnten bewährt. Bei Revisionseingriffen empfiehlt sich insbesondere die Verwendung von Knochenzementen mit Antibiotikakombinationen (z. B. COPAL® G+C, COPAL® G+V). Metastudien in den USA mit einem großen Patientenkollektiv bestätigen eine nachhaltige Senkung des Infektionsrisikos von Implantaten bei der Verwendung von Antibiotika zur Prophylaxe am Beispiel von antibiotikahaltigen Knochenzementen (4).
Lokale Wirkstoffplatzierung in der zementfreien Endoprothetik
Die klinisch bewährte Verwendung antibiotikahaltiger PMMA-Zemente zur Reduzierung des Infektionsrisikos in der zementierten Primärendoprothetik legt nahe, das Konzept des Infektionsschutzes durch lokale Antibiotika auch auf Primäreingriffe mit zementfreien Prothesen zu übertragen. Während bei der zementierten Prothesenverankerung der PMMA-Zement als Träger für Antibiotika dient, kann bei zementfreien Prothesen nur die Prothese selbst als Wirkstoffträger fungieren. Von daher scheint es sinnvoll, die antiinfektiven Wirkstoffe direkt auf die Implantatoberfläche aufzubringen.
Herausforderung: Beschichtung mit antiinfektiven Substanzen
In der zementierten Endoprothetik wird das Gentamicin dem PMMA-Zement in Form von wasserlöslichem Gentamicinsulfat (GS) zugefügt. In dem Fall erweisen sich die hydrophilen Eigenschaften des Gentamicinsulfats als vorteilhaft, da das Gentamicin durch Diffusion aus der Zementmatrix ins Implantatumfeld gelangt und eine hohe Freisetzungsrate besonders in den ersten Tagen postoperativ ermöglicht werden kann. Auf Metalloberflächen zeigt das Gentamicinsulfat – wie viele andere antiinfektiven Substanzen auch – allerdings keine ausgeprägte Haftung. Dies hat zur Folge, dass die meisten Antiinfektiva zur Beschichtung metallischer Prothesen wenig geeignet sind, da die Wirkstoffe nur über einen unzureichenden Zeitraum von einigen Minuten im Implantatumfeld verbleiben und der Aufbau eines effektiven Wirkspiegels unterbleibt. Ideal wäre stattdessen ein antiinfektiver postoperativer Schutz gleichsam der erzielbaren Schutzwirkung im Rahmen der Verwendung antibiotikahaltiger PMMA-Zemente.
Fettsäuresalze zur Beschichtung von Implantaten
Bei zementfreien Titanprothesen kann eine Beschichtung über eine neuartige gering wasserlösliche Form von Antiinfektiva erfolgen (5), die die klinischen Erfordernisse an einen sicheren Infektionsschutz erfüllen. Für die Beschichtung ze ment freier Implantate mit antiinfektiven Wirkstoffen kann das Gentamicinsulfat durch Umsalzung in ein gering lösliches Gentamicinfettsäuresalz überführt werden. Gentamicinfettsäuresalze sind wachsartige Feststoffe, die in dünnen Schichten eine ausgeprägte Haftwirkung auf unterschiedlichsten Oberflächen besitzen. Die Wirksamkeit des Gentamicins bleibt bei dieser Überführung unverändert (6). Die Fettsäuresalze sind nicht toxisch und können im humanen Organismus abgebaut werden. Das Gentamicin wird aus den Fettsäurekomplexen freigesetzt und in das Implantatumfeld abgegeben.
Gentamicinpalmitat in der Endoprothetik
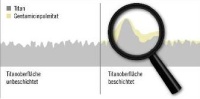
Als besonders interessant für eine antiinfektive Beschichtung von metallischen Implantaten hat sich das Gentamicinpalmitat (nachfolgend teilweise als „GP“ aufgeführt) ge - zeigt. Dieses neuartige Gentamicinsalz ist ein farbloser bis gelblicher, wachsartiger Feststoff, der in organischen Lösungsmitteln löslich ist (6). Bei der Beschichtung von rauen Titan-Implantaten mit dünnen Schichten aus Gentamicinpalmitat bleibt die ursprüngliche Rauhigkeit der Prothesen oberfläche weitestgehend erhalten, da sich die GP-Beschichtung in den Vertiefungen der rauen Titanoberfläche befindet (7) (Abb. 1). Dadurch wird die Primärstabilität der implantierten beschichteten Endoprothesen nicht negativ beeinflusst und eine weitere Verankerung im Knochen kann ungehindert erfolgen. Gentamicinpalmitat kann als Beschichtungslösung beispielsweise durch ein Sprühverfahren auf die Oberfläche von zementfreien Endoprothesen aufgebracht werden. Die Dosierung kann dabei leicht eingestellt werden. Eine Sterilisation der mit GP be schich teten zementfreien Endoprothesen ist – wie die unbeschichteten Implantate auch - durch Gammabestrahlung leicht möglich. Heraeus Medical GmbH hat auf diesen Grund lagen AntibiotiCoat®+G entwickelt.
Schutzwirkung vergleichbar zu antibiotikabeladenem PMMAZement
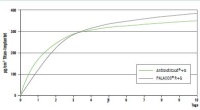
Unter in vitro-Bedingungen erfolgt die Gentamicinfreisetzung aus dem Gentamicinpalmitat in Abhängigkeit von den VersuchsbeSchutzwirkung vergleichbar zu antibiotikabeladenem PMMAZement Unter in vitro-Bedingungen erfolgt die Gentamicinfreisetzung aus dem Gentamicinpalmitat in Abhängigkeit von den Versuchsbedingungen im Zeitraum von 10 - 14 Tagen (8, 9). Um der Biofilmbildung auf Implantaten, z. B. durch Staphylococcus aureus, durch eine Beschichtung mit lokalen Antibiotika auf der Prothese gezielt vorzubeugen, ist die Höhe der Wirkstoffkonzentration am Implantationsort in nerhalb der ersten 48 Stunden nach Implantation maßgeblich für die Effizienz des Infektionsschutzes. Versuche mit GPbeschichteten sandgestrahlten Titanscheiben im Vergleich zur Gentamicinfreisetzung aus PALACOS® R+G zeigen eine vergleichbare Wirkstofffreisetzung. Wie auch bei PALACOS® R+G erfolgt bei der GP-Beschichtung zu - nächst eine initiativ hohe und danach kontinuierliche Freisetzung des Gentamicins ins Gewebe (Abb. 2). Ein zu erwartendes identisches Verhalten von GP und gentamicinhaltigem PMMA-Zement bezogen auf die antibakterielle Wirksamkeit - z. B. gegen einen biofilmbildenden Staphylococcus epidermidis - konnte im Proliferationstest (DIN ISO EN 17025, Quality Labs BT GmbH) bestätigt werden. Ebenso belegen Hemmhofversuche die analoge Wirkstofffreisetzung und infolgedessen gleichsame antibakterielle Wirkung (10). Sowohl bei GP-beschichteten Titanplättchen als auch bei gentamicinhaltigem PMMA-Zement bildet sich durch Keimabtötung ein Hemmhof aus. Im Vergleich dazu werden unbeschichtete TitanVersuchsbeplättchen von Keimen kolonisiert; die Bildung eines Hemmhofes bleibt aus (Abb. 3).
Versuche am Tiermodell (Kaninchen) zur Osteo integration von GP-beschichteten Titan- Stiften zeigten, dass die Osteointegration von beschichteten und unbeschichteten Titanstiften vergleichbar ist. Zudem konnten keine Osteolysen und keine Entzündungsreaktionen beobachtet werden. Das für die Beschichtung verwendete Gentamicinpalmitat erwies sich bei allen vorgeschriebenen Tests als biokompatibel nach ISO 10993 (8).
Reduzierung des Infektionsrisikos bei zementfreien Primäreingriffen möglich
Neuartige Beschichtungen mit Antibiotika- Fettsäurekomplexen sind geeignet für die antiinfektive Ausrüstung zementfreier Prothesen. Eine Gentamicinpalmitatbeschichtung auf Titanprothesen zeigt vergleichbare antiinfektive Eigenschaften wie gentamicinhaltiger PALACOS® R+G. Eine GP-Beschichtung auf Titan für zementfreie Primärendoprothesen kann daher ebenso zur Infektionsprophylaxe eingesetzt werden wie genta mi cin hal - tiger Knochenzement. Heraeus Medical bietet Implantatherstellern Antibioti Coat®+G als exklusive Beschichtungslösungen mit Gentamicinpalmitat zur industriellen Beschichtung von Implantaten im Vorfeld der OP an. Mit einem patentierten innovativen Ready-to-use Coating Device kann erstmals eine effektive antibiotische Beschichtung während der OP auf die Prothese aufgetragen werden. Antimikrobiell beschichtete Implantate können so in Zukunft den Patienten einen nachhaltigen Nutzen bringen und durch Reduktion der septischen Revisionen zur Kos tensenkung beitragen.
Datum: 27.06.2013
Quelle: Wehrmedizin und Wehrpharmazie 2013/2