VORBEUGENDER GESUNDHEITSSCHUTZ IM EINSATZ MIT CHEMISCHER HIGH-TECH-ANALYTIK
Frisches Obst und Gemüse sind auch im Einsatz Bestandteil einer ausgewogenen Ernährung, die weitgehend frei von Rückständen, Kontaminanten und Schadstoffen sein soll. Dies zu prüfen und zu bewerten ist Aufgabe der Lebensmittelchemie unter besonderer Betrachtung weltweit eingesetzter Pflanzenschutz- und -behandlungsmittel. Aktuelle Untersuchungsergebnisse amtlicher und privater Verbraucherschutzeinrichtungen zeigen, dass der Einsatz von Pestiziden und Fungiziden nach wie vor zu Überschreitungen der zulässigen Höchstwerte führt.
Greenpeace fand im Herbst 2005 auffällig hohe Rückstandskonzentrationen in Tafeltrauben, das Chemische Untersuchungsamt in Stuttgart berichtete über 55 unterschiedliche Wirkstoffe in Erdbeeren der Ernte 2005. Gemüsepaprika aus ver-schiedenen Herkunftsländern wurde in den letzten Jahren darüber hinaus als mehrfach belastet identifiziert. In 88 % der untersuchten Proben aus konventionellem Anbau aus Spanien, der Türkei und Israel wurden im Mittel 7,9 Wirkstoffe gleichzeitig gefunden. Ge-genstand derzeitiger Diskussionen ist die Bewertung von sog. Mehrfachrückständen; der Stellenwert von Mehrfachrückständen und Summengrenzwerten wird aktuell durch das Bundesinstitut für Risikobewertung (BfR) sowie die US-EPA (environmental protection agency) unter toxikologischer Betrachtung diskutiert, um Verfahren zur Abschätzung des kumulativen Risikos zu erarbeiten. Betrachtet man allein den in Deutschland für solche komplexen Rückstandsuntersuchungen notwendigen materiellen und personellen Aufwand, so wird deutlich, dass dies trotz des Einsatzes hoch modern ausgestatteter Laborcontainer eine Herausforderung für den Analytiker bleibt. Die Container enthalten prinzipiell die für die analytischen Fragestel-lungen notwendigen Analysengeräte, doch fehlt es an Platz und Zeit, um mit den derzeit verfügbaren amtlichen Untersuchungsmethoden diese wichtigen Fragestellungen vor Ort bearbeiten zu können. Deswegen ist es notwendig, mit schnellen und effizienten Multimethoden eine möglichst große Anzahl an relevanten Rückständen zu erfassen. Ziel ist es, derartige Methoden im Zentralen Institut des Sanitätsdienstes in München zu entwickeln, und diese anschließend in die lebensmittelchemischen Laborcontainer zu transferieren.
Strategien der Methodenentwicklung / Methodenoptimierung
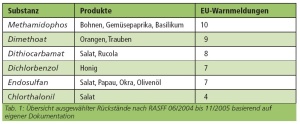
Die Europäische Union (EU) stellt mit dem Rapid Alert System for Food and Feed (RASFF) eine schnelle und transparente Informationsübermittlung bei auffälligen Rückstandshöchstmen-genüberschreitungen an die Überwachungsbehörden sicher. Seit dem Jahr 2004 werden diese Meldungen in unserer Laborgruppe nach relevanten Kontaminanten und Rückständen ausgewer-tet und dokumentiert. Tab 1. gibt einen Überblick über die häufigsten Warnmeldungen von Rückständen seit Juni 2004. (Tab. 1) Auffallend häufig waren hierbei Beanstandungen bei Salat, Gemüsepaprika, Tafeltrauben und Honig. Darüber hinaus werden durch die EU regelmäßig Monitoringprogramme zur Überwa-chung von Rückständen in Lebensmitteln initiiert. Das aktuelle Überwachungsprogramm enthält 55 Rückstände, die in den Jahren 2005 bis 2007 untersucht werden sollen. Während die Belastungssituation seitens der EU zunehmend transparenter wird, fehlen ver-gleichbare Daten für unsere Haupteinsatzgebiete. Ungeklärt ist die detaillierte Rückstandssituati-on, die wir auf dem Balkan, in Afghanistan, Usbekistan und Pakistan im Zusammenhang mit Rückständen und Kontaminanten zu erwarten haben. Lediglich durch die Food and Drug Admi-nistration (FDA) wurden erste Angaben zur weltweiten Rückstandsituation aus dem Jahr 2003 publiziert. Eine Recherche lieferte hierbei Anhaltspunkte für Pakistan (34 untersuchte Proben) sowie für Usbekistan, Bosnien, Mazedonien und Jugoslawien (< 10 untersuchte Proben pro Land). Diese dürftige Datenlage war Anlass, ab 01. Januar 2006 ein eigenes Monitoringprog-ramm für Obst und Gemüse aus den Einsatzländern am Zentralen Institut des Sanitätsdienstes der Bundeswehr in München zu etablieren. Bei der Auswahl der Analysenmethode war die Entscheidung schwieriger. In den letzten zehn Jahren wurden immer wieder Multimethoden zur Analytik von Pflanzenschutzmitteln in Le-bensmitteln publiziert, um den enormen Zeitaufwand für die Probenvorbereitung zu minimieren. Neben der klassischen Festphasenextraktion (solid phase extraktion = SPE), die bereits in der Wasseranalytik etabliert ist, kamen für uns die dispersive SPE, bei der das Sorbens direkt im Lebensmittelextrakt dispergiert wird, die Solid Phase Microextraction (SPME), bei der die Rück-stände an einer wenige µm dicken Faser gebunden werden und die Stir Bar Sorptive Extraction - Thermo Desorption (SBSE-TD), bei der die Analyten mittels Verteilungschromatographie an einem mit Polydimethylsiloxan belegten Rührfisch (stir bar) gebunden und anschließend in einem kleinen Heizblock bei ca. 250°C wieder freigesetzt werden (thermisch desorbiert), in Betracht. Wir verfolgen für die Analytanreicherung und -aufreinigung derzeit zwei Wege:
a) die von Pat Sandra etablierte Stir Bar Sorptive Extraction (SBSE) und
b) die von Michelangelo Anastassiades geprägte dispersive QuEChERS-Technik (Quick - Easy - Cheap - Effective - Rugged and Safe).
Die SBSE-TD ermöglicht die automatisierbare massenspektrometrische Untersuchung von ca. 500 organischen Verbindungen, so dass wir sukzessive ein Bild von der tatsächlichen Rück-standssituation über ein Monitoringprogramm in den Einsatzländern erhalten können. Wegen des technischen Aufwandes ist diese Methode allerdings nur in einem Institut durchführ-bar. Die QuEChERS-Technik hingegen stellt die ideale und schnelle Multimethode für den La-borcontainer dar, um die für das jeweilige Einsatzgebiet typischen bzw. weltweit am häufigsten anzutreffenden Rückstände zu analysieren. Ausgehend von den FDA-Daten erfolgte eine Aus-wahl von vorerst 70 Rückständen, die von einer Multimethode sicher quantifiziert werden müssen.
Multimethoden zur Erweiterung des Untersuchungsspektrums in den Auslandseinsätzen
1. Stir Bar Sorptive Extraction Thermo Desorption (SBSE-TD)
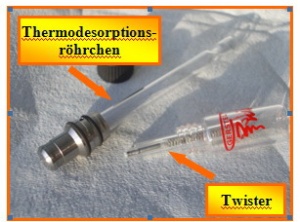
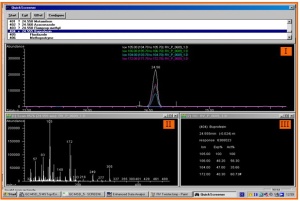
Lösemittelarme bzw. lösemittelfreie Extraktionstechniken haben sich seit der Einführung der SPME durch Pawliszyn in den 90`er Jahren als gute Alternative zur klassischen Flüssigextraktion erwiesen. Unter Verwendung mit Polydimethylsiloxan (PDMS) belegter Fasern bzw. Rührfischen (TwisterÒ, Abb. 1) konnte die Technik in Kombination mit einer thermischen oder auch flüssigen Desorption erfolgreich eingesetzt werden. Der Vorteil der SBSE gegenüber der SPME resultiert aus der größeren Menge an PDMS (ca. 25 µl) auf dem Rührfisch, so dass der Rück-stand in Abhängigkeit vom Octanol-Wasser-Quotienten (Log KOW) in bis zu 1000-fach höherer Konzentration gebunden werden kann. (Abb. 1) Nach dem Zerkleinern der Obst- / Gemüseprobe werden 5 bis 10 g Püree mit 10 ml Methanol homogenisiert. Ein Aliquot von 1 ml des so erhaltenen Rohextraktes, der ggf. kurz zentrifugiert wurde, wird im Anschluss mit 10 ml Wasser in einem kleinen Glasgefäß (Headspaceglas) ver-dünnt. Dieser Extrakt wird mit einem TwisterÒ 60 Minuten bei 1000 Umdrehungen gerührt. Die Probenvorbereitung mittels TwisterÒ kann der schematischen Darstellung in Abb. 2 entnommen werden. (Abb. 2) Der Rührfisch wird vorsichtig entnommen, mit etwas Wasser gespült, mit einem fusselfreien Trockentuch getrocknet und dann direkt für die GC-MS-Bestimmung mittels Thermodesorption eingesetzt. Bis zu 98 dieser Thermodesorptionsröhrchen incl. TwisterÒ können über den Auto-sampler MPS 2 des GC-MS-Systems in einer Sequenz abgearbeitet werden. Die neue SBSE-TD-Technik ist mit dem uns zur Verfügung stehenden GC-MS-System mit ei-nem Kaltaufgabesystem gekoppelt. Nach der thermischen Desorption der Analyten werden diese in einem 2 mm dicken Liner (Glasrohr) bei –20°C wieder niedergeschlagen und dann blitzartig mit einer Rate von 600 °C/min verdampft. (Abb. 3) Dies liefert bei der gaschromatographischen Trennung scharfe Substanzpeaks. Die Datenauf-nahme erfolgt im Massenspektrometer im Full-Scan-Modus im Massenbereich von m/z = 35 – 500 Masseneinheiten. Die Auswertung erfolgt unter Zuhilfenahme einer Retention-Time-Locking-Datenbank (RTL), die neben dem Massenspektrum auch den Retentionsindex bezogen auf eine Standardsubstanz wie z.B. Chlorpyriphosmethyl betrachtet. Hierbei wird zunächst das GC-MS-System über eine fünfmalige Injektion des Standards unter systematisch veränderlichen Bedingungen „gelockt“, so dass anschließend die Retentionszeit von Chlorpyriphosmethyl auch bei leicht schwankenden GC-Bedingungen eindeutig über die Laufzeit erkannt wird. Auf diesen Bezugspunkt werden alle anderen Pestizide über das Retentionszeitverhältnis zugeordnet. Massenspektrometrisch gilt eine unbekannte Substanz als identifiziert, wenn sowohl das Mas-senspektrum als auch die Retentionszeit übereinstimmen. Dies wird durch diese Technik ge-währleistet, so dass derzeit 572 Pestizide über die RTL-Datenbank identifiziert werden können. Neben Chlorpyriphosmethyl als zeitlichem Bezugspunkt (time reference peak) setzten wir den Proben als internen Standard 13C-DDT sowie PCB-18 bzw. PCB-185 zur Systemprüfung zu. In Abb. 4 ist beispielhaft die Zuordnung von Buprofezin aus einer Tomatenprobe in einer Kon-zentration von 108 ng/kg dargestellt: Im oberen Teil (I) ist der Substanzpeak mit 4 charakteristi-schen Massen dargestellt; links unten das Massenspektrum (II) und rechts daneben die Identifi-kationskriterien (III). (Abb. 4)
2. Die QuEChERS-Technik - erste Multimethode für den Laborcontainer
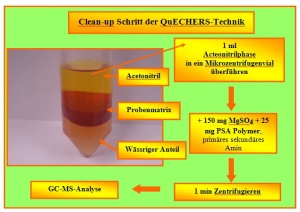
Quick- Easy - Cheap - Effective - Rugged and Safe (QuEChERS) sind die Schlagworte einer heute aus der modernen instrumentellen Pestizidanalytik nicht mehr wegzudenkenden Untersu-chungstechnik. Die von Anastassiades et al. im Jahr 2003 publizierte Methode war für uns die Grundlage zur Validierung der ersten Schnellmethode, die auch im Lebensmittelchemischen Laborcontainer zur effizienten Analytik von Pestizidrückständen eingesetzt werden kann. Die Probenvorbereitungstechnik basiert auf der dispersiven Festphasenextraktion bei der das Sorbens im Extrakt direkt verteilt und durch Zentrifugation wieder entfernt wird. Bei der Imple-mentierung der Technik haben wir als Probenmatrix Tomatenmark ausgewählt. 5 bis 10 g fein zerkleinertes Probenmaterial wird mit 10 ml Acetonitril 1 Minute in einem Zentrifugenglas ho-mogenisiert. Anschließend werden 4 g Magnesiumsulfat und 1 g Kochsalz zugesetzt, erneut ho-mogenisiert und 5 Minuten zentrifugiert. Im zweiten Aufarbeitungsschritt – dem Clean-Up – erfolgt eine Aufreinigung des Acetonitril-Überstandes mit einem speziellen Sorbens: PSA = pri-märes sekundäres Amin. Das PSA entfernt organische Säuren und Zucker und ermöglicht erst eine vernünftige gaschromatographische Untersuchung des so geklärten Acetonitril-Extraktes. Abb. 5 zeigt eine Übersicht zu den einzelnen Verfahrensschritten des Clean-Ups.
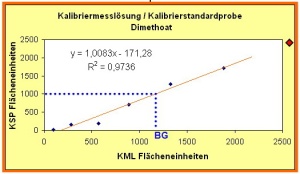
Nach der Aufreinigung kann der i.a. klare Extrakt direkt zur GC-MS-Bestimmung eingesetzt werden. Die QuEChERs-Technik wurde an unserem GC-MS-System mittels „Single Ion Moni-toring (SIM = Einzelionenmessung)“ für vorerst 70 ausgewählte Pestizide validiert und routine-mäßig eingeführt. Da die QuEChERs-Technik nicht wie die SBSE zu einer Aufkonzentration der Pestizidrückstände führt, war es nur mit einer SIM-Methode möglich, die notwendige Nachweis-empfindlichkeit zu erzielen. Als interner Standard wurde wie bei der SBSE-Methode 13C-DDT und PCB-18 bzw. PCB-185 eingesetzt. Die Quantifizierung der Rückstände und Kontaminanten erfolgt über Standardmischungen zu je 20 bis 30 Pestiziden. Unter der Voraussetzung, dass in den Zentralen Instituten des Sanitätsdienstes („Home Base“) ein Bild von der Rückstandssituati-on des Einsatzlandes, z.B. unter Einsatz der SBSE, entwickelt wurde, ist die Auswahl der 20 bis 30 bedeutendsten Pestizide für das Einsatzgebiet möglich und auch weniger geübtes Personal kann eine sichere Identifikation der Substanzen im Containerlabor realisieren. Als Beispiel ist abschließend das Ergebnis der Validierung der Methode für Dimethoat, eines Carbaminsäureesters, dargestellt. Die Abb. 6 zeigt die Gegenüberstellung der Peakflächen aus einer Standardlösung (Kalibriermesslösung) im Vergleich zu einer Kalibrierstandardprobe (do-tierte Probe) mit identischen Konzentrationen von 12,5 bis 200 ng/ml. Dies entspricht einer Kon-zentration von 0,025 bis 0,4 mg/kg in der realen Probe. Die Gerade weist eine hohe Korrelation aller erhaltenen Datenpunkte auf, so dass als Verfahrenskenndaten eine Nachweisgrenze von 0,08 mg/kg und eine Bestimmungsgrenze von 0,27 mg/kg berechnet werden konnte. Die Be-stimmungsgrenze von 0,27 mg/kg ist in der Mitte der Grafik blau markiert. Der Grenzwert von Dimethoat ist für Salat nach Rückstandshöchstmengen-Verordnung mit 0,5 mg/kg festgesetzt und in der Grafik als rote Raute dargestellt. Selbst bei ungünstigen Analy-senbefunden ist die eingesetzte Methode somit geeignet, den Grenzwert sicher zu bestimmen.
Zusammenfassung
Der Nachweis von Pflanzenschutzmittelrückständen wird auch in Zukunft eine Herausforderung für die moderne Rückstandsanalytik bleiben. Die weltweit mehr als 500 eingesetzten Substanzen sind für den Verbraucher unerwünscht und risikobehaftet, aber technisch nicht immer vermeid-bar. Mit dem vorliegenden Beitrag werden Wege aufgezeigt, wie für die mobilen Lebensmittel-chemischen Laborcontainer Multimethoden zum Nachweis von Pestiziden zur Verfügung gestellt werden können. Die Beschaffung von frischen Lebensmitteln “Vor-Ort“ bzw. aus nicht europäischen Ländern wird auch bei zukünftigen Szenarien zu berücksichtigen bleiben. Während mit der Stir Bar Sorptive Extraction mehr als 500 Pflanzenschutzmittelrückstände mittels GC-MS im Heimatland nachgewiesen werden können, gelingt es mit der QuEChERS-Technik, die erste Multimethode zum Nachweis von Pflanzenschutzmittelrückständen in Obst und Gemüse für die Einsatzlabore zur Verfügung zu stellen. Die vorgestellten Methoden und Techniken verkürzen die Analysenzeit bei der Analytik von Pflanzenschutzmittelrückständen erheblich und tragen somit wesentlich zu einem risikominimierenden Gesundheitsschutz bei, um auch weiterhin die Versorgung der Soldaten im Auslandseinsatz mit gesundheitlich unbedenklichen Lebensmitteln nach den sanitätsdienstlichen Maximen und Sonderregelungen gewährleisten zu können.
Datum: 01.01.2006
Quelle: Wehrmedizin und Wehrpharmazie 2006/1