Bioresorbierbare Magnesiumschrauben (MgYREZr) in der orthopädischen Chirurgie
Bioresorbierbare Schrauben auf Magnesiumbasis sind relativ neu in der Gruppe der orthopädischen Osteosynthese-Materialien. Magnesium (Mg) wird vollständig vom Körper resorbiert, hat osteokonduktive Eigenschaften und hilft, Infektionen vorzubeugen. Der Implantat-Werkstoff MgYREZr ist die erste für eine Anwendung in der orthopädischen Chirurgie zugelassene Magnesium-Legierung weltweit und wird bereits seit 2013 in der klinischen Praxis eingesetzt.
Zusammenfassung
Bioresorbierbare Schrauben auf Magnesiumbasis sind relativ neu in der Gruppe der orthopädischen Osteosynthese-Materialien. Magnesium (Mg) wird vollständig vom Körper resorbiert, hat osteokonduktive Eigenschaften und hilft, Infektionen vorzubeugen. Der Implantat-Werkstoff MgYREZr ist die erste für eine Anwendung in der orthopädischen Chirurgie zugelassene Magnesium-Legierung weltweit und wird bereits seit 2013 in der klinischen Praxis eingesetzt. Es gibt seither eine überschaubare Anzahl klinischer Studien, die Informationen über die funktionellen und radiologischen Ergebnisse sowie die Indikationen und mögliche Komplikationen dieses Materials liefern. Eine umfassende Übersichtsarbeit aus Sicht des klinisch tätigen Chirurgen wurde bislang nicht vorgelegt. Diese narrative Übersichtsarbeit bietet einen Überblick über klinische Studien, radiologische Befunde sowie die Indikationen und Ergebnisse bei der Verwendung Bioabsorbierbarer Magnesiumschrauben.
Stichworte: Magnesium, Schraube, orthopädische Chirurgie, MgYREZr-Legierung, WE43, biodegradierbares Implantat
1. Einleitung
Derzeit werden in der orthopädischen Chirurgie überwiegend metallische Osteosynthese-Materialien aus Edelstahl, Titan, Kobalt-Chrom und seinen Legierungen eingesetzt. Diese Materialien bieten zwar eine relativ hohe mechanische Festigkeit, führen aber durch Unterschiede im Elastizitätsmodul von Knochen und Metallimplantat auf längere Sicht zum sog. „Stress-Shielding-Effekt“. Ferner müssen diese metallischen Implantate oftmals wieder entfernt werden [1]. Operationen zur Implantatentfernung haben in vielerlei Hinsicht zahlreiche Nachteile. Zum einen stellt eine zweite OP eine erhebliche Belastung für die in ihren Ressourcen begrenzten Gesundheitsversorgungseinrichtungen dar [2], zum anderen handelt es sich bei der Implantatentfernung um einen Eingriff, der erneute Komplikationsrisiken birgt. So kann es zu Refrakturen und Infektionen, als auch zu Nerven- und Gefäßschädigungen kommen [3]. Hinzu kommt die mit dem erneuten Eingriff verbundene psychische Belastung des Patienten.
Deshalb wurden alternative Biomaterialien entwickelt. Dabei sollte das ideale Fixationsmaterial für Frakturen über eine angemessene mechanische Festigkeit verfügen, biokompatibel sein, keine unerwünschten Wirkungen auf die Knochenheilung haben und nach abgeschlossener Knochenheilung vollständig vom Körper resorbiert werden. Polymere wie Polyglykolsäure (PGA) oder Polylactid (PLA) sind bereits seit Jahren in der orthopädischen Chirurgie im Einsatz. Aufgrund ihrer geringen mechanischen Festigkeit und der geringen Belastbarkeit sind ihre Anwendungsgebiete allerdings limitiert [4]. Zudem traten immer wieder Probleme wie Entzündungs- und Fremdkörperreaktionen auf [5].
Auf der Suche nach dem optimalen bioresorbierbaren Material hat die Forschung ihren Blick auf Metalle gerichtet, die im Körper abgebaut werden können. Magnesium (Mg) ist gerade deshalb ein attraktiver Werkstoff für die Herstellung orthopädischer Implantate, weil er metallisch ist und die Dichte sowie das Elastizitätsmodul sehr nah an denen des kortikalen Knochens liegen [6]. Die beim Abbauprozess anfallenden Produkte induzieren bzw. fördern zudem die Knochenneubildung. Mg besitzt zudem anti-infektiöse Eigenschaften, die u.a. durch ein Verschieben des pH-Wertes ins basische Milieu begründet sind [7, 8].
Die erstmalige Anwendung von Mg in der orthopädischen Chirurgie reicht schon ins späte 19. Jahrhundert zurück. Der rapide Abbau der ersten Implantate aus reinem Magnesium führte damals allerdings zu einem raschen Verlust der mechanischen Eigenschaften und zur raschen Entstehung großer Mengen von Abbauprodukten im Gewebe, insbesondere Gas [9]. Das eigentliche Problem war also der frühe Zeitpunkt der Degradation. Allerdings konnte durch Fortschritte in Materialwissenschaft, Herstellungstechnik sowie Oberflächenbehandlung dieses Verhalten in der Entwicklung von Mg-Legierungen der neuen Generation auf Basis des Legierungssystems WE 43 (wie z.B. MgYREZr) deutlich verbessert werden. Die Menge der pro Zeit freigesetzten Abbauprodukte wurde dadurch reduziert [10, 11] oder anders: die in vivo-Abbaurate wurde verlängert, so dass die biomechanische Festigkeit der Implantate im Gewebe länger aufrechterhalten blieb. Die Implantate wurden dabei so ausgelegt, dass sie sich - unmittelbar nach Erfüllung ihrer Funktion – restlos im Körper abbauen. Nach mehrjähriger Entwicklung wurden Kompressionsschrauben als erste Implantate aus einer solchen Mg Legierung der neuen Generation 2013 – nach ihrer Zulassung und Erhalt des CE-Zeichens – auf den Markt gebracht [12].
Bislang wurde eine überschaubare Anzahl klinischer Studien publiziert. Ähnliches gilt für Übersichtsarbeiten zu MG-Implantaten. Da diese Implantate in der orthopädischen Chirurgie in den letzten Jahren vermehrt zur Anwendung kommen, soll diese Arbeit in einem narrativen Literaturüberblick die Bedeutung von bioresorbierbaren Magnesiumschrauben in der orthopädischen Chirurgie aufzeigen, ihre klinisch relevanten Anwendungsgebiete, die bisherigen Ergebnisse, Befunde aus bildgebenden Verfahren und potenzielle Komplikationsmöglichkeiten.
2. Anwendungsgebiete für bioresorbierbare Magnesium-Kompressionschrauben
Die Mg-Kompressions-Schraube MAGNEZIX® CS kann für eine ganze Reihe unterschiedlicher Indikationen in der orthopädischen und der Trauma-Chirurgie eingesetzt werden (Abbildung 1): grundsätzlich ist sie geeignet für die Versorgung von Frakturen und Pseudoarthrosen sowie Arthrodesen kleiner Knochen, im Speziellen Kahnbeinfrakturen, Abrissfrakturen, Sprunggelenksfrakturen, intraartikuläre Frakturen der Fußwurzel- und der Mittelfußknochen, der Handwurzel- und Mittelhandknochen, Bunionektomien und Osteotomien am Fuß oder Knöchel, Arthrodesen kleiner Gelenke (z. B. Phalangen), Patella-Frakturen, distale Ulna und Radiusfrakturen, Radiuskopffrakturen und intraartikuläre Frakturen des distalen Humerus [13].
3. Implantate und Operationstechnik
Die Mg-Kompressionsschrauben werden nach dem Herbert- Schrauben-Design hergestellt (Abbildung 2). Hierbei handelt es sich um eine kanülierte Kompressionsschraube mit unterschiedlicher Gewindesteigung und ohne Schraubenkopf, die vom britischen Chirurgen, Timothy James Herbert, entwickelt wurde. Sie war ursprünglich für die stabile Kompressionsosteosynthese von Kahnbeinfrakturen entwickelt worden [14].
Diese Schrauben verfügen über typische Merkmale, die einen operativen Eingriff erleichtern. Zunächst kann die Schraube durch den fehlenden Schraubenkopf vollständig im Knochen versenkt werden und es gibt keine Überstände, die Reizungen verursachen, selbst bei intraartikulärer Platzierung. Die Kanülierung ermöglicht eine exakte Platzierung der Schrauben und erlaubt auch die perkutane Applikation. Im Gegensatz zu den Kortikalisschrauben, die eine konstante Gewindesteigung aufweisen, sorgen diese Schrauben durch die unterschiedliche Steigung am proximalen und distalen Gewinde für eine interfragmentäre Kompression. Die Applikation und die Anwendung von Magnesiumschrauben unterscheiden sich nur wenig von Titan- und Edelstahlimplantaten. Gerade bei der Verwendung von Mg-Schrauben ist das zweistufige Vorgehen beim Einbringen (Vorbohren und Fräsen des Kopfraums) maßgeblich. Ebenso selbstverständlich ist es den Schraubendreher orthogonal aufzusetzen und beim Eindrehen ein nicht zu hohes Drehmoment anzuwenden, um den Schraubenkopf nicht zu beschädigen.
4. Bildgebende Befunde von bioresorbierbaren Magnesiumschrauben
Während des Abbauprozesses bzw. im Resorptionszeitraum der Mg-Implantate können teilweise „ungewöhnliche bildgebende Befunde“ beobachtet werden. Diese Befunde gehören jedoch zum normalen Abbauprozess, sind aber vielen orthopädisch tätigen Chirurgen nicht bekannt. In diesem Dokument sollen die Befunde in der konventionellen Radiographie, der Computertomographie (CT) und der Magnetresonanztomographie (MRT) detailliert behandelt werden.
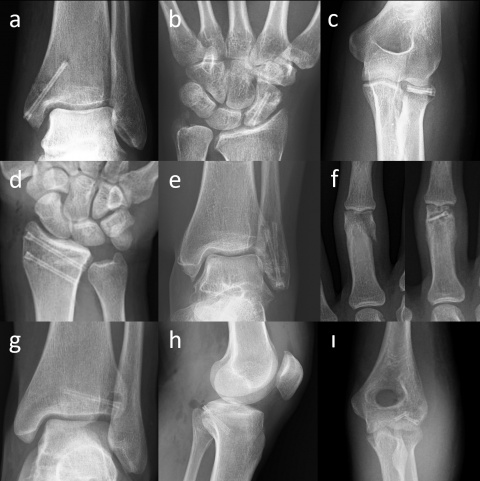
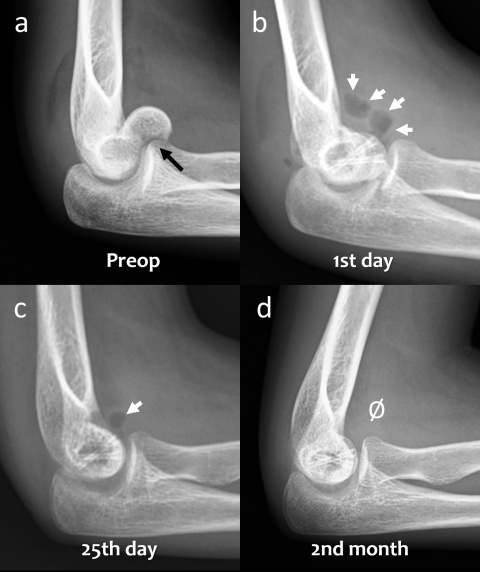
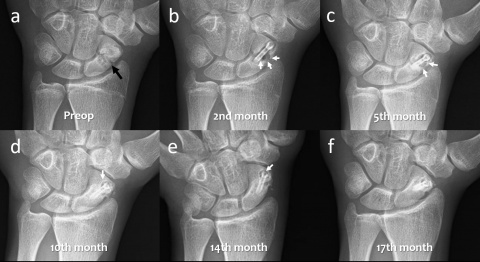
4.1. Konventionelles Röntgen
4.2. Computertomographie
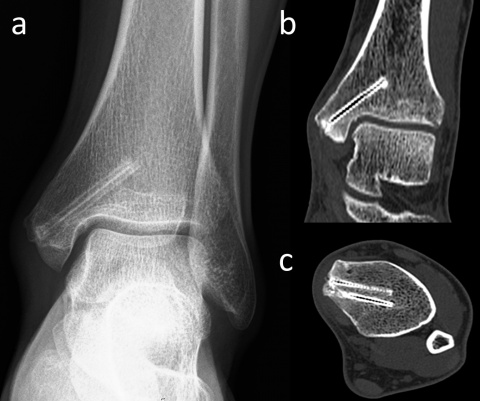
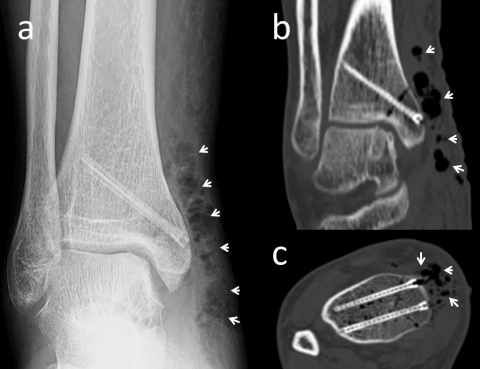
In Bezug auf die Gasbildung und Resorption zeigt die Computertomographie ähnliche Ergebnisse wie die konventionellen Röntgenaufnahmen. In der Frühphase sind sowohl die Schrauben als auch die umgebenden Gasansammlungen deutlich sichtbar (Abbildung 5). Langfristige CT-Untersuchungen zeigen, dass das Gas vollständig resorbiert wird und damit vollständig verschwindet. Die Schrauben sind bis zu ihrer Umwandlung in kortikales Knochengewebe deutlich erkennbar (Abbildung 6). Adil et al. haben nachgewiesen, dass diese Konturen vier Jahre nach der Implantation in der tomographischen Dichtemessung ähnliche Hounsfield-Einheiten aufweisen wie die umgebende Kortikalis (17). Darüber hinaus erzeugen Implantate auf Magnesiumbasis - im Gegensatz zu konventionellen Metallimplantaten wie Titanschrauben - nur minimale Metallartefakte (18-20). Für die Nachbeobachtung der Patienten stellt dies einen signifikanten Vorteil dar.
4.3. Magnetresonanztomographie
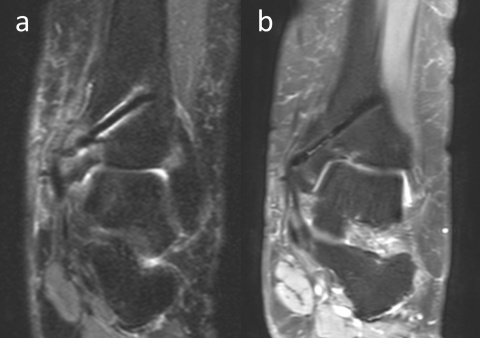
MRT-Scanner erzeugen mithilfe starker Magnetfelder und entsprechender Radiofrequenzsignale digitale Bilder. Wenn metallische Gegenstände im Magnetfeld platziert werden, kann dies zu Verzerrungen des Magnetfelds führen. Diese Verzerrungen können zu signifikanten Störungen der im konventionellen MRT verwendeten räumlichen Kodierungsmechanismen führen und Bilder mit Artefakten und/oder verzerrter Anatomie erzeugen. Dies kann die optimale Beurteilung der MRT-Aufnahmen erheblich beeinträchtigen (18-20).
Als eines der Metalle aus der Gruppe IIa des Periodensystems hat Magnesium paramagnetische Eigenschaften. Frühere experimentelle Studien haben jedoch gezeigt, dass Magnesiumimplantate deutlich weniger Artefakte erzeugen als andere Metallimplantate (Abbildung 7). Sonnow et al. verglichen mithilfe einer 1,5 T MRT mit verschiedenen Sequenzen die Größe der Artefakte, die von Magnesium- und Titanschrauben in Hühnerknochen erzeugt wurden. Sie berichteten bzgl. Magnesiumimplantaten von einer signifikant geringeren Artefaktbildung gegenüber Titanschrauben (18). In ähnlicher Weise demonstrierten Filli et al. und Ernstberger et al. mit Implantaten auf Magnesiumbasis eine geringere Artefaktbildung in der MRT (19, 20). Diese Studien wurden allerdings nicht mit korrodierten Magnesiumimplantaten durchgeführt. Es liegt mit degradierten Implantaten im Menschen jedoch eine MRT-Studie vor, die drei Jahre nach Implantation durchgeführt wurde. Plaass et al. nahmen eine MRT-Evaluation an acht Patienten nach korrektiver Hallux valgus-Osteotomie vor und berichteten über eine lineare Hypointensität im Bereich des ehemaligen Implantatlagers ohne Metallartefakte (21). Diese Ergebnisse weisen darauf hin, dass die Menge der Artefakte während der Resorption des Implantats im Zeitverlauf abnimmt.
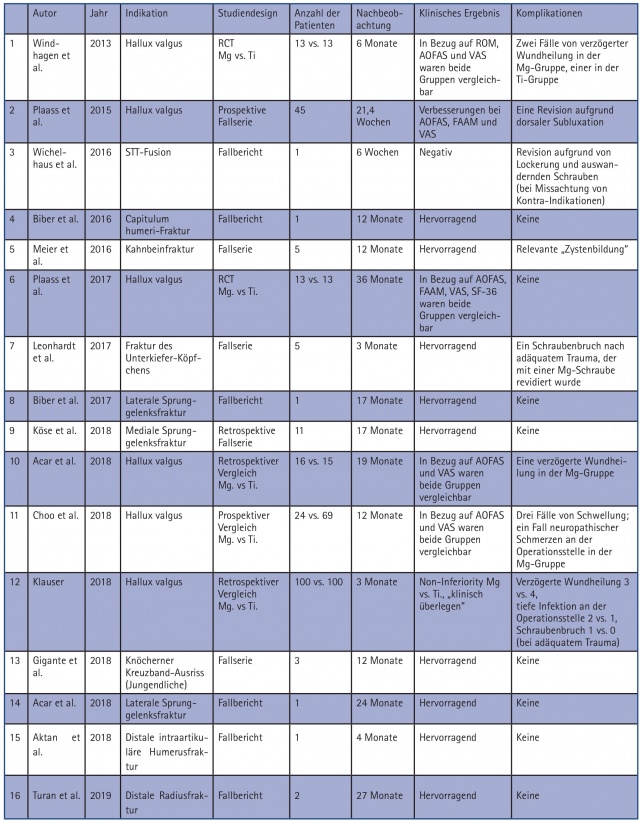
Seit Beginn der Anwendung von Magnesiumimplantaten in der klinischen Praxis im Jahr 2013 wurden insgesamt 16 klinische Studien und Fallberichte zur Verwendung von Magnesium-Implantaten vorgelegt (Tabelle 1) (12, 17,21-34). In sechs dieser früheren Studien wurden Mg-Schrauben zur Fixation von Metatarsal-Osteotomien bei Hallux valgus eingesetzt (21-23, 29-31). Es wurden dabei stets ähnliche Ergebnisse erzielt wie bei Titanschrauben. Es konnte mehrfach gezeigt werden, dass Magnesiumschrauben der Anwendung von Titanschrauben bei der Hallux valgus-Korrektur nicht unterlegen sind (sog. „Non-inferiority“). Auch bei medialen und lateralen Sprunggelenksfrakturen wurden positive Ergebnisse erzielt (27, 33). Köse et al. berichteten, dass die Anwendung von Mg-Schrauben insbesondere bei Sprunggelenksfrakturen von Vorteil ist, weil die Implantate gerade in diesem Bereich sehr häufig entfernt werden müssen (28). Ferner liegen Berichte über die intraartikuläre Anwendung von Magnesiumschrauben vor. Gigante et al. verwendeten Magnesiumschrauben zur Fixierung von Ausrissen des vorderen Kreuzbandes in der Kinderchirurgie und berichteten hervorragende Ergebnisse (32). Aktan et al. verwendeten diese Schrauben zur Fixierung kleiner intraartikulärer osteochondraler Fragmente bei Trümmerfrakturen des distalen Humerus, um die Gelenkfläche wiederherzustellen (34). Magnesiumschrauben zeigten sich sogar in der Anwendung bei Kiefer- und Gesichtsoperationen als geeignet (26).
6. Schlussfolgerungen
Die orthopädische Chirurgie hat sich im Laufe der Jahre nicht nur durch die Beschreibung neuer Operationstechniken, sondern auch durch die Einführung neuartiger Implantationsmaterialien und -designs verändert. Der nahezu vollständige Umstieg von Edelstahlimplantaten zu Titan war eine Entwicklung, die wohl jeder orthopädische Chirurg mitgemacht hat. Was Mg-Implantate angeht, so hat diese Umstellung bereits begonnen und es ist anzunehmen, dass die Ära der konventionellen Implantate aus Polymeren und Titan schon bald ihrem Ende entgegengeht. In den letzten sechs Jahren wurden in einer begrenzten Anzahl von Studien vergleichbare funktionelle Ergebnisse erzielt wie mit Titanimplantaten. Es wurde nur in einem einzigen Fall von einem negativen klinischen Ergebnis berichtet, wobei wir der Ansicht sind, dass dieses negative Ergebnis einer falschen Indikation in der klinischen Situation zuzuschreiben ist. Die negative Auswertung einer Fallserie von fünf Patienten ist ganz offensichtlich auf eine Fehlinterpretation radiologischer Befunde zurückzuführen. Die korrekte Interpretation dieser Aufnahmen sowie die Unterscheidung zwischen pathologischen Prozessen und normalen Abbauprozessen ist sowohl für den orthopädisch tätigen Chirurgen als auch für den mitbefundenden Radiologen äußerst wichtig. Magnesiumbasierte Implantate scheinen aufgrund ihrer signifikanten Vorteile, die sie gegenüber den konventionellen Metallimplantaten bieten, über unterschiedliche Indikationen hinweg zukünftig eine breite Anwendung zu finden.

Artikel von der Syntellix AG zur Verfügung gestellt. Orthopädische Magnesiumimplanate sind u.a. in den BwKrhs Berlin und Hamburg verfügbar. Die Verantwortung für den Inhalt übernimmt der Autor. Übersetzt aus dem Englischen.
7. Literaturangaben
- Hofmann GO. Biodegradable implants in traumatology: a review on the state-of-the-art. Arch Orthop Trauma Surg. 1995;114(3):123-32.
- Böstman O, Pihlajamäki H (1996) Routine implant removal after fracture surgery: a potentially reducible consumer of hospital resources in trauma units. J Trauma 41(5):846–849.
- Kasai T, Matsumoto T, Iga T, Tanaka S. Complications of implant removal in ankle fractures. J Orthop. 2019;16(3):191-194. doi: 10.1016/j.jor.2019.02.017.
- Marukawa E, Tamai M, Takahashi Y, Hatakeyama I, Sato M, Higuchi Y, Kakidachi H, Taniguchi H, Sakamoto T, Honda J, Omura K, Harada H. Comparison of magnesium alloys and poly-l-lactide screws as degradable implants in a canine fracture model. J Biomed Mater Res B Appl Biomater. 2016;104(7):1282-9. doi: 10.1002/jbm.b.33470.
- Raikin SM, Ching AC. Bioabsorbable fixation in foot and ankle. Foot Ankle Clin. 2005 Dec10(4):667-84, ix. Review.
- Kamrani S, Fleck C. Biodegradable magnesium alloys as temporary orthopaedic implants: a review. Biometals. 2019;32(2):185-193. doi: 10.1007/s10534-019-00170-y.
- Waizy H, Diekmann J, Weizbauer A, Reifenrath J, Bartsch I, Neubert V, Schavan R, Windhagen H. In vivo study of a biodegradable orthopedic screw (MgYREZr-alloy) in a rabbit model for up to 12 months. J Biomater Appl. 2014 Jan;28(5):667-75. doi: 10.1177/0885328212472215.
- Rahim MI, Eifler R, Rais B, Mueller PP. Alkalization is responsible for antibacterial effects of corroding magnesium. J Biomed Mater Res A. 2015 Nov;103(11):3526-32. doi: 10.1002/jbm.a.35503.
- Payr E. Beiträge zur Technik der Blutgefäss- und Nervennaht nebst Mitteilungen über die Verwendung eines resorbierbaren Metalles in der Chirurgie. Arch Klin Chir. 1900;62:67–93.
- Witte F. The history of biodegradable magnesium implants: a review. Acta Biomater. 2010 May;6(5):1680-92. doi: 10.1016/j.actbio.2010.02.028.
- Liu C, Ren Z, Xu Y, Pang S, Zhao X, Zhao Y. Biodegradable Magnesium Alloys Developed as Bone Repair Materials: A Review. Scanning. 2018 Mar 13;2018:9216314. doi: 10.1155/2018/9216314.
- Biber R, Pauser J, Geßlein M, Bail HJ (2016) Magnesium-Based Absorbable Metal Screws for Intra-Articular Fracture Fixation. Case Rep Orthop 2016:9673174.
- Seitz JM, Lucas A, Kirschner M (2016) Magnesium-based compression screws: a novelty in the clinical use of implants. JOM 68:1177-1182.
- Herbert TJ, Fisher WE. Management of the fractured scaphoid using a new bone screw. J Bone Joint Surg Br. 1984 Jan;66(1):114-23.
- Dijkman BG, Sprague S, Schemitsch EH, Bhandari M. When is a fracture healed? Radiographic and clinical criteria revisited. J Orthop Trauma. 2010 Mar;24 Suppl 1:S76-80. doi: 10.1097/BOT.0b013e3181ca3f97.
- Mueller WD, Nascimento ML, de Mele MFL (2010) Critical discussion of the results from different corrosion studies of Mg and Mg alloys for biomaterial applications. Acta Biomater 6:1749–1755.
- Turan A, Kati YA, Acar B, Kose O. Magnesium Bioabsorbable Screw Fixation of Radial Styloid Fractures: Case Report. Jnl Wrist Surg 2019 . DOI: 10.1055/s-0039-1685489.
- Sonnow L, Könneker S, Vogt PM, Wacker F, von Falck C. Biodegradable magnesium Herbert screw - image quality and artifacts with radiography, CT and MRI. BMC Med Imaging. 2017 Feb 14;17(1):16. doi: 10.1186/s12880-017-0187-7.
- Filli L, Luechinger R, Frauenfelder T, Beck S, Guggenberger R, Farshad-Amacker N, Andreisek G. Metal-induced artifacts in computed tomography and magnetic resonance imaging: comparison of a biodegradable magnesium alloy versus titanium and stainless steel controls. Skeletal Radiol. 2015 Jun;44(6):849-56. doi: 10.1007/s00256-014-2057-5.
- Ernstberger T, Buchhorn G, Heidrich G. Artifacts in spine magnetic resonance imaging due to different intervertebral test spacers: an in vitro evaluation of magnesium versus titanium and carbon-fiber-reinforced polymers as biomaterials. Neuroradiology. 2009 Aug;51(8):525-9. doi: 10.1007/s00234-009-0537-4.
- Plaass C, von Falck C, Ettinger S et al. (2017) Bioabsorbable magnesium versus standard titanium compression screws for fixation of distal metatarsal osteotomies - 3 year results of a randomized clinical trial. J Orthop Sci. pii: S0949-2658(17)30300-7. https://doi.org/10.1016/j.jos.2017.11.005.
- Windhagen H, Radtke K, Weizbauer A et al. (2013) Biodegradable magnesium-based screw clinically equivalent to titanium screw in hallux valgus surgery: short term results of the first prospective, randomized, controlled clinical pilot study. Biomed Eng Online. 12:62. https://doi.org/ 10.1186/1475-925X-12-62.
- Plaass C, Ettinger S, Sonnow L et al. (2016) Early results using biodegradable magnesium screw for modified chevron osteotomies. J Orthop Res 34(12):2207-2214. https://doi.org/10.1002/jor.23241.
- Wichelhaus A, Emmerich J, Mittlmeier T (2016) A Case of Implant Failure in Partial Wrist Fusion Applying Magnesium-Based Headless Bone Screws. Case Rep Orthop 2016:7049130.
- Meier R, Panzica M (2017) First results with a resorbable MgYREZr compression screw in unstable scaphoid fractures show extensive bone cysts. Handchir Mikrochir Plast Chir 49(1):37-41.
- Leonhardt H, Franke A, McLeod NMH, Lauer G, Nowak A. Fixation of fractures of the condylar head of the mandible with a new magnesium-alloy biodegradable cannulated headless bonescrew. Br J Oral Maxillofac Surg. 2017 Jul;55(6):623-625. doi: 10.1016/j.bjoms.2017.04.007.
- Biber R, Pauser J, Brem M, Bail HJ (2017) Bioabsorbable metal screws in traumatology: A promising innovation. Trauma Case Reports (8):11-15.
- Kose O, Turan A, Unal M, Acar B, Guler F. Fixation of medial malleolar fractures with magnesium bioabsorbable headless compression screws: short-term clinical and radiological outcomes in eleven patients. Arch Orthop Trauma Surg. 2018 Aug;138(8):1069-1075. doi: 10.1007/s00402-018-2941-x.
- Acar B, Kose O, Turan A, Unal M, Kati YA, Guler F. Comparison of Bioabsorbable Magnesium versus Titanium Screw Fixation for Modified Distal Chevron Osteotomy in Hallux Valgus. Biomed Res Int. 2018 Nov 19;2018:5242806. doi: 10.1155/2018/5242806.
- Choo JT, Lai SHS, Tang CQY, Thevendran G. Magnesium-based bioabsorbable screw fixation for hallux valgus surgery - A suitable alternative to metallic implants. Foot Ankle Surg. 2018 Sep 22. pii: S1268-7731(18)30392-8. doi: 10.1016/j.fas.2018.09.001.
- Klauser H. Internal fixation of three-dimensional distal metatarsal I osteotomies in the treatment of hallux valgus deformities using biodegradable magnesium screws in comparison to titanium screws. Foot Ankle Surg. 2018 Feb 16. pii: S1268-7731(18)30030-4. doi: 10.1016/j.fas.2018.02.005.
- Gigante A, Setaro N, Rotini M, Finzi SS, Marinelli M. Intercondylar eminence fracture treated by resorbable magnesium screws osteosynthesis: A case series. Injury. 2018 Nov;49 Suppl 3: S48-S53. doi: 10.1016/j.injury.2018.09.055
- Acar B, Unal M, Turan A, Kose O. Isolated Lateral Malleolar Fracture Treated with a Bioabsorbable Magnesium Compression Screw. Cureus. 2018;10(4):e2539. doi:10.7759/cureus.2539.
- Aktan C, Ertan MB, Turan A, Kose O. Fixation of Small Osteochondral Fragments in a Comminuted Distal Humerus Fracture with Magnesium Bioabsorbable Screws: A Case Report. Cureus. 2018 Dec 19;10(12):e3752. doi: 10.7759/cureus.3752.
Datum: 07.08.2019