Perspektiven Molekularer Diagnostik und maßgeschneideter Therapien
Personalisierte Medizin auf dem Vormarsch
Es ist jedem Mediziner ins Stammbuch geschrieben, dass er auftretende Krankheiten zu heilen, zu lindern oder gar zu vermeiden habe.
Zu Beginn des 21. Jahrhunderts befinden sich die biomedizinsche Forschung und die klinische Medizin in einem Umbruch, der nicht von wenigen als Paradigmen wechsel bezeichnet wird.
Neue, auf Genomanalysen und biomedizinischen Technologien basierende Ansätze machen es möglich, Lebensprozesse präziser und umfassender als bisher zu analysieren. Damit verbunden ist die Hoffnung, Krankheitsursachen besser zu verstehen, eindeutige Diagnosen zu stellen und nicht zuletzt hochwirksame, zielgenaue und nebenwirkungsarme Therapien zu entwickeln.
Der Begriff “Precision Medicine“ hat in der internationalen Fachliteratur Konjunktur. Die Anzahl der Publikationen zu diesem Thema wächst exponentiell, die Suchanfragen in Internet nehmen zu.
Vor diesem Hintergrund ist es sicherlich ein guter Zeitpunkt, sich mit dem Thema grundsätzlich einmal zu befassen.
Heilung nach Maß
Schnellere Computer und intelligente Datenverknüpfung ermöglichen erstmals einen völlig neuen Ansatz in der Heilkunde: “Die Präzionsmedizin“, der alte Traum von der personalisierten Therapie, könnte damit Wirklichkeit werden, unser Verständnis von Krankheiten grundlegend zu verändern.
Seit Hippokrates bestimmen empirische Beobachtungen, Befundaufzeichnungen und zeitgemäße Vorgehensweisen die medizinische Behandlung von erkrankten Menschen. Bahnbrechende Forschritte sind zu jeder Zeit mit der Entwicklung der Naturwissenschaften erfolgt. Der Kausalitätsgrundsatz bestimmte den Weg neuzeitlicher Diagnostik und Therapie (Abb. 1).
Die Entschlüsselung des menschlichen Genoms bildet nun einen Meilenstein auf dem neuesten Weg zu einer auf umfassenden individuellen Merkmalen von Patienten aufbauenden Dignose und Therapie von Erkrankungen.
Precision Medicine zielt darauf ab, durch gezielte Prävention, systematische Diagnostik und den Einsatz maßgeschneideter, auf die Bedürfnisse einzelner Patienten oder Patientengruppen ausgerichteter Therapieverfahren die Wirksamkeit und Qualität der Behandlung zu verbessern Dabei sollen unerwünschte Nebenwirkungen reduziert und langfristig die “Non-responder Rate“ vermindert werden (Abb. 2).
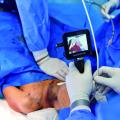
Es sind vorrangig molekulare Techniken zur gezielten Bestimmung biologischer Messgrößen, sogenannte Biomarker; die in den Behandlungsprozess einbezogen werden (Abb. 3).
Es ist eine gewaltige interdisziplinäre Herausforderung, die Vielzahl der dabei gewonnenen Daten zu analysieren und mit bestimmten Krankheitsbildern bzw. der Wirkung medizinischer Behandlung zu korrelieren.
Therapieverfahren auf dem Prüfstand
Die Tumortherapie durchläuft zurzeit einen fundamentalen Wandel. Tumoren sind überwiegend die Folge genetischer Veränderungen in Körperzellen. Die meisten Tumorzellen beinhalten zahlreiche (50 - 30 000) Mutationen, die komplexe Veränderungen nach sich ziehen. Das vertiefte Verständnis der molekularen Mechanismen der Entstehung zahlreicher Tumorarten führt zu einer neuen Klassifiziereung der Tumorerkrankungen und ermöglicht, molekulare Tumordiagnostika und darauf aufbauende zielgerichtet wirkende Therapeutika zu entwickeln. Es zeichnet sich ab, dass die Anwendung dieser Therapien mit geringen Nebenwirkungen verbunden ist als konventionelle Behandlungsmethoden. Somit stehen althergebrachte Therapieformen auf dem Prüfstand.
Weltweit werden jährlich viele Millionen an Krebs erkrankte Patienten chemotherapeutisch behandelt. Herkömmliche Chemotherapeutika wirken in der Regel auch auf Wechselgewebe mit sich schnell teilenden Zellen (Knochenmark, Epithel des Magen-Darmtraktes.
Krebszellen teilen sich relativ häufig, auf diese Weise wächst ein Tumor schnell und verdrängt und zerstört das Nachbargewebe. Also greift man nach wie vor zum Chemotherapeutikum, das all jene Zellen angreift, die sich rasch teilen. Doch das tun neben Krebszellen auch andere Zellen in den Haarwurzeln, im Verdauungstrakt und im Immunsystem. Eine Chemotherapie erwischt eine Menge Tumorzellen, aber eben noch mehr andere Körperzellen. Das führt dazu, dass der Patient sich elend fühlt, seine Haare verliert, an Übelkeit und Erbrechen leidet und extrem anfällig gegenüber Infektionen ist. Kurz gesagt, man greift alles im Körper an, was sich schnell vermehrt, nur um einen bestimmten, zumeist nur wenige Millimeter großen Zellhaufen zu zerstören.
Tumorerkrankungen sind ganz überwiegend genetische Veränderungen in Körperzellen.Die Verfügbarkeit von Gewebeproben, die zu diagnostischen Zwecken entnommen werden, macht die molekulare Analyse möglich. Aus dem resultierendem genetischen Profil erhält man tiefgreifendes Verständnis des Tumorgeschehens. Darüber hinaus erhält man eine präzise Zuordnung der Tumoren zu den molekularen Untergruppen. Bereits heute werden bei vielen malignen Tumoren Therapieentscheidungen in Abhängigkeit nicht nur von morphologischen, sondern auch vom zusätzlich erhobenen molekularbiologischen Befund getroffen. Ähnliche Verfahrensweisen gelten auch für die Diagnostik und Therapie von Infektionskrankheiten. In der Neurologie sollen molekularbiologische Analysen Wege für die frühzeitige Diagnose und Differenzierung unterschiedlicher Formen der Demenz eröffnen. Eine frühzeitige und präzise Diagnose molekularer Ursache einer langsam fortschreitenden Erkrankung, wie des Morbus Parkinson und des Morbus Alzheimer ist der erste notwendige Schritt zur Entwicklung einer Therapie oder einer Präventionsmaßnahme.
Ein großer Teil der häufigsten chronischen Erkrankungen, die insbesondere im höheren Alter auftreten sind multifaktoriell bedingt. Es sind neben genetisch bedingter Erkrankungen auch Umwelteinflüsse und nicht konforme Lebensgewohnheiten. Hierzu gehören die Herz-Kreislauferkrankungen, ebenso wie Diabetes mellitus, und neurodegenerative Erkrankungen. Chronische Erkrankungen können bisher nur eingeschränkt kausal behandelt werden
Präzisionsmedizin BIG DATA: Molekulare Diagnostik und IT-Technologie
Ärzte haben schon immer auf der Grundlage von Patientendaten eine Anamnese von Patienten erhoben, eine körperliche Untersuchung durchgeführt und die Beschwerden mit ihrem ärztlichen Wissen und Können – mit und ohne adjuvante Diagnostik mit pysiologischen Daten und Laborparametern – in einen Befund einfließen lassen. Daraus wurde die Diagnose gestellt, um eine – wie auch immer geartete Therapie – durchzuführen (Abb. 4).
Dieses eingespielte Instrumentarium der Medizin wird nun um einen gezielten methodischen Einsatz vorrangig molekularer Techniken erweitert. Biologische Messgrößen, insbesondere molekulare Biomarker, sollen zusätzlich zu Behandlungsprozess herangezogen werden. Vom Einsatz dieser Biomarker wird erwartet, dass sie eine zunehmend präzise Bestimmung individueller biologischer Eigenschaften ermöglichen, die als Grundlage für eine entsprechende Diagnose und Therapie dienen. Im weiten Blick bietet sich die Möglichkeit, die Medizin zu objektivieren, indem relevante Veränderungen beim Patienten präzise vermessen und kuriert werden können. Weiterhin wird langfristig eine aussagekräftige, verfeinerte Zuordnung von Erkrankungen in taxonomische Gruppen angestrebt, die ihrerseits den Ausgangspunkt für die Entwicklung von darauf abgestimmten Diagnostika und Therapien bilden. Es ist davon auszugehen, dass sich die verfügbare Menge krankheitsrelevanter Patientendaten erhöhen wird. Die Herausforderung für die individualisierte Medizin besteht unter anderem darin, diese komplexen personenbezogenen Daten standardisiert zu sichern und daraus Ergebnisse und Handlungsoptionen abzuleiten. Diese müssen für den behandelnden Arzt, den in der medizinischen Forschung tätigen Wissenschaftler und für den Patienten transparent sein. Die Bewältigung neuer Anforderungen in der individualisierten Medizin kann nur in einem multidisziplinären Team erfolgen (Abb. 5).
Die Konsequenzen einer individualisierten Medizin lassen sich schwer voraussagen. Sie erfordert die Integration neuer organisatorischer Abläufe in bestehende Strukturen des Gesundheitswesens. Hiervon wird auch der militärische Sanitätsdienst betroffen sein, wenn er der Maxime weiter folgt, dass er dem Soldaten die im Ergebnis gleiche medizinische Versorgung zugestehen will, wie im zivilen Bereich üblich.
Obgleich die ökonomischen Auswirkungen für die Gesundheitsversorgung, die mit der “Individualisierten Medizin“ verbunden sind, nicht verlässlich absehbar sind, ist davon auszugehen, dass trotz anfänglich zu erwartenden Kostensteigerungen, es in der Folge durch die evidenzbasierte Medizin zu Kosteneinsparungen kommen wird. Die Datenverarbeitung auf der Grundlage von Bioinformatik wird eine zunehmende Bedeutung erlangen.
Die Bioinformatik stellt die methodische Grundlage zur Zusammenführung der Patientendaten sowie zu deren Filterung, Korrelation und Auswertung dar. Die qualitativ sehr unterschiedlichen Daten müssen medizinisch redundant und reliabel sein.
Insbesondere die Next-Generation DNA Sequenzierung ist für die Entwicklung von genomischen Biomarkern von herausragender Bedeutung. Mit ihr können pro Gerät und Untersuchungsgang hundert Millionen DNA Fragmente parallel sequenziert werden, so dass diese Hochleistungsmethode es mittlerweile erlaubt, das Genom von Einzelpersonen für bald unter 1 000 Dollar in wenigen Tagen vollständig zu entschlüsseln. Die NGS(Next-Generation Sequenzierung) ist bereits heute state of the art und wird in der Onkologie (Sequenzierung von Tumorgewebe) als Standard angewendet.
Die vollständige oder teilweise Erfassung der DNA ist eine wichtige Basis für Precision Medicine. Biomarker können in Zukunft auch einen wichtigen Beitrag für die Planung und Gestaltung klinischer Studien zur Erprobung neuer Therapien leisten. Da das Auftreten und die Ausprägung von Biomarkern dem klinischen Ansprechen eines Patienten auf eine Therapie zeitlich vorausgehen, können sie als alternative Endpunkte klinischer Studien dienen und diese damit deutlich beschleunigen und vereinfachen.
Ausblick
Im Hinblick auf medizinische Fragestellungen und die Notwendigkeit zur Beratung der zu untersuchenden Menschen stellt die Interpretation der Millionen DNA Sequenzierungsdaten eines individuellen Genoms eine große Herausforderung dar. Die Ermittlung von Krankheiten sowie von Krankheitsrisiken aufgrund genetischer Disposition kann die individuelle Anpassung von Versorgungsstrategien ermöglichen. So wie die Prävention von genetisch mitbedingten häufigen Erkrankungen wenig erforscht ist, so ist die Behandlung in der Onkologie durch Therapieempfehlungen bereits heute schon weit verbreitet.
Als US Präsident Richard Nixon 1971 den “Krieg gegen den Krebs“ erklärte, schien das Ziel, die Krankheit in einem nationalen Kraftakt binnen 25 Jahren zu besiegen nicht utopischer als John F. Kennedy`s Vorgabe von 1961, noch vor dem Ablauf des Jahrzehnts einen Menschen auf den Mond zu bringen. Doch der Krebs hat sich als hartnäckiger Gegner erwiesen.
Im Januar 2015 hat der US Präsident Obama 215 Mio Dollar für Forschungszwecke bezüglich Precision Medicine auf die nationale Agenda gehoben. Seine Initiative gilt dem Kampf gegen den Krebs auf der Grundlage von molekularer Medizin. Zunächst werden Studien unterstützt mit dem Ziel Genomdaten auszuwerten. Precision Medicine soll genetische Profile auf neuzeitliche medikamentöse Therapien individuell adaptieren.
Der Aufbruch in ein neues medizinisches Zeitalter hat begonnen. Wir sind inmitten einer hoffnungsvollen “Transformation“!
Literatur beim Verfasser.
Datum: 12.11.2015
Quelle: Wehrmedizin und Wehrpharmazie 2015/3