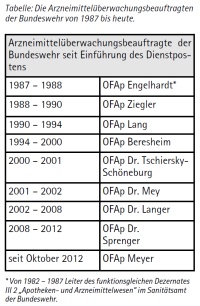
ARZNEIMITTELÜBERWACHUNGSBEAUFTRAGTER DER BUNDESWEHR
Rund 30 Jahre lang haben die Inhaber des Dienstpostens „Sanitätsstabsoffizier Apotheker beim Inspizienten Wehrpharmazie der Bundeswehr“ die Aufgaben einer „zentralen aufsichtsbehördlichen, arzneimittel- und apothekenrechtlichen Überwachungsstelle der Bundeswehr“ wahrgenommen.
Im Rahmen der Neuausrichtung der Bundeswehr wurde der Arzneimittelüberwachungsbeauftragte der Bundeswehr (AMÜBBw) am 1. Oktober 2012 eigenständig. Im Folgenden wird die Entwicklung des Dienstpostens und der Aufgaben des AMÜBBw kurz dargestellt.
Rechtliche Rahmenbedingungen1
Nach Aufstellung der Bundeswehr wurde in Analogie zur rechtlichen Stellung bei Reichswehr und Wehrmacht das Arzneimittel- und Apothekenwesen in der Bundeswehr zunächst von den in der jungen Bundesrepublik zivil gültigen Rechtsbestimmungen ausgenommen. Dadurch sollte gewährleistet werden, dass die Bundeswehr im Verteidigungsfall ohne Verzug Handlungsfreiheit u.a. bei der Herstellung, Prüfung, Lagerung und Verteilung sowie bei der Ver- und Anwendung von Arzneimitteln besitzt. Sowohl der Verkehr mit Arzneimitteln als auch der Betrieb von Apotheken in der Bundeswehr wurden allerdings durch Zentrale Dienstvorschriften geregelt, die eng an die zivilen Rechtsbestimmungen angelehnt waren.
Ab Mitte der 1960er Jahre wurden zwischen dem Bundesministerium der Verteidigung (BMVg) und dem Bundesgesundheitsministerium erste Gespräche aufgenommen, um die Gültigkeit nicht nur der arzneimittel- und apothekenrechtlichen zivilen Rechtsbestimmungen auf den Bereich der Bundeswehr auszudehnen. Dass Regelungsbedarf bestand, wurde Anfang der 1970er Jahre deutlich: Mit der Öffnung der Bundeswehrkrankenhäuser (BwKrhs) für Zivilpatienten war das Arzneimittel- und Apothekenwesen in der Bundeswehr zu einer rechtlichen Grauzone geworden. Schließlich erfolgte die Versorgung der zivilen Patienten in den BwKrhs mit Arzneimitteln, die formal nicht dem Arzneimittelrecht unterlagen, noch dazu aus Apotheken, die formal nicht dem Apothekenrecht unterlagen. Die Gespräche fruchteten, so dass die Bundeswehr nach und nach in den zivilen Rechtsbestimmungen berücksichtigt wurde, zum Beispiel 1968 in der Bundesapothekerordnung, 1976 im Arzneimittelgesetz und 1980 im Apothekengesetz.
Aufgrund des föderalistischen Prinzips der Überwachungsaufgaben und der militärischen Besonderheiten der Streitkräfte sah der Gesetzgeber jedoch von Anfang an vor, dass die Durchführungs- und Überwachungsaufgaben weiterhin von bundeswehreigenen Stellen und Sachverständigen wahrzunehmen sind. Diese in den jeweiligen Rechtsvorschriften verankerte „Eigenvollzugskompetenz“ der Bundeswehr bedeutet in der Praxis die rechtliche Gleichstellung der Bundeswehr mit den Bundesländern. Sie ist die Grundlage für sämtliche öffentlich-rechtlichen Aufgaben des Sanitätsdienstes der Bundeswehr und damit auch für den Arzneimittelüberwachungsbeauftragten der Bundeswehr.
Organisatorische Entwicklung
Zeitgleich mit dem Beginn der Sondierungsgespräche wurde im Jahr 1965 der Dienstposten des „Inspizienten Pharmazie und Sanitätsmaterial der Bundeswehr“ beim Sanitätsamt der Bundeswehr geschaffen, der seit 1984 „Inspizient Wehrpharmazie der Bundeswehr“ (Inspiz WehrPharmBw) heißt. Dem Inspizienten wurde ein Sanitätsstabsoffizier (SanStOffz) Apotheker zur Seite gestellt, der ihn bei seinen Inspizierungsaufgaben unterstützen sollte.
Ab dem Jahr 1970 wurde in Erlassen, Geschäftsverteilungsplänen und schließlich mit einer Dienstanweisung geregelt, worin die Inspizierungsaufgaben des Inspizienten und seines Mitarbeiters eigentlich bestanden. Dem „Sanitätsstabsoffizier Apotheker beim Inspizienten“ wurde u.a. die Wahrnehmung der Aufgabe einer „zentralen aufsichtsbehördlichen, arzneimittel- und apothekenrechtlichen Überwachungsstelle der Bundeswehr“ zugewiesen.
Als im Jahr 1982 das Dezernat III 2 „Apotheken- und Arzneimittelwesen“ im Sanitätsamt der Bundeswehr neu eingerichtet wurde, wurde dessen Leitung dem beim Inspizienten tätigen SanStOffz Apotheker übertragen. Diese seinerzeit erste sollorganisatorische Abbildung der pharmazeutischen öffentlich-rechtlichen Überwachungsaufgaben in der Bundeswehr trug der Umsetzung der neuen rechtlichen Rahmenbedingungen Rechnung, nämlich der Gültigkeit der zivilen Rechtsbestimmungen für den Bereich der Bundeswehr.
Noch weitere fünf Jahre vergingen, ehe am 24. Februar 1987 der nach wie vor so bezeichnete „Sanitätsstabsoffizier Apotheker beim Inspizienten Wehrpharmazie der Bundeswehr im Sanitätsamt der Bundeswehr“ als „Beauftragter für die aufsichtsbehördliche Überwachung des Verkehrs mit Arzneimitteln in der Bundeswehr“, kurz „Arzneimittelüberwachungsbeauftragter“ der Bundeswehr (AMÜbwBeauftrBw – AMÜBBw) mit einer vom Inspekteur des Sanitäts- und Gesundheitswesens erlassenen Dienstanweisung auch begrifflich institutionalisiert wurde2. Diese eingängige Bezeichnung sollte klar stellen, wer die in der Bundeswehr „zuständige Behörde“ ist, die in den einschlägigen Rechtsbestimmungen immer wieder genannt wird. Darüberhinaus ist eine deutliche Vereinfachung in Schriftverkehr und sprachlichem Gebrauch gegenüber der umständlichen Langbezeichnung ist sicher auch nicht zu verkennen.
Noch heute, 26 Jahre nach Einführung des Dienstpostens, wird die Kurzbezeichnung verwendet, meist sogar nur in Form des Akronyms „AMÜB“, auch wenn die Zuständigkeit der „zuständigen Behörde“ inzwischen weit mehr als „nur“ das Arzneimittel- und Apothekenrecht umfasst.
Die Verknüpfung des Inspiz WehrPharmBw als zentrale zuständige Stelle für die aufsichtsbehördliche Überwachung des Verkehrs mit Arzneimitteln in der Bundeswehr und der Wahrnehmung dieser Aufgabe durch den AMÜBBw hatte bis zum 30. September 2012 Bestand.
Vom 1. Oktober bis 31. Dezember 2012 war der AMÜBBw im neu aufgestellten Kommando Sanitätsdienst der Bundeswehr (Kdo SanDstBw) übergangsweise in der Abteilung A „Planung, Führung und Steuerung der Gesundheitsversorgung“ und dort in der Unterabteilung V „Pharmazie und Lebensmittelchemie“ im Referat 1 „Pharmazie“ als Sachgebietsleiter V 1.5 „Arzneimittelüberwachungsbeauftragter“ erstmals unabhängig vom Inspiz WehrPharmBw ausgebracht.
Mit Wirkung vom 1. Januar 2013 wurde der Dienstposten in die ebenfalls zu diesem Datum neu aufgestellte „Überwachungsstelle für öffentlich-rechtliche Aufgaben des Sanitätsdienstes der Bundeswehr“ (ÜbwStÖffRechtlAufgSanDstBw) Süd mit dem Schwerpunkt Lebensmittelchemie und Pharmazie überführt. Derzeit befindet sich diese Überwachungsstelle noch im Niederbayerischen Bogen, in der Zielstruktur 2020 wird sie jedoch mit dem Zentralen Institut des Sanitätsdienstes der Bundeswehr (ZInstSanBw) München coloziert werden, das ebenfalls den Schwerpunkt Lebensmittelchemie und Pharmazie besitzt.
Mit der Entkopplung des AMÜBBw in seiner Eigenschaft als „zuständige Behörde“ vom Inspizienten Wehrpharmazie der Bundeswehr bei gleichzeitiger Einführung des Referatsleiters V 1 als „Oberbehörde“ beim Kdo SanDstBw folgt die Behördenstruktur im wehrpharmazeutischen Aufgabenbereich nunmehr dem zivilen Beispiel. Damit wurde der vorerst letzte noch ausstehende Schritt der 1965 begonnenen Anpassung der öffentlich-rechtlichen Aufgaben im Arzneimittel- und Apothekenwesen der Bundeswehr an den Aufbau im zivilen Bereich auch sollorganisatorisch vollzogen.
Aufgaben im Überblick
Wie die Bundeswehr selbst waren die öffentlich-rechtlichen pharmazeutischen Überwachungsaufgaben in den vergangenen Jahrzehnten erheblichen Änderungen unterworfen. Ursache dafür ist zum Einen die stetige qualitative und quantitative Weiterentwicklung der regulatorischen Anforderungen im Verkehr mit Arzneimitteln und beim Betrieb von Apotheken und zum Anderen die Erweiterung der Zuständigkeit des AMÜBBw auf neue Rechtsgebiete. Er überwacht nunmehr die Einhaltung rechtlicher Bestimmungen nach dem
- Apotheken-,
- Arzneimittel-,
- Betäubungsmittel-,
- Grundstoffüberwachungs-,
- Medizinprodukte-,
- Transfusions-,
- Transplantations-,
- Gewebe- und
- Chemikaliengesetz sowie
- der Bundes-Apothekerordnung,
jeweils einschließlich der nachgeordneten Rechtsvorschriften sowie der dazu erlassenen Verwaltungsvorschriften, Richtlinien, Dienstvorschriften und Durchführungsbestimmungen. Die Bezeichnung „Arzneimittelüberwachungsbeauftragter“ umfasst also nur einen Teil seines vielfältigen und anspruchsvollen Überwachungsauftrages.
Sämtliche Einrichtungen und Dienststellen der Bundeswehr unterliegen unabhängig von Teilstreitkraft oder Organisationsbereich der Überwachung durch den AMÜBBw, wenn sie am Verkehr mit Arzneimitteln (einschließlich Betäubungsmittel, Blut- und Blutprodukte sowie Gewebe) oder Medizinprodukten (einschließlich der Durchführung laboratoriumsmedizinischer Untersuchungen) teilnehmen. Das sind alle Dienststellen und Einrichtungen, in denen Arzneimittel hergestellt, geprüft, gelagert, verpackt oder in Verkehr gebracht oder Arzneimittel entwickelt oder klinisch geprüft werden sowie solche, in denen Medizinprodukte hergestellt, klinisch geprüft, verpackt, ausgestellt, betrieben, errichtet, angewendet, in den Verkehr gebracht werden oder sonst mit ihnen Handel getrieben wird bzw. in denen laboratoriumsmedizinische Untersuchungen durchgeführt werden.
Im Rahmen seiner Überwachungstätigkeit führt der AMÜBBw daher aufsichtsbehördliche Abnahmen, Revisionen und Inspektionen durch bei den
- Bundeswehrapotheken des Bundeswehrzentralkrankenhauses Koblenz sowie der BwKrhs Hamburg, Berlin und Ulm;
- Bundeswehrapotheken der Versorgungs- und Instandsetzungszentren Sanitätsmaterial Quakenbrück, Pfungstadt, Blankenburg und Sigmaringen sowie bei der Bundeswehrapotheke Wilhelmshaven;
- Bundeswehrapotheken der Gerätehauptdepots der Streitkräftebasis (Sanitätsmateriallager) in Bramstedtlund, Epe und Krugau;
- Bundeswehrapotheken im Einsatz, einschließlich des Marineeinsatzrettungszentrums;
- Arzneimittelherstellungsbetrieben der Bundeswehr mit einer Erlaubnis nach § 13 Arzneimittelgesetz;
- Einrichtungen, die Laboruntersuchungen für die Herstellungsbetriebe der Bundeswehr durchführen;
- Sektionen/Abteilungen Laboratoriumsmedizin der BwKrhs, einschließlich spezialdiagnostischer Laboratorien der Abteilungen sowie der patientennahen Labordiagnostik (point-of-care treatment – POCT) und der ZInstSanBw;
- Gewebegewinnungseinrichtungen der Bundeswehr, einschließlich der Laboratorien zur Spendereignungsuntersuchung;
- in Einrichtungen der Bundeswehr durchgeführten klinischen Prüfungen.
Bei der Überwachung der regionalen Sanitätseinrichtungen und der Sanitätseinrichtungen der Teilstreitkräfte und Organisationsbereiche in der Basis Inland sowie in den Einsatzgebieten wird der AMÜBBw von den pharmazeutischen Sachverständigen der Abteilung IV des ZInstSanBw München und den Abteilungen IV der ÜbwStÖffRechtlAufgSanDstBw bzw. den Leitenden Apothekern im Einsatz unterstützt, die ihm hinsichtlich ihrer pharmazeutischen Überwachungstätigkeit fachlich unterstellt sind.
Der AMÜBBw ist die in der Bundeswehr zuständige Ortsbehörde im Sinne des Arzneimittel-, des Apotheken- und des Medizinproduktegesetzes und damit u. a. für die Erteilung arzneimittel- und apothekenrechtlicher Erlaubnisse und Genehmigungen
- zur Herstellung von Arzneimitteln,
- zur Gewinnung, Weiterverarbeitung und Untersuchung von Gewebe sowie
- zum Betrieb von Apotheken zuständig.
Er ist die Stelle, der die Durchführung von klinischen Prüfungen oder die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte anzuzeigen ist. Darüber hinaus entnimmt der AMÜBBw amtliche Proben nach § 65 Arzneimittelgesetz und § 26 Medizinproduktegesetz.
Qualitätsmanagement
Der AMÜBBw betreibt ein Qualitätsmanagementsystem (QMS) in Anlehnung an die Vorgaben der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG). Das Qualitätssystem der Länder hat zum Ziel, die Arzneimittelüberwachung und –untersuchung nach nationalen und internationalen Standards zum Schutz von Mensch und Tier zu harmonisieren und darüber hinaus transparent und vertrauensbildend darzustellen.
Das QMS schließt die Schulung und Auditierung der pharmazeutischen Sachverständigen des ZInstSanBw München und der ÜbwStÖffRechtlAufgSanDstBw sowie die Leitung und Durchführung von Dienstbesprechungen im Bereich der pharmazeutischen Überwachungsaufgaben mit ein.
Zusammenarbeit mit zivilen Stellen
Aufgrund seiner Funktion als „zuständige Behörde“ bestehen zahlreiche Schnittstellen zwischen dem AMÜBBw und dem zivilen Bereich. Bei den regelmäßig durchzuführenden Inspektionen des Blutspendedienstes der Bundeswehr zum Beispiel, werden immer die Sachverständigen des Paul-Ehrlich-Instituts (PEI) beteiligt, wie im Arzneimittelgesetz vorgesehen. Aber auch die im jeweiligen Bundesland regional zuständigen Überwachungsbehörden werden regelmäßig eingeladen, Inspektionen als Gast zu begleiten.
Auch wenn die Überwachung der Arzneimittelherstellungsbetriebe oder der Bundeswehrapotheken in alleiniger Zuständigkeit der Bundeswehr liegt, ist Transparenz in diesem sensiblen Bereich wichtig, um gegenseitiges Vertrauen zu schaffen. Darüber hinaus kann man von den Erfahrungen der Spezialisten in vielfältiger Weise profitieren. Weitere Kontakte bestehen bei der Weitergabe von Meldungen im Zusammenhang mit Arzneimittelereignissen, Look-back-Verfahren und bei der Mitarbeit in nationalen und internationalen zivilen und militärischen Fachgremien der Arzneimittelüberwachung.
Der AMÜBBw ist Mitglied in den Expertenfachgruppen (EFG) „Biotechnologie und Gewebe“ sowie „Blut und Blutprodukte“ der ZLG. Im Rahmen des o.g. länderübergreifenden Qualitätssystems der Arzneimittelüberwachung sind die vorrangigen Aufgaben der EFG Grundlagen für die Arzneimittelüberwachung und -untersuchung zu erarbeiten, Stellungnahmen zu nationalen und europäischen Rechtsvorschriften und Leitlinien zu verfassen sowie Fortbildungsveranstaltungen für die in der Arzneimittelüberwachung und -untersuchung Tätigen durchzuführen.
Die EFG „Biotechnologie und Gewebe“ beschäftigt sich mit den speziellen Anforderungen, die an die Herstellung von Gewebe und Gewebezubereitungen sowie von bio- und gentechnisch hergestellten Arzneimitteln und Wirkstoffen einschließlich der im Rahmen der Gewinnung erforderlichen Laboruntersuchungen gestellt werden. Das sind z. B. Arzneimittel, die Gewebe sind oder enthalten (wie Knochen, Knochenmark Herzklappen, Augenhornhaut oder Keimzellen aber auch Chondrozyten- und Leberzellpräparate), Zelltherapeutika, Tissue Engineering Produkte, durch Zellen produzierte, rekombinante und nicht rekombinante Proteine und Polypeptide, monoklonale Antikörper, Impfstoffe, Gentherapeutika oder Arzneimittel aus transgenen Tieren. Gerade der Themenbereich Gewinnung und Verarbeitung von Gewebe gewinnt an Bedeutung und spielt auch in den BwKrhs eine immer größer werdende Rolle.
Die EFG „Blut und Blutprodukte“ befasst sich mit allen Fragestellungen, die sich aus der Umsetzung der gesetzlichen Grundlagen in Bezug auf die Spende, Verarbeitung, Lagerung und Prüfung von Blut und Blutprodukten wie Erythrozyten- und Thrombozytenkonzentrate, gefrorenes Frischplasma und Produkte aus der Plasmafraktionierung, Granulozyten- und Lymphozytenpräparate oder Blutstammzellen ergeben. Das sind beispielsweise Herstellungsverfahren für Blutprodukte, Anforderungen an Blutspendeeinrichtungen einschließlich Eigenblutbanken, an Nabelschnurblutentnahmen und Nabelschnurblutbanken, an die plasmaverarbeitende Industrie einschließlich Plasmapheresezentren oder an infektionsserologische und immunhämatologische Laboratorien.
Zusammenfassung
Während in den 1980er Jahren noch die Revision der Bundeswehrapotheken den Schwerpunkt der Tätigkeiten des AMÜBBw darstellte, ist mittlerweile die Schnittstelle Arzt-Apotheker deutlich in den Vordergrund seiner Überwachungsaufgaben gerückt. Das ist zum Einen der stärkeren Ausrichtung der Apotheken auf die qualitätsgesicherte pharmazeutische Dienstleistung und zum Anderen den zusätzlichen Überwachungsaufgaben geschuldet, die sich insbesondere aus dem Transplantations-, dem Gewebe-, dem Transfusions- und dem Medizinproduktegesetz ergeben.
Datum: 31.07.2013
Quelle: Wehrmedizin und Wehrpharmazie 2013/2