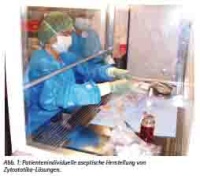
ARZNEIMITTELHERSTELLUNG IN DER BUNDESWEHR
Die Sanitätsmaterialversorgung der Bundeswehr im Einsatz und Grundbetrieb stellt eine der wesentlichen Kernfähigkeiten des Sanitätsdienstes der Bundeswehr dar. Zur Sicherstellung einer ordnungsgemäßen und nachhaltigen Sanitätsmaterialversorgung betreibt der Sanitätsdienst Bundeswehrapotheken, die befähigt sind, pharmazeutische Produkte selbst herzustellen.
Unter pharmazeutischen Produkten versteht man Arzneimittel, einschließlich Blutzubereitungen und medizinischer Gase, Medizinprodukte, Dermopharmazeutika sowie die als Biozid einzustufende Repellent-Lotion der Bundeswehr.
Die Kommission der Europäischen Gemeinschaften, die Food and Drug Administration in den USA sowie das Bundesamt für wirtschaftliche Landesversorgung der Schweizer Eidgenossenschaften weisen seit Jahren auf die zunehmende Gefahr von Arzneimittelengpässen hin. Als Folge der Globalisierung auf dem Arzneimittelmarkt wird ein Großteil der in der Bundesrepublik Deutschland konsumierten Arzneimittel, aber auch der für deren Herstellung erforderlichen Wirkstoffe (insbesondere Antibiotika mit einem Anteil von
80 %) in Fernost produziert. Lieferengpässe infolge des Ausfalls dieser Produktionsanlagen bzw. ungünstige politische Rahmenbedingungen können daher schnell die Arzneimittelversorgung gefährden. Darüber hinaus ist die Arzneimittelbevorratung einiger Mitgliedsstaaten der Europäischen Union zur sanitätsdienstlichen Versorgung in der Folge von Angriffen mit biologischen oder chemischen Kampfstoffen teilweise unvollständig und unzureichend.
Die Herstellung pharmazeutischer Produkte ist durch einen Erlass des Referats III 5 des Führungsstabes Streitkräfte im Bundesministerium der Verteidigung geregelt. Auf der Basis einer vorgenommenen Risikobewertung umfasst der darin festgelegte Herstellungsumfang in erster Linie solche Produkte, bei denen die Eintrittswahrscheinlichkeit einer Nichtbelieferung am Markt aufgrund einer Monopolstellung des Lieferanten relativ hoch ist und/oder die Auswirkung einer Nichtbelieferung dramatisch wäre. Die Festlegung des Spektrums der herzustellenden pharmazeutischen Produkte erfolgt auf der Grundlage ärztlicher Forderungen aus den Konsiliargruppen und Spezialinstituten für den medizinischen ABC-Schutz sowie der Zentralen Arzneimittelkommission der Bundeswehr.
Arzneimittelherstellung im apothekenüblichen Maßstab
Alle Bundeswehrapotheken im In- und Ausland (Einsatz) haben die Fähigkeit, sogenannte Rezeptur- und Defekturarzneimittel herzustellen. Die Rezepturherstellung erfolgt patientenindividuell auf der Grundlage einer ärztlichen Einzelverordnung. Rezepturarzneimittel werden in der Regel dann verordnet, wenn ein entsprechendes Fertigarzneimittel nicht verfügbar ist. Dies bietet dem Arzt die Möglichkeit, auf Besonderheiten des Patienten bei der Therapie optimal einzugehen.
Als weitere patientenindividuelle Zubereitungen werden Zytostatika zur Krebstherapie in den Bundeswehrkrankenhausapotheken hergestellt. In enger Zusammenarbeit mit den onkologischen Fachabteilungen werden nach einem von ärztlicher Seite festgelegten, auf die Art der Krankheit und die gesundheitliche Konstitution des Patienten zugeschnittenen Therapieschema, gebrauchsfertige Infusions- und Injektionslösungen, überwiegend aus gefriergetrockneten Pulvern oder durch Herabverdünnen von Konzentraten, qualitätsgesichert unter aseptischen Bedingungen zubereitet. Durch die Zentralisierung der Zytostatika-Herstellung in der Apotheke kann man sowohl den hohen hygienischen Anforderungen als auch den arbeitsschutzrechtlichen Bestimmungen im Umgang mit zelltoxischen Wirkstoffen in optimaler Weise gerecht werden.
Sofern bestimmte Rezepturarzneimittel häufiger verordnet werden, sieht die Arzneimittelgesetzgebung die Möglichkeit der Defekturherstellung vor. Hierbei handelt es sich um eine Vorratsherstellung, die einen Umfang von 100 abgabefertigen Packungen pro Tag nicht übersteigen darf.
Um die pharmazeutische Qualität der Rezeptur- und Defekturarzneimittel sicherzustellen, werden diese nach den Vorgaben der Apothekenbetriebsordnung hergestellt und im apothekeneigenen Labor geprüft. Herstellung oder Prüfung erfolgen nach den anerkannten pharmazeutischen Regeln, z. B den Arzneibüchern oder dem Neuen Rezepturformularium. Alle qualitätsrelevanten Herstellungsschritte und die Prüfung sind in schriftlichen Anweisungen im Rahmen des apothekeninternen Qualitätssicherungssystems festzulegen.
Herstellung über den apothekenüblichen Maßstab hinaus
In der Bundeswehrkrankenhausapotheke Ulm werden Arzneimittel auch über den Defekturmaßstab hinaus hergestellt. Seit Mitte des letzten Jahrzehntes findet die Herstellung dort in einem Apothekengebäude statt, das neben den Räumlichkeiten einer Krankenhausapotheke über einen Herstellungsbereich mit moderner Pharmatechnik verfügt. Das Kernstück bildet dabei der nur über eine mehrstufige Schleuse zugängige Sterilbereich, in dem unter hohen hygienischen Reinraumbedingungen parenterale Lösungen hergestellt werden können. Daneben lassen sich in Ulm auch Tabletten, nicht-sterile Lösungen, Gele, Salben und Cremes im Produktionsumfang eines mittelständischen zivilen Pharmaunternehmens herstellen.
Sobald das Ausmaß der Arzneimittelherstellung den apothekenüblichen Betrieb überschreitet, bedarf es einer Herstellungserlaubnis gemäß § 13 Arzneimittelgesetz (AMG). Diese wurde der Bundeswehrkrankenhausapotheke Ulm erstmals 2006 produktbezogen für die Tablettenherstellung erteilt und seitdem sukzessive um nicht-sterile Lösungen sowie endsterilisierte Injektions- und Infusionslösungen erweitert. Die letztgenannten parenteralen Arzneiformen bilden zwischenzeitlich den Schwerpunkt der Arzneimittelherstellung in Ulm. Hierzu zählen beispielsweise die Atropin-Injektionslösungen in verschiedener Stärke als Antidot bei Nervenkampfstoffvergiftungen, Midazolam-Injektionslösung als Antikonvulsivum oder das Antibiotikum Metronidazol-Infusionslösung. Die in der Bundeswehrkrankenhausapotheke Ulm hergestellten Fertigarzneimittel werden grundsätzlich für den Einsatzvorrat produziert und, mit Ausnahme bestimmter Notfallarzneimittel, größtenteils vor Erreichen des Verfalldatums im Rahmen der unentgeltlichen truppendienstlichen Versorgung verbraucht.
Die Erteilung einer Herstellungserlaubnis ist an die Einhaltung einer Vielzahl von gesetzlichen Regularien geknüpft. Allen voran ist hierbei die Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) zu nennen. Mit ihr wurde der EG-Leitfaden der Guten Herstellungspraxis (Good Manufacturing Practices – GMP) in nationales Recht umgesetzt. Auch für die Bundeswehrkrankenhausapotheke Ulm gelten die AMWHV und der EG-GMP-Leitfaden uneingeschränkt als Standard. Eine wesentliche Forderung dieser Regelwerke ist das Einrichten und Betreiben eines funktionierenden Qualitätssicherungssystems, in dem für jedes Verfahren mit Auswirkung auf die Qualität des hergestellten Produktes eine schriftliche Anweisung erstellt werden muss. Über die Durchführung der Verfahren sind umfangreiche Aufzeichnungen zu führen. Dies führte dazu, dass GMP nicht selten auch als Abkürzung für „Große Mengen Papier“ gedeutet wird.
Abb. 2: Automatisiertes Verschmelzen von Ampullen nach Abfüllung von Injektionslösung.
Vor jeder Erweiterung der Herstellungserlaubnis erfolgt in der Regel eine aufsichtsbehördliche Besichtigung der Betriebsstätte, bei der die sach- und fachgerechte Durchführung und Dokumentation der Herstellungsprozesse und der Qualitätskontrolle durch den Arzneimittelüberwachungsbeauftragten der Bundeswehr als zuständige Behörde vor Ort geprüft wird. Um sicher zu stellen, dass die Bewertung unter den gleichen strengen Kriterien wie im zivilen Bereich erfolgt, wird für die behördliche Begehung gelegentlich ein ziviler GMP-Inspektor als externer Sachverständiger hinzugezogen.
Über die Herstellung der oben genannten Antidot- und Antibiotika-haltigen Zubereitungen hinaus, sind in Ulm Vorbereitungen getroffen, um im Bedarfsfall mit geringer Vorlaufzeit nicht marktverfügbare, einsatzrelevante Notfallarzneimittel bereitstellen zu können. Hierzu zählen beispielsweise Ribavirin-Lösung zur Therapie von Krim-Kongo-Hämorrhagischem Fieber und Chinindihydrochlorid-Lösung, welche bei komplizierten Verlaufsformen der Malaria tropica als ein Mittel der Wahl gilt. Auch im Zuge der Ausstattung der deutschen Einsatzkräfte Mali konnten diese beiden Arzneimittel innerhalb von wenigen Wochen aus der Eigenherstellung zur Verfügung gestellt werden.
Grundstoffbevorratung
Für Arzneimittel, die lediglich im Krisen- oder Katastrophenfall benötigt werden oder die wegen Verlagerung der Wirkstoffproduktion von Lieferengpässen betroffen sein können, wird zunehmend das Ziel verfolgt, Wirk- und Hilfsstoffe sowie Packmittel einzulagern.
So lagern in den Bundeswehrkrankenhausapotheken beispielsweise bereits jetzt schon größere Mengen des antiviral wirksamen Oseltamivirphosphat inkl. der zur ad hoc-Herstellung einer oralen Lösung im Falle einer Grippepandemie benötigten Packmittel und Etiketten. In der Zentrallogistik wird Natriumthiosulfat als Ausgangstoff für eine Infusionslösung als Antidot bei Cyanid-Vergiftungen bevorratet.
Weitere Wirk- und Hilfsstoffe sowie Packmittel sollen den Notfallvorrat in naher Zukunft ergänzen. Durch einen regelmäßigen Umschlag des eingelagerten Materials bei der Routineherstellung von Fertigarzneimittel, kann in vielen Fällen eine „Überlagerung“ und Entsorgung vermieden werden.
Arzneimittelherstellung im Einsatz
Auch die Bundeswehrapotheken in den Einsatzlazaretten Marzar-e-Sharif und Prizren verfügen über Räumlichkeiten und Ausstattung zur Herstellung von Arzneimitteln, die in etwa denen einer Bundeswehrapotheke im Inland entsprechen. In der täglichen Routine beschränken sich die Herstellungstätigkeiten in der Regel auf dermatologische Verordnungen sowie die Defekturherstellung von beispielweise antiseptischen Lösungen und Gelen für den Klinikbedarf. Darüber sind die Einsatzapotheken mit Herstellungssätzen für einsatzrelevante Notfallarzneimittel ausgestattet, wie z. B. für eine Trinklösung mit dem oben bereits genannten Wirkstoff Oseltamivir oder Eisenhexacyanoferrat („Berliner Blau“)-Kapseln als Dekorporationstherapeutikum bei Radionuklid-Vergiftungen. Die Sätze enthalten das für die Herstellung erforderliche Material inklusive der Herstellungsutensilien sowie eine detaillierte Anleitung und einen Protokollvordruck für die ordnungsgemäße Dokumentation. Durch die Lagerung von Trockensubstanzen in Sätzen wird eine deutliche Verlängerung der Verwendbarkeit gegenüber fertigen, insbesondere flüssigen Zubereitungen erreicht.
Die in der Einsatzapotheke eingeplanten Sanitätsoffiziere Apotheker (SanOffzApotheker) und Sanitätsfeldwebel Pharmazeutisch-technische Assistenten (SanFw PharmTAss) werden in einem 2-wöchigen praktischen Lehrgang auf die Herstellung wehrmedizinisch relevanter Produkte im Einsatz, mit Schwerpunkt auf Notfalltherapeutika, vorbereitet. Dieser Lehrgang findet zweimal jährlich in einem eigens hierfür an der Sanitätsakademie in München aus Einsatzcontainern und Zelten aufgebauten Herstellungsbereich statt.
Herstellung von Sauerstoff
Im Einsatzlazarett Mazar-e-Sharif betreibt die Bundeswehr eine Sauerstofferzeugungsanlage. Auch die Versorgungs- und Instandsetzungszentren werden gegenwärtig mit Sauerstofferzeugungs- und -abfüllanlagen ausgestattet. Diese Anlagen ermöglichen die Herstellung von 93 %-igen Sauerstoff nach dem Molekularsiebverfahren in Arzneibuchqualität einschließlich der Abfüllung in Druckgasflaschen zur Sicherstellung der Versorgung der sanitätsdienstlichen Einrichtungen der Ebenen 1 bis 3 und von Verwundetentransportmitteln. Die Einweisung in die Herstellung von Sauerstoff erfolgt im Rahmen eines einsatzvorbereitenden Lehrgangs.
Regulatorische Voraussetzungen
Wie im zivilen Bereich darf auch die Bundeswehr über den apothekenüblichen Maßstab hinaus hergestellte Fertigarzneimittel nur mit arzneimittelrechtlicher Zulassung in den Verkehr bringen. Für einen Teil der Produkte kann man hierfür Standardzulassungen nutzen. Darüber hinaus hält die Bundeswehr jedoch auch eigene Zulassungen. Pharmazeutischer Unternehmer und Zulassungsinhaber in der Bundeswehr ist das Kommando Sanitätsdienst der Bundeswehr; die Aufgabenwahrnehmung erfolgt dort durch die Unterabteilung V. Wie in einer Zulassungsabteilung eines zivilen Pharmaunternehmens müssen die Zulassungsunterlagen an die sich ständig ändernden, rechtlich bindenden, regulatorischen Vorgaben angepasst werden. Darüber hinaus erfüllt die Unterabteilung V die umfangreichen gesetzlichen Pharmakovigilanzpflichten, legt Inhalt und Form der Gebrauchs- und Fachinformationen fest und gibt mit dem Qualitätssicherungshandbuch der Wehrpharmazeutischen Herstellung der Bundeswehr wesentliche Rahmenbedingungen für die Herstellung pharmazeutischer Produkte in der Bundeswehr vor.
Herstellung von Blutzubereitungen
Neben Arzneimitteln mit chemisch definierten Wirkstoffen, stellt die Bundeswehr auch Blutzubereitungen her. Die Herstellung erfolgt in der Abteilung V des Zentralen Instituts des Sanitätsdienstes der Bundeswehr, dem Blutspendedienst der Bundeswehr. Das Spektrum der dort hergestellten Blutzubereitungen umfasst leukozytendepletierte Erythrozytenkonzentrate sowie Gefrorenes Frischplasma. Die Erythrozytenkonzentrate werden klassisch durch Trennung von Vollblutspenden und seit 2012 auch mittels Hämapherese hergestellt. Bei Letzterer handelt es sich um ein Verfahren, bei dem die Trennung des Vollblutes maschinell bereits in situ, d. h. während der Spende erfolgt. So kann dem Patienten hierbei anfallendes Plasma wieder zurückgeführt werden. Aufgrund der dadurch geringeren Volumenbelastung des Spenders können im Gegensatz zur Vollblutspende mit einem Spendetermin zwei Erythrozytenkonzentrate gewonnen werden. Für die genannten Blutzubereitungen hält die Bundeswehr eigene Zulassungen.
Aktuell wird angestrebt, beim Blutspendedienst der Bundeswehr ein Verfahren zur Herstellung von kryokonservierten Thrombozytenkonzentraten zu etablieren und hierfür auch eine arzneimittelrechtliche Zulassung in Deutschland zu erlangen. Durch das Einfrieren bei -80°C kann die Haltbarkeit von Thrombozytenkonzentraten von vier Tagen auf zwei Jahre gesteigert werden, wobei der erforderliche Auftauprozess nur kurze Zeit in Anspruch nimmt. Das ermöglicht eine Bevorratung solcher Produkte im Einsatz. Gerade für schwerverletzte Soldaten mit hohen Blutverlusten wird die ärztliche Versorgung damit deutlich verbessert. Das Projekt „Kryokonservierte Thrombozytenkonzentrate“ der Bundeswehr erfährt eine sehr intensive Unterstützung durch die niederländische Militärblutbank in Leiden. Das niederländische Militär setzt kryokonservierte Thrombozytenkonzentrate bereits seit Jahren mit Erfolg in Auslandseinsätzen ein und stellt dankenswerterweise bis zum Zeitpunkt der Zulassungserteilung für die Bundeswehr auch die Versorgung im Einsatzlazarett in Mazar-e-Sharif sicher.
Zusammenfassung
Vorrangiges Ziel der Herstellung pharmazeutischer Produkte in der Bundeswehr ist es, schwer oder nicht marktverfügbare, wehrmedizinisch relevante Arzneimittel oder dringend benötigte Arzneimittel, bei denen es zu einem Versorgungsengpass kommen kann, verfügbar zu machen. Hierbei wird den Anforderungen im Einsatz im besonderen Maße Rechnung getragen. Neben den Bundeswehrapotheken betreibt die Bundeswehr hierfür in der Bundeswehrkrankenhausapotheke Ulm eine Herstellungsstätte mit Herstellungserlaubnis nach § 13 Arzneimittelgesetz, in der Arzneimittel im Maßstab eines mittelständischen Pharmaunternehmens produziert werden können. Die Herstellung von Arzneimittel, insbesondere von Notfallarzneimittel, im apothekenüblichen Umfang ist auch im Einsatz möglich. In Mazar-e-Sharif sowie in Kürze in den Versorgungs- und Instandsetzungszentren Sanitätsmaterial im Inland wird Sauerstoff 93% hergestellt und in Druckflaschen abgefüllt. Für die Herstellung von Arzneimittel ist eine Vielzahl von gesetzlichen Regelungen zu beachten, die auch für die Bundeswehr in vollem Umfang Gültigkeit besitzen. Die Unterabteilung V im Kommando Sanitätsdienst fungiert als „Zulassungsabteilung“. Hinsichtlich der Versorgung mit Blut wird neben der bereits etablierten Herstellung von Erythrozytenkonzentraten und Gefrorenem Frischplasma die Eigenversorgung mit kryokonservierten Thrombozytenkonzentraten durch den Blutspendedienst der Bundeswehr angestrebt.
Datum: 06.07.2013
Wehrmedizin und Wehrpharmazie 2013/2